自1999年 巴塞罗那分期提出以来,一直备受争议
BCLC早期分期的缺陷包括
1. 不考虑肝结节的位置,这是定义外科可切除性基本要素
2. 没有反映肝硬化的病因,病因对治疗的预后有影响
3. 在肝癌诊断时是基于一个可变值的测量,随着时间推移肝癌的大小是可变化的
4. 并没有考虑Child C,肝硬化肝癌患者肝移植的可能性,尽管在米兰标准之内
5. 没有反映出TACE的禁忌症
6. 单结节肝切除的推荐仅仅在缺乏门静脉高压超早期(BCLC 0),而早期(BCLC A)可能门静脉高压并不反映已切除病人的生存率
7. 推荐非常早期(BCLC 0)和早期(BCLC A)肝切除,但是被选择肝切除病人中甚至在更晚期的患者有良好的生存
8. . 没有考虑治疗顺序或联合治疗
9. BCLC B 的肿瘤负荷和肝功能太过宽泛
10 对BCLC C期患者除了索拉非尼,没有考虑其它治疗方法
11) 对非肝硬化患者次分类系统不利
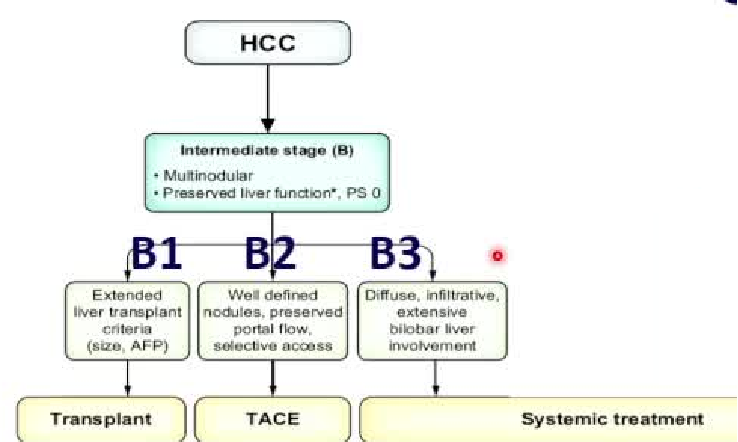
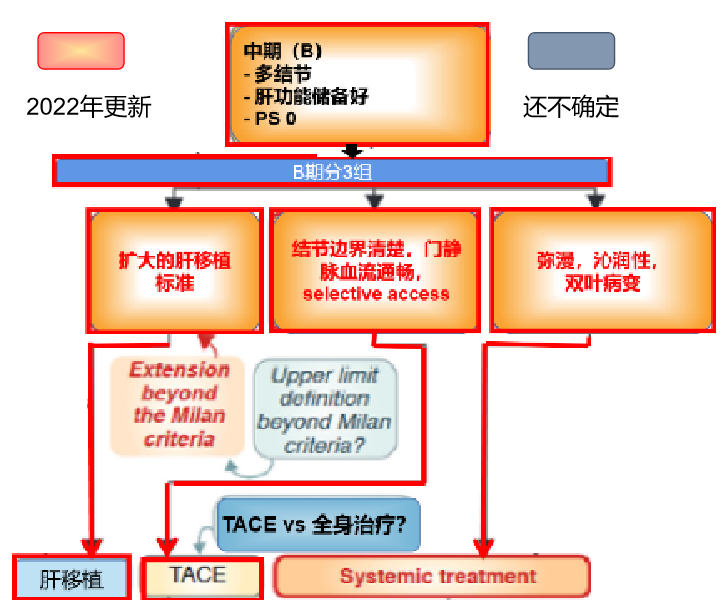
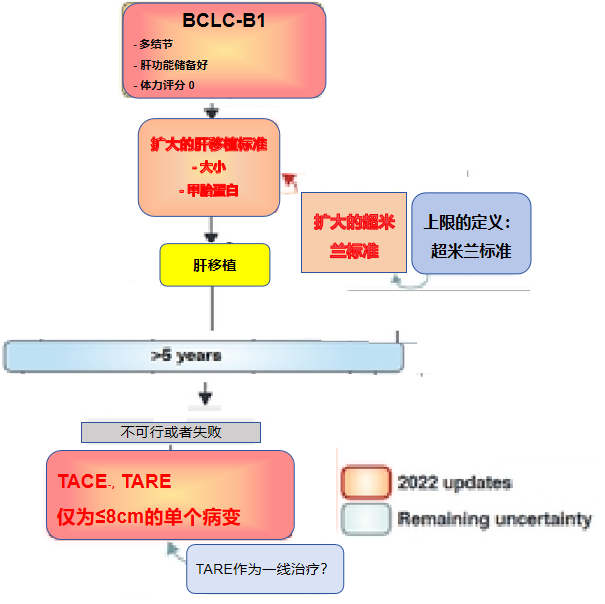
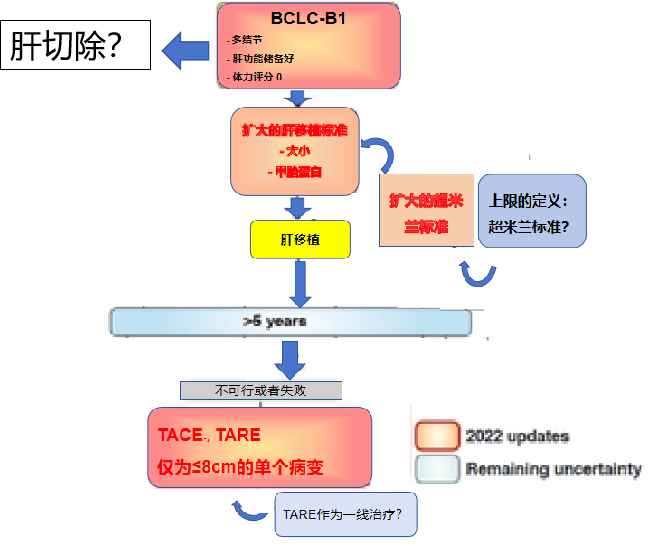
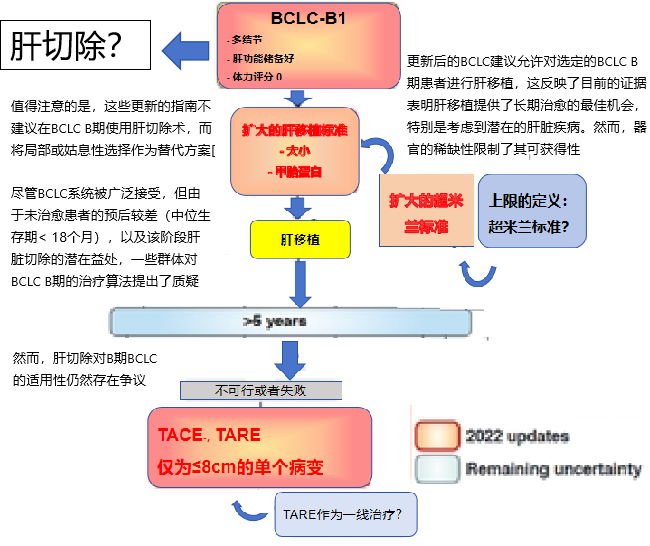
正是因为BCLC-B组的肿瘤负荷太过宽泛,最新版BCLC分期,将B期分为三个亚组,并为每组制定了优化了的独立的预后因素
BCLC-B1
|
 |
| 肿瘤数量和大小的报告以标准差为平均值,或以极差为中位数。最近9项纳入研究的患者水平数据(来自Berardi等人)。来自慈善机构的数据是根据个人交流提供的。 |
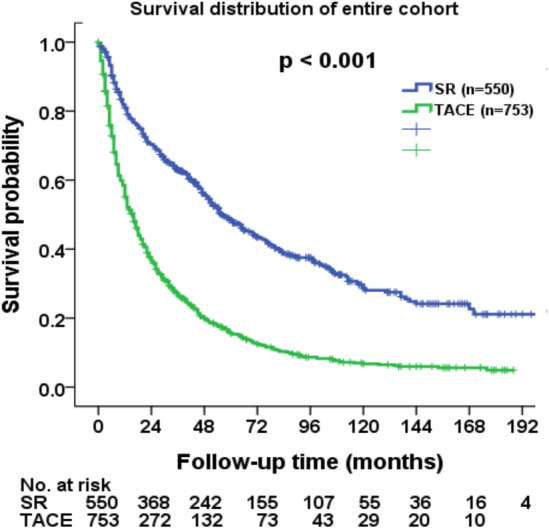
BCLC B 切除后患者的生存率
在包括423例患者的患者水平分析中,切除后的中位总生存期(OS)为50个月(95% CI 38-62个月),5年生存率为46%(下图)。
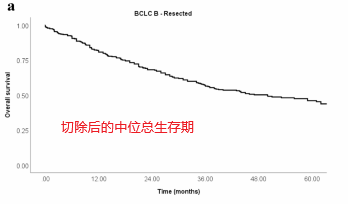
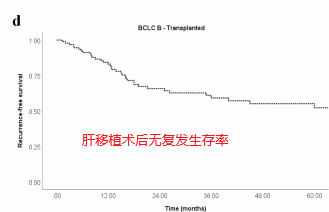
患者水平的数据分析显示无复发生存期(RFS)为15个月(95% CI 12-18个月),5年无复发率为21%(下图)。
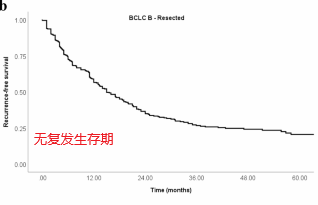
对于缺乏患者水平数据的研究,报道的肝切除术后5年生存率在30%至63%之间。在9项有患者水平数据的研究中,微血管和大血管侵犯率为0.42 (95% CI, 0.34-0.51;I2 = 66%, p < 0.01)和0.08 (95% CI, 0.03-0.21;I2 = 63%, p = 0.01)。值得注意的是,R0切除率高(0.92;95% ci, 0.82 - -0.97;I2 = 83%, p < 0.01)。
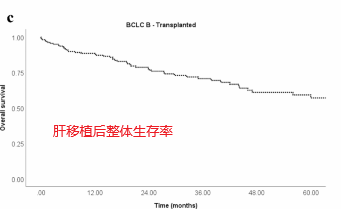 |
 |
BCLC B期 外科切除,选什么样的病人?
考虑到肝切除术在B期BCLC中并不常见,仔细的患者选择是至关重要的,我们旨在分析该患者群体中肝切除术的选择标准。
肝功能
大多数接受肝切除术的患者Child-Pugh评分为 a,发生率为0.93 (95% CI, 0.90-0.96;I2 = 90%, p < 0.01)。Child-Pugh B和MELD评分超过10在切除患者中都很少见(Child-Pugh B: 0.07;95% ci, 0.04-0.11;;I2 = 90%, p < 0.01, MELD评分:7.5;95% ci, 5.31-9.69;I2 = 0, p = 0.61)。
甲胎蛋白水平
8项研究的数据报告了AFP水平的中位数,除了一项研究外,没有超过70。此外,11项研究提出AFP临界值为400。在这些研究中,AFP水平低于400的患者比例为0.64 (95% CI, 0.58-0.70;I2 = 83%, p < 0.01)。
肿瘤数目
平均肿瘤数为2.88个(95% CI, 1.69 ~ 4.07;I2 = 0, p = 0.85),
肿瘤大小
最大肿瘤大小为6.85 cm (95% CI, 2.96 ~ 10.74;I2 = 0, p = 0.99)。值得注意的是,接受肝切除术的患者不符合米兰标准(0.99;95% ci, 0.95-1;I2 = 0, p = 0.6)。
并发症和死亡率
并发症总发生率
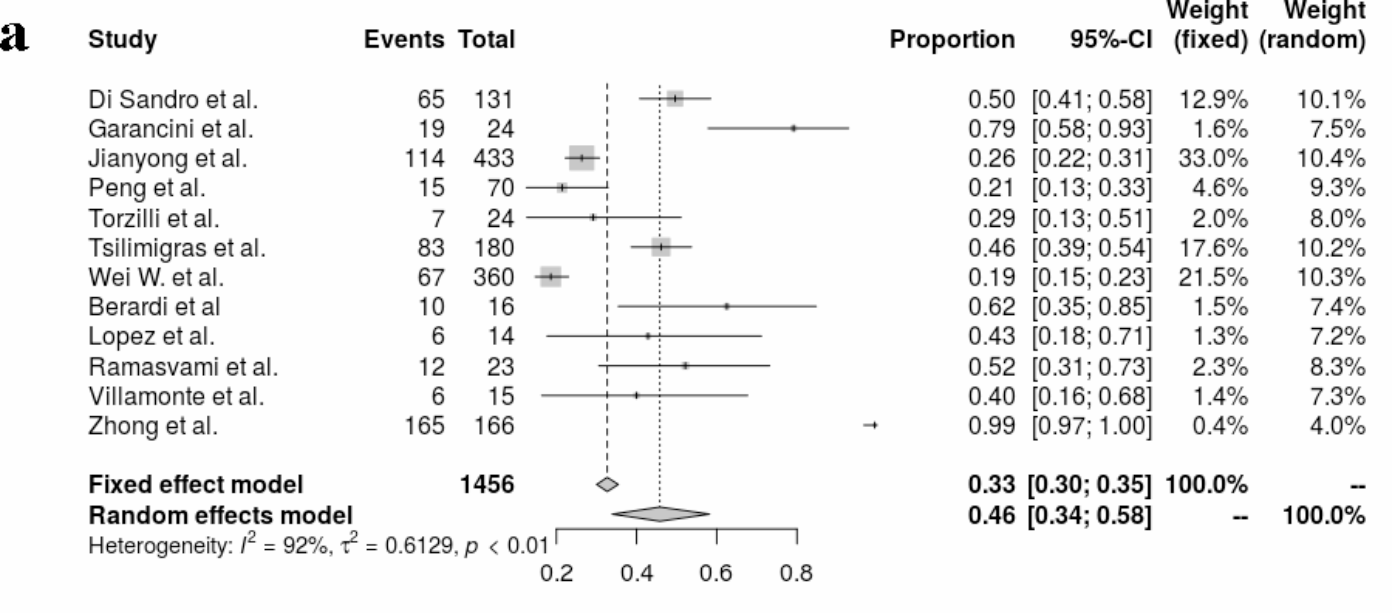 |
| 肝切除术后并发症的总发生率为0.46 (95% CI, 0.34-0.58;I2 = 92%, p < 0.01) |
严重并发症发生率
 |
|
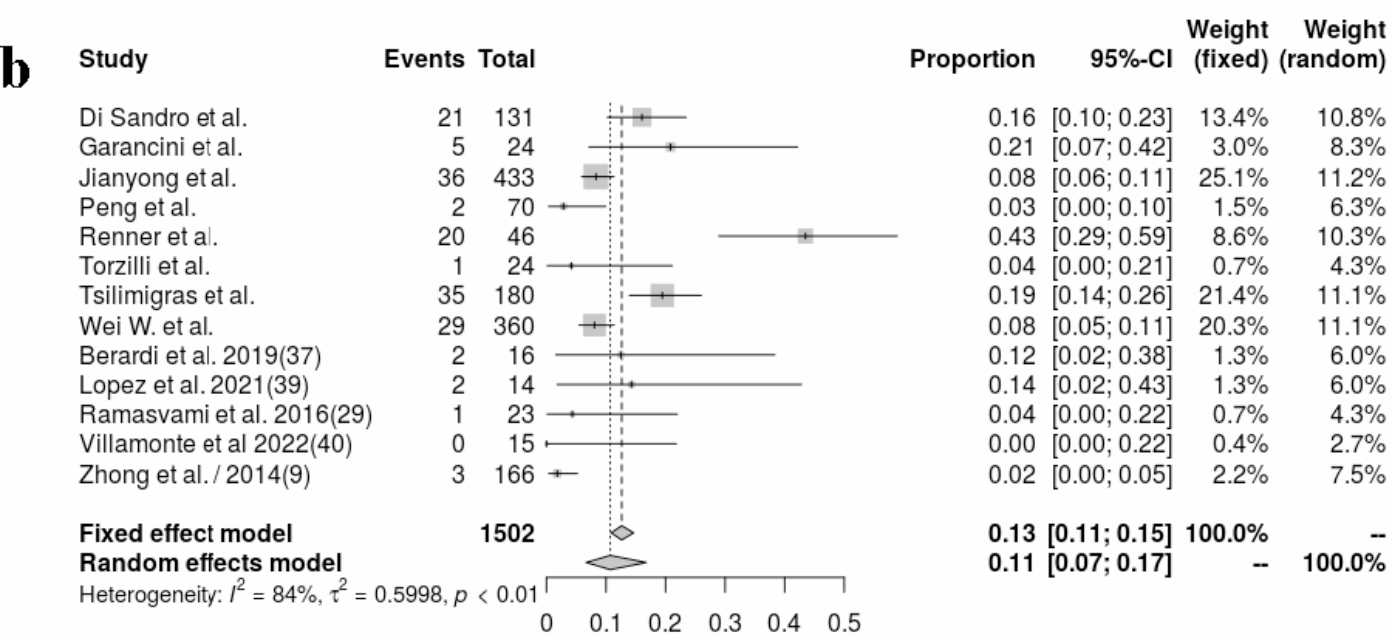
同样地,严重并发症(Clavien-Dindo分级≥3a)的合并发生率为0.11(95%置信区间,0.0-0.17;I2=84%,p<0.01)。
|
90天死亡率
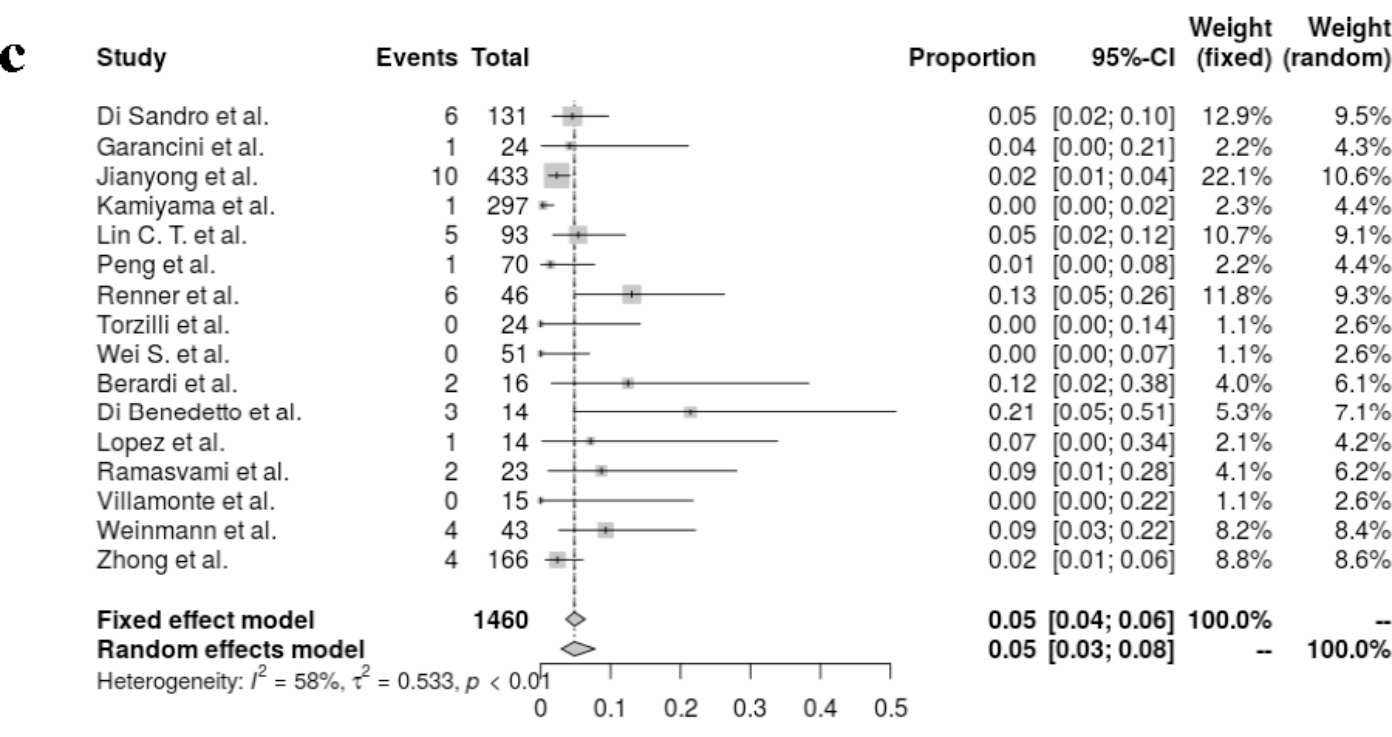 |
| 来自16项研究的分析显示,合并的90天死亡率是0.03(95%置信区间,0.03-0.08;I2=58%,p<0.01)。 |
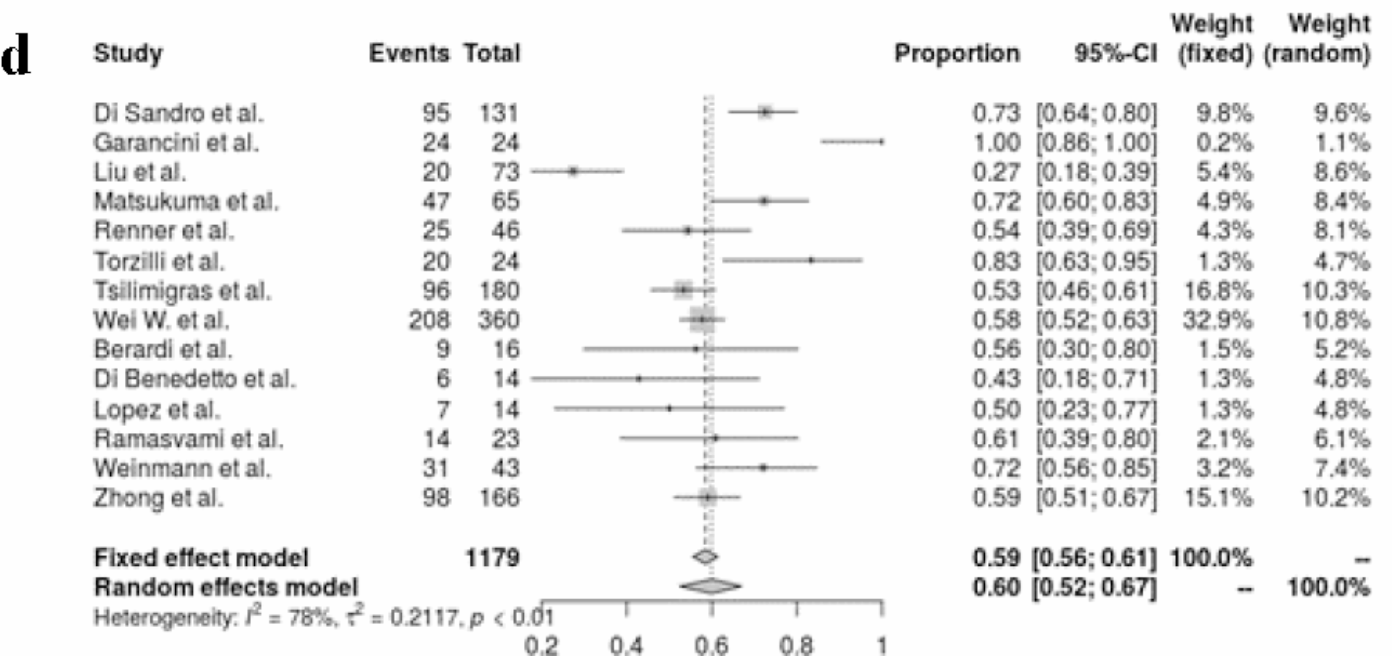 |
| 最常见的手术类型是小手术切除(minor 热section,<3段),发生率为0.60(95%置信区间,0.5-0.67;I2=78%,p<0.01)。 |
这项荟萃分析旨在解决关于BCLC分期B期肝癌患者是否适合肝切除术和移植的持续争论。研究结果显示,在选定的患者中可以安全地进行肝切除术,死亡率低,不到4%,五年生存率前景良好,为46%。然而,复发率仍然很高。未来的研究,特别是前瞻性设计的研究,需要完善患者选择标准,并优化这类患者群体肝切除术后的长期预后。
BCLB B 肝切除 与 肝功能
尽管肝切除术通常被推荐用于非常早期和早期阶段的肝癌,但对于像BCLC B这样的中期或晚期阶段的患者使用肝切除术是有争议的。这主要是由于对存在基础肝硬化的患者术后肝衰竭的担忧。然而,BCLC B期的患者往往表现出不同程度的肝功能损害,因此对每个病例进行单独评估对于确定肝切除术的资格至关重要。Lopez 等人的研究结果也支持这一点【Lopez 2024】,其中接受切除术的94%的患者Child-Pugh评分A级,报告的中位MELD评分为10分以下。
众所周知,代偿性肝硬化的患者能够很好地耐受肝脏切除术【Clavien PA 2007】。这一发现与【Lopez 2024】的研究中观察到的低死亡率(4%)和主要并发症发生率(12%)相一致。虽然Child-Pugh和MELD评分是有价值的工具,但它们并不一定是预测肝硬化患者肝脏切除术后死亡率的最佳指标。像白蛋白-胆红素梯度、肝脏体积数据或动态肝功能测试等额外的评估可以提供更精确的关于术前功能性肝脏容量的信息。不幸的是,这些数据对于这个特定的患者亚组是不可用的。然而,考虑到并发症的低发生率,合理地假设这些患者表现出保留的肝脏功能。值得注意的是,很大一部分切除手术被归类为小手术(小于3个段),这表明倾向于较小且非解剖学的手术。
BCLC B 肝切除 与 肿瘤的范围
Lopze 等人的分析表明,纳入的研究在选择肝切除术的候选者时考虑了肿瘤范围。接受肝切除术的BCLC B患者超出了米兰标准(一个病灶<5厘米或最多三个病灶每个<3厘米)。考虑到任何大小的单一肿瘤被归类为BCLC A而非BCLC B,这一发现是可以预料的,正如2011年更新版所推荐的那样。根据纳入研究中平均肿瘤数量少于3个的多结节性疾病,患者分别被分类为BCLC B,而肿瘤数量超过3个的患者未被切除。仔细的患者选择通常包括肝脏功能完好的人群,这在分析中被观察到。肝切除术显示出良好的安全性结果。这一发现以及有希望的5年生存率50%,反映了围手术期风险和生存获益之间的有利平衡。值得注意的是,这些结果超过了任何报告的姑息治疗选项[7, 8]。值得注意的是,这里观察到的5年生存率与报道的BCLC 0-A阶段切除术的生存率相当【Torzilli G 2013】。
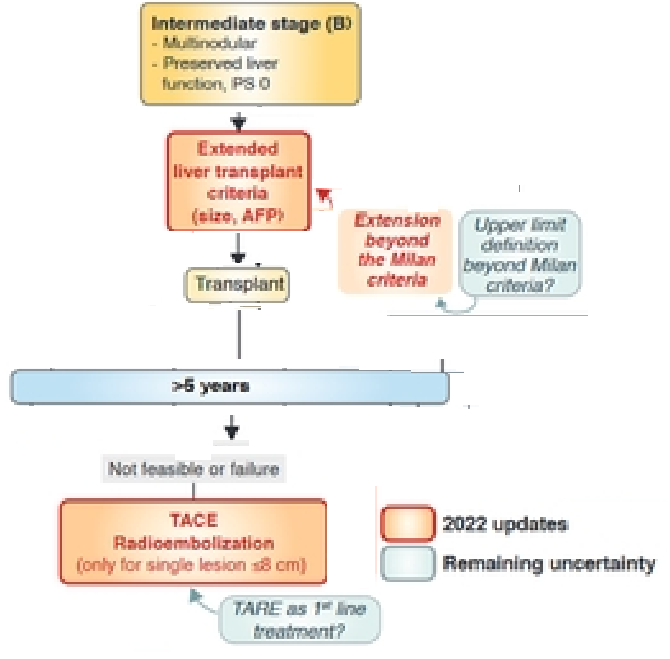
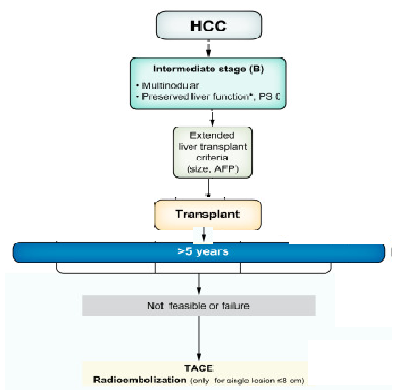
BCLC B 肝切除 与 肿瘤生物学特性(非BCLC肿瘤分期系统的有机组成部分)
肝癌的生存率不仅取决于肿瘤的大小和/或数量,还取决于肿瘤生物学特性。后者并非BCLC肿瘤分期系统的有机组成部分。BCLC中期阶段B的定义完全基于肿瘤数量,这一事实遭到了多位作者的质疑。许多先前的报告已经证明,尽管肝癌超过了当前肝移植形态学限制(例如米兰标准)【Reig M 2022】,具有有利肿瘤生物学的患者仍可获得显著的生存优势。例如,据报道使用AFP水平或形态学评估来评估肿瘤生物学【Mazzaferro V 2018】。PET扫描的结果、对降期治疗的局部区域性治疗的反应也有助于确定和选择具有有利肿瘤生物学的患者。文献中的这些有希望的数据最终成为了将肝移植纳入具有有利肿瘤生物学的BCLC阶段B患者的治疗算法的原因。目前,更新版本指出TACE作为唯一治疗或桥接选项,而肝切除可能是对于具有BCLC阶段B肝癌的患者的一种合理治疗选项。值得注意的是,荟萃分析包括一项随机对照试验,该试验观察到在BCLC B和BCLC C患者的联合分析中,与TACE相比,肝切除后生存率有所提高【Hyun MH 2018】。仅包括BCLC B患者的亚组分析证实了与TACE相比,切除术的优势【Hyun MH 2018】。尽管如此,肝切除并不推荐对所有BCLC B期的患者都进行肝切除术,而且TACE和肝切除术的选择可能在不同国家和医疗保健系统之间有所不同。在移植等待时间只有几个月的国家,可能会继续选择TACE作为过渡到移植的手段,或者评估肿瘤生物学。然而,如果肝移植不可用或者等待名单上的时间非常长,肝切除可能是一个合理的策略。然而,在接受过患者中,肿瘤复发很常见。尽管【Lopez 2024】研究没有关于复发治疗的数据,但长期结果表明需要进一步治疗复发。(BCLC B 肝切除后需要惯序治疗的方案,缺少惯序治疗或联合治疗的方案是BCLC B的一个缺项)
虽然由于同时治疗了基础肝病,肝脏移植后的复发率通常较低,但大多数中心在进行扩展标准肝脏移植时并不按照BCLC系统对患者进行分类,即使他们经常应用扩展标准。这表明肿瘤生物学可能是选择扩展标准肝脏移植的最重要因素,而肝功能和患者表现状态可能潜在地被强调得较少,这可能是因为这些问题在移植过程中得到了解决。这可以解释为什么在HCC患者中进行扩展标准肝脏移植时,BCLC分期系统的使用并不常见。
【Lopez 2024】综述有几个局限性。首先,所有纳入的研究都是回顾性的,因此存在选择偏倚。虽然平均肿瘤数为3个,但有多结节性疾病的患者可能影响了预后。由于患者的选择是根据肿瘤生物学、肝功能和表现状况进行的,因此研究结果不能推广到所有b期BCLC患者。此外,由于患者在切除之前或之后有其他治疗方式,例如TACE,因此不能排除重叠治疗方式。然而,在探讨b期BCLC的肝移植时,只有少数研究被确定,并且荟萃分析主要基于现有的患者水平数据。因此,所有关于肝移植在这一特定阶段有效性的结果都应谨慎解释。【Lopez 2024】分析旨在评估肝切除和移植治疗b期BCLC的有效性,并不是故意对两种手术进行直接比较。在他们看来,没有证据支持在该患者群体中使用病例对照研究来比较切除与移植。事实上,该荟萃分析中没有一项研究报告了b期BCLC的肝切除和移植数据,这一发现支持了仅关注单臂研究的决定。
总结【Lopez 2024】荟萃分析显示,精心挑选的BCLC B期HCC患者可以安全地进行肝切除术,5年生存率为50%,5年无复发生存率为21%。值得注意的是,观察到的死亡率低于4%。这些发现支持肝切除术作为BCLC - B患者,特别是肝功能保留患者的一种有价值的治疗选择和替代方案的潜在作用。此外,在等待时间较长的地区,肝切除可能是移植的一种桥接策略。然而,由于缺乏meta分析的数据,尚无法得出这一阶段肝移植的结论。