本栏目将
1. 探讨介入放射学中设备的非标准使用情况
2. 考虑一下在何种情况下进行超说明书用药是被允许的
3. 推断何时出现超说明书用药是不可接受的
在医学领域,许多器械和药物的使用往往都是“非官方”的。 例如,对于未获得监管机构(如美国食品药品监督管理局)批准的患者群体或治疗手段,这种情况就属于此类情况。 示例: 普萘洛尔:静脉曲张出血的预防性治疗(包括一级预防和二级预防) 加巴喷丁:神经性疼痛 ASCO 调查:约 50% 的癌症患者在其患病过程中曾因非官方适应症而接受过化疗。 临床实践指南通常会推荐非标准用药方式【ASCO 2006】。
药物或 设备 经过监管机构批准后授权 对于特定病症的使用和销售,它既相对安全又相对有效 ,“标签” 被称为Label ,而Label off 是未经监管部门授权的
为何会存在超说明书用药的情况呢?
尽管有些器械超范围应用有充分的安全性和有效性证据,但适应症扩大的审批的步骤仍未制定出来。
- 狭窄的监管途径 - 一旦专利到期,缺乏经济激励措施 循证医学的“灰色地带”;高水平的证据难以获取,即便对于那些可能有效的治疗方法也是如此(比如针对罕见病症的治疗) 原因:没有合适的已获批准的方案可供选择 创新的速度比审批的速度要快【ESMO 2007】。
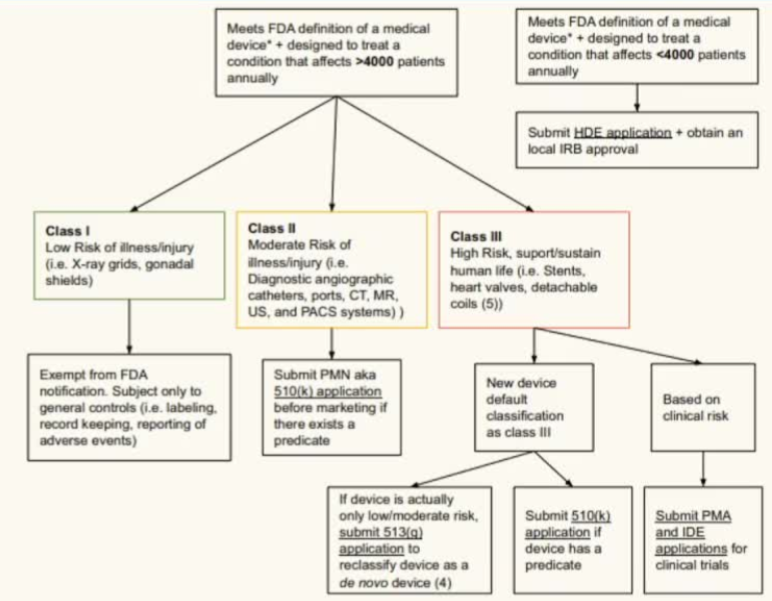
医疗器械的美国食品药品监督管理局审批路径

本文由Joshua L. Weintraub, MD, Karim Valji, MD, 和Daniel Y. Sze, MD, PhD撰写,发表在2025年3月出版的JVIR上。文章探讨了介入放射学(IR)领域创新与伦理边界之间的关系。文章指出,尽管IR领域的快速变化和广泛创新是其独特魅力所在,但这种创新精神也带来了即兴发挥与系统研究之间界限模糊的问题。随着IR成为独立的专业,并受到各种监管机构的严格审查,如何在保持创新的同时遵守更高的伦理标准成为了一个关键问题。
IR领域的创新精神
历史背景:IR自60年前首次进行治疗性操作以来,一直以其独特的创新精神著称,吸引了许多寻求更多日常即兴发挥和创造力的医学生。
实践特点:IR医生高度依赖各种设备进行操作,并且经常是患者最后的希望,因此被赞誉为医学界的“MacGyvers”。
即兴发挥与系统研究的界限
伦理挑战:虽然绝望的患者可能愿意尝试未经证实的治疗方法,但现代医学规则要求区分即兴实践和定义明确的研究。
伦理准则:《赫尔辛基宣言》作为医学研究中涉及人类受试者的伦理指南的基础文件,强调了知情同意、行善和尊重个人自主权的重要性。
监管框架与实践标准
国际准则:除了《赫尔辛基宣言》,还有国际优良临床实践指南和美国卫生与公共服务部的共同规则等补充规定。
医师权限:医生可以执行任何他们认为对患者有益的干预措施,前提是已获得知情同意。然而,患者和医生通常假设医疗设备和程序由政府监管,但实际上FDA只监管设备本身,而不是医疗实践和设备的使用方法。
设备审批机制的问题
510(k)途径:大多数IR设备通过较宽松的510(k)途径获得批准,只需证明新设备与先前批准的设备具有相同用途和技术特征即可,这可能导致未经充分验证的设备进入市场。
标签外使用:尽管有官方批准的使用范围,但设备的标签外使用在IR中一直是必要且接受的标准做法,这导致了合理创新使用与随意实验之间的灰色地带。
案例分析:CCSVI与MS
CCSVI假说:2009年提出的CCSVI假说认为,中枢神经系统静脉流出障碍是多发性硬化症的原因之一,IR医生迅速采纳了“Label off”程序,尽管缺乏高级别科学证据。
后果与反思:尽管初期有积极的个案报告,但后来的研究表明该疗法无效,甚至导致了一些患者的伤害。这一事件暴露了早期未受监管的实验带来的问题。
其他设备的使用与风险
液体栓塞剂:n-butyl cyanoacrylate (nBCA) 和ethylene vinyl alcohol copolymer (EVOH) 虽然最初用于脑动静脉畸形治疗,但在外周应用中显示出复杂的安全问题。
新型栓塞剂:新型非牛顿流体栓塞水凝胶Obsidio Conformable Embolic在用于胃肠道出血时导致严重不良事件,随后被召回以进行进一步培训。
研究与创新的区分
JVIR指南:自JVIR发布要求IRB批准的指南以来,所有提交的文章都必须包含关于批准或豁免的信息。不同规模的研究需要不同程度的IRB审查。
IRB政策不统一:不同地方的IRB政策不统一,一些文章在当地获得豁免后在同行评审过程中被判定为需要正式IRB监督的研究。
建议与解决方案
建立本地委员会:提议建立一个包括IR医生在内的本地临时委员会,评估新程序,区分研究与合理扩展已批准设备或技术,并确定是否需要正式IRB监督。
促进透明度与伦理决策:该委员会应促进透明度和伦理决策,其成员可以包括诊断放射科医生、转诊医生、医学伦理学家、法律顾问和患者代表。
结论
创新的重要性:IR的进步依赖于从业人员的创造力和发明精神,但未来的发展和扩展现在取决于更高的实践和出版标准。
区分创新与研究:区分即兴发挥和研究对于维护伦理标准、确保患者安全以及获得监管批准、临床采用和报销至关重要。
持续发展:通过建立明确的指导方针和促进IR专业人士之间的协作决策,该领域将继续以严谨和道德的方式推动边界并推进患者护理。
总结
文章核心观点在于讨论介入放射学领域中创新与伦理之间的平衡。作者指出,尽管介入放射学以其快速变革和广泛创新而闻名,但这种创新精神有时会导致即兴操作与科学研究之间的界限变得模糊。随着介入放射学成为一个独立的专业,受到越来越多的监管,如何在保持创新精神的同时遵守更高的伦理标准成为了一个重要议题。文章通过分析具体的案例,如CCSVI与MS的关系,强调了区分即兴创新与系统研究的重要性,并提出了建立本地委员会等建议,以促进透明度和伦理决策,确保患者安全,同时推动介入放射学领域的进步。
循证医学 EBM 评级采用 1 至 5 的评分标准,具体如下:、
第 1 级(a - c):由至少一项精心设计的随机对照试验所获得的证据。
第 2 级(a - c):通过精心设计的对照试验获得的非随机化数据。
第 3 级(a - b):通过精心设计的队列研究或病例对照分析研究获得的证据,最好来自多个中心或研究团队。
第 4 级:通过多个时间序列(有时伴有干预措施)获取的证据,例如案例研究。在未受控制的试验中取得的显著结果也可被视为此类证据。 •
第 5 级:由受人尊敬的权威人士提出的观点,这些观点基于临床经验、描述性研究或专家委员会的报告得出。
通常Label off 的应用,都属于较低级别的证据等级
SIR 立场声明
Society of Interventional Radioinnv Position Statement on Off-Label Use

本文是《介入放射学会》(Society of Interventional Radiology, SIR)关于“超说明书用药”的立场声明。该声明确认了医生自主临床决策权的重要性,并支持在有充分科学依据或医学意见支持的情况下,医生合法使用FDA批准的医疗器械或药物产品用于未标注的适应症。声明还涉及了第三方支付者(包括医疗保险)应如何对待这些治疗,以及医生获取有关未标注用途的准确和无偏见信息的重要性。
医生的自主临床决策权
支持医生自主权:SIR 强烈支持医生根据充分的科学证据或医学意见,合法使用 FDA 批准的医疗设备或药物产品用于未标注的适应症。
安全有效治疗:当“超说明书”使用代表安全有效的治疗时,第三方支付者应考虑这种干预为合理的必要医疗服务。
第三方支付者的责任
覆盖合理治疗:无论标签如何,第三方支付者包括 Medicare 应覆盖符合临床适当性的“超说明书”治疗。 | 



