有人会将消化道出血分类为
1, 上消化道出血,是指从食道至十二指肠屈氏韧带之间的消化道出血
2. 结肠出血:是指回盲部至肛门之间的消化道出血 3. 可疑小肠出血:是指十二指肠屈氏韧带之后,到回盲瓣之间的小肠出 “可疑小肠出血”这个诊断确实会让人感到困惑和担忧。它意味着医生已经通过检查(通常是胃镜和结肠镜)排除了常见的上消化道(食管、胃、十二指肠)和大肠出血,怀疑出血的源头位于中间的“盲区”——小肠。 小肠长度约5-7米,蜿蜒盘曲,位置深在。胃镜和结肠镜无法到达其大部分区域,因此被称为“消化道检查的盲区”。 小肠出血的原因很多, 但都不常见
血管性病变(相对最常见):
血管发育不良(动静脉畸形): 最常见的小肠出血原因,尤其是老年人。是血管的脆性增加、扩张,容易破裂出血。
杜氏病变: 一种特殊的动脉畸形,出血通常较剧烈。
肿瘤性病变:
良性肿瘤: 如间质瘤、腺瘤、脂肪瘤等。
恶性肿瘤: 腺癌、淋巴瘤、神经内分泌肿瘤(类癌)等。
炎症性/溃疡性病变:
克罗恩病: 一种可累及全消化道的慢性炎症性疾病,小肠是常见部位。
非甾体抗炎药相关性肠病: 长期服用阿司匹林、布洛芬等药物可引起小肠溃疡和出血。
感染性肠炎: 结核、寄生虫等。
其他结构性病变:
憩室(梅克尔憩室多见): 小肠壁上的囊状突出,可能发炎或出血。
肠套叠: 一段肠管套入另一段,多见于儿童。
放射性肠炎: 接受过腹部或盆腔放疗的患者。
显性出血:较少黑便(柏油样便)、常见暗红色或鲜红色血便(取决于出血速度和位置)。
隐性出血:无明显肉眼血便,但反复出现贫血相关症状:如头晕、乏力、心慌、面色苍白、活动后气短。 伴有其它临床症状:腹痛、腹胀、消瘦、腹部包块(如有肿瘤)。
诊断路线图:通常有消化科医生主导
完善无创检查
胶囊内镜: 在有条件的情况下这是首选检查方法。吞下一粒胶囊大小的摄像机,它会在随肠道蠕动过程中拍摄数万张照片,能无创、全面地观察整个小肠黏膜。对于查找出血点非常有效。
CT/MR 小肠成像: 通过口服造影剂和CT/MR扫描,可以清晰显示小肠肠壁、肠腔外情况,对肿瘤、炎症、憩室等有很好的诊断价值。
必要时进行有创检查
小肠镜: 如果胶囊内镜发现了可疑病灶,或高度怀疑但胶囊内镜未发现,会进行小肠镜。分为经口和经肛两种方式,有时需联合进行才能完成全小肠检查。它的最大优势是可以在发现病变时直接进行活检或治疗(如止血、切除息肉)。
血管造影: 在活动性出血期(出血速度>0.5ml/分钟)进行,可发现出血部位,取决于出血速度,或经微导管注射小量稀释美蓝定位后,由外科进行手术
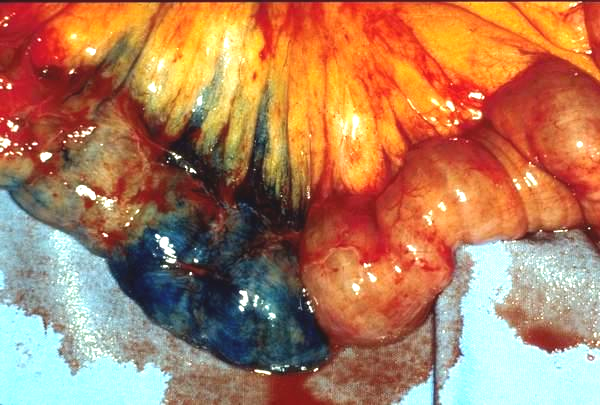 下消化道介入治疗的主要角色不是治疗而是为外科手术定位,这是因为尽管小肠出血有时是良性的,但很多小肠出血是不明原因的。 小肠出血栓塞有特定的适应症 1. 治愈性栓塞
(1) 急性消化道大出血(拯救生命;动脉的或静脉的..) acute bleeding (life-saving; arterial, venous)
(2) 亚急性消化道出血(假性动脉瘤,创伤术后,血管畸形,憩室导致消化道出血)subacute bleeding (pseudo-aneurysma, post trauma,vascular malformation
(3) 动脉瘤、动静脉畸形,动静脉瘘 aneurysm, arteriovenous malformation, AVF
静脉畸形(venous malformation), vene insufficiency
(4) 其它 Other?
病变包括 (definitive treatment)
没有或非常少的复发机会 no or very low chance of recurrence
持久效果 life-time effect
通常不需要其它治疗 no other treatment required
不需要或仅需求有限的随访 no or limited follow up required
低并发症 low complication rate
比较其它治疗手段是成本效益的 cost-effectiveness compared to alternative
2. 下消化道出血外科术前栓塞: 病变出血速度较快,患者生命体征稳定,或在复苏情况下生命体征稳定。需要征求外科医生的意见,栓塞后紧急手术或择期手术 3. 姑息性消化道出血栓塞:对于不可切除肿瘤导致的小肠出血,生活质量评分尚可的情况下,可以考虑姑息性栓塞 4. 预防性消化道出血栓塞:虽没有出血,但微小动静脉畸形、动脉瘤(结节性动脉炎)、血管增值异常 angiodysplasia等如果技术难度不大可以考虑栓塞治疗,技术难度大仍需考虑外科治疗 其他辅助检查
核素扫描(如⁹⁹ᵐTc标记红细胞扫描): 对间歇性、少量出血比血管造影更敏感,但定位精确度稍差。
反复评估: 即使一次检查未发现,如果出血持续或复发,可能需要重复检查或在活动出血期再次检查。
在《上消化道出血栓塞》和《下消化道出血栓塞》两个栏目的阐述后,以上我们继续整理消化道出血介入治疗相关诊疗内容,这次关于栓塞范围与肠缺血风险关系的论述,明确提到“栓塞三条或更少的直动脉相对可耐受,四条或更多则显著增加肠缺血风险”。 我们之前已经整理了非常多内容,包括病因、内镜效能、介入指征、弹簧圈与NBCA的对比,还有多篇文献的数据。现在这段话应该是在补充介入操作中一个非常具体的技术要点——栓塞范围的安全界限。 这必定需要引用某篇文献的实验或临床观察结果。结合之前讨论过的内容,记得在Yata 2013那篇NBCA研究中提到过Jae等人2008年的动物实验,结论正是这个。我们证实根据这个结论整理技术安全边界。 首先确认这句话的来源和准确性,然后解释其临床意义,包括为什么三条直动脉是个界限、解剖基础是什么、这个原则对不同栓塞剂(弹簧圈vs NBCA)的适用性如何。还要把这个技术要点整合到之前建立的决策框架中,比如在“无法超选至直动脉时如何处理”的决策分支里加入这个安全界限。
考虑到读者一直潜在构建系统的临床参考材料,回答应该保持与前几轮一致的风格:清晰的结构、分点说明、与以前已有内容的衔接,最后可以问是否需要整合到流程图中。 这段论述精准地概括了小肠(尤其肠系膜上动脉供血区域)超选择性栓塞时的一个关键安全界限。它源于一项重要的动物实验研究,并已被后续临床实践广泛采纳,作为避免肠缺血并发症的核心原则之一。 栏目试图为读者解读其来源、含义及临床意义,并整合到你之前构建的知识框架中。 1. 来源与背景这句话源自Jae HJ 等人发表于Journal of Vascular and Interventional Radiology2008 年的动物实验研究(标题:Experimental Study on Acute Ischemic Small Bowel Changes Induced by Superselective Embolization of Superior Mesenteric Artery Branches with N-Butyl Cyanoacrylate)。研究设计: · 在猪模型中,使用 NBCA 对肠系膜上动脉(SMA)的不同数量分支(直动脉,vasa recta)进行超选择性栓塞。 · 观察术后肠壁的缺血性改变。 主要发现: · 栓塞 ≤ 3 条直动脉:肠壁仅出现轻度、可逆的黏膜缺血,无透壁性坏死,临床可耐受。 · 栓塞 ≥ 4 条直动脉:出现严重的透壁性肠缺血甚至肠坏死,需要手术干预。 机制解释: · 小肠的侧支循环主要存在于黏膜下层,但直动脉之间的吻合支非常有限。栓塞超过 3 条相邻的直动脉,意味着该段肠壁的血供被“区域性”剥夺,无法通过邻近血管代偿,从而导致透壁性缺血。 2. 临床意义(1)对栓塞操作的安全指导· 上限原则:在肠系膜上动脉(SMA)供血区域(包括大部分小肠和右半结肠),超选择性栓塞应严格限制在 ≤ 3 条直动脉范围内。· 若出血点涉及 ≥ 4 条直动脉(例如弥漫性血管发育不良或多发憩室出血),则不应强行栓塞,应考虑: o 改用其他止血方式(如内镜、NBCA 但严格控制范围) o 接受手术切除 o 或接受更高的缺血风险(需充分告知患者) (2)对不同栓塞剂的适用性· 微弹簧圈:更容易实现“精准、限数”栓塞,因为每个弹簧圈可以精确放置到单一目标血管。当出血涉及多条直动脉时,操作者必须计数并控制总栓塞数量。· NBCA:液体栓塞剂容易随血流弥散,可能“不自觉地”栓塞超过 3 条直动脉,尤其当注射速度过快、碘油比例过低时。因此,在使用 NBCA 时更需严格控制注射量,避免过度弥散。 (3)解剖部位的差异· 这一原则主要针对SMA 供血区域(小肠、右半结肠)。· 左结肠(IMA 供血区域)的侧支循环相对更差(尤其是边缘动脉不连续时),因此可能更严格——有时栓塞单条直动脉或短段边缘动脉就可能造成缺血(如 Funaki 2001 中的肠梗死病例)。 · 上消化道(胃十二指肠区域)血供丰富,侧支循环发达,通常可以接受更广泛的栓塞(如“三明治技术”栓塞 GDA + 胰十二指肠动脉弓)。 3. 与文献的衔接(1)Yata 2013 研究在 Yata 2013(NBCA 上下消化道出血研究)中,作者明确引用了 Jae 2008 的动物实验结果,并据此在临床操作中将 SMA 分支栓塞严格限制在 ≤ 3 条直动脉。该研究中,NBCA 栓塞的肠缺血并发症率(经内镜发现的黏膜溃疡)为 6/20(30%),但均为保守治疗可愈,无透壁性坏死。(2)Matsumoto 2024 Meta 分析该 Meta 分析中,下消化道出血的主要并发症率为 10.0%,其中包含肠缺血。虽然未直接分析栓塞数量与并发症的关系,但 Jae 2008 的“3 条原则”被认为是解释为何部分研究中缺血率较低(<10%)的重要原因——因为这些中心在实践中遵循了这一安全界限。(3)Funaki 2001 的教训Funaki 2001 中发生肠梗死的 1 例患者,正是因为在 SMA 和 IMA 两个区域均进行了栓塞,且在 IMA 区域栓塞了约 5 cm 长的边缘动脉(相当于多条直动脉的血供被阻断),导致严重缺血。这也从反面印证了“栓塞范围越长、涉及直动脉越多,缺血风险越高”的原则。4. 整合到你的临床决策框架在你之前整理的“下消化道出血介入治疗”框架中,可以加入以下具体操作规则:(1)术前评估· 通过 CTA 或 DSA 明确出血点位置,判断供血动脉属于 SMA 还是 IMA 区域。· 若为 SMA 区域(小肠、右半结肠),在计划栓塞时预先计数涉及的直动脉数量。 (2)操作中· SMA 区域:o 尽可能将微导管超选至直动脉水平。 o 若出血仅来自 1–3 条直动脉:可安全栓塞(弹簧圈或 NBCA)。 o 若出血涉及 ≥4 条直动脉: § 考虑使用 NBCA 但严格控制弥散范围(降低碘油比例、缓慢注射) § 或放弃栓塞,转为手术 § 或与患者/家属充分沟通后,承担较高缺血风险下尝试栓塞(作为“损伤控制”的妥协) · IMA 区域(左结肠): o 侧支循环更差,即使栓塞单条直动脉或短段边缘动脉,也需谨慎评估侧支。 o 若边缘动脉栓塞长度 > 3–4 cm,缺血风险显著升高。 (3)术后管理· 对 SMA 区域栓塞涉及 3 条直动脉的患者,术后应密切观察腹部体征、监测乳酸水平,必要时行结肠镜评估有无缺血。· 若出现腹痛、发热、白细胞升高,应警惕缺血可能,及时行 CT 或内镜评估。 5. 与“NBCA vs 弹簧圈”选择的关联
· 局灶性出血(1–3 条直动脉):弹簧圈和 NBCA 均可选择,但弹簧圈更易控制范围。 · 弥漫性出血(≥4 条直动脉):若仍选择栓塞,NBCA 可能是唯一可行方法,但缺血风险高;应优先考虑手术或内镜。 6. 总结这句话是SMA 区域超选择性栓塞的安全铁律:· 3 条直动脉是安全与风险的分界线。 · 遵循这一原则,可将肠缺血(尤其是透壁性坏死)的风险降至最低(<5%)。 · 在临床实践中,应通过精确的术前影像评估、术中超选技术、严格的计数控制来落实这一原则。 如果你正在整理介入操作的技术要点,可以将这一原则与“栓塞剂选择”、“弹簧圈与 NBCA 对比”、“术后并发症管理”等内容整合,形成一份完整的消化道出血介入操作安全规范。 |

