1. 旧瓶装新酒和上消化道出血栓塞不同,下消化道出血是个“旧观念”:早在20世纪70年代初,就有学者尝试用栓塞治疗下消化道出血,但当时没有微导管,使用的导管较粗(5F),无法超选择到出血的末梢血管,尽管有Rosch 1972 和 Bookstein(1974) 改良的凝血块作为栓塞材料,导致肠梗死发生率高达13-33%【Rosch 1972 Bookstein(1974 VP Chuang 1979】。因此,栓塞技术被弃用,转而采用血管加压素灌注(通过导管持续输注药物收缩血管止血)。 微导管的引入,开辟了一个“新时代”:20世纪90年代,微导管(3F,同轴技术)的出现,使介入医生能够将导管超选择到直动脉(vasa recta) 或更末梢的出血点进行精准栓塞。这既阻断出血,又通过侧支循环保留肠壁血供,肠梗死发生率降至接近0%。因此,栓塞重新成为严重下消化道出血的一线血管内治疗方法。在当时微导管的诞生在下消化道出血栓塞被称为"一个时机已到的旧观念”  2. 患者分层文章将下消化道出血患者分为四类,这与我们之前讨论的“分层处理”逻辑一致:
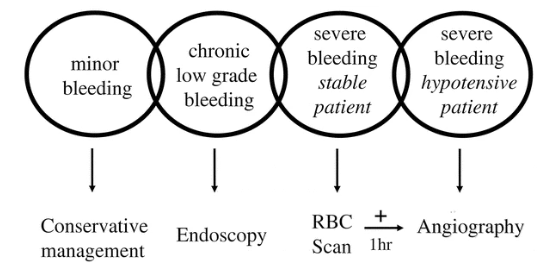 这一点与其它栏目之前整理的“严重出血稳定→CT;严重出血不稳定→血管造影”的思路完全一致,只是本文更强调用核素显像作为“稳定但严重出血”的定位手段(在CT血管成像尚未普及时的主流做法)。 微导管远端栓塞主要是出血量大,生命体征稳定或不稳定的患者 3. 微导管远端栓塞病因与临床特点
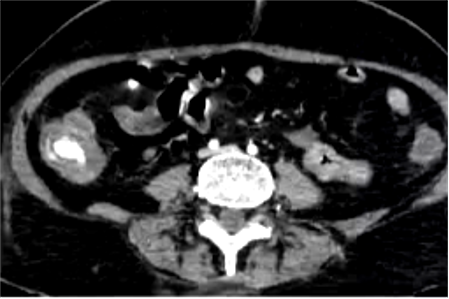
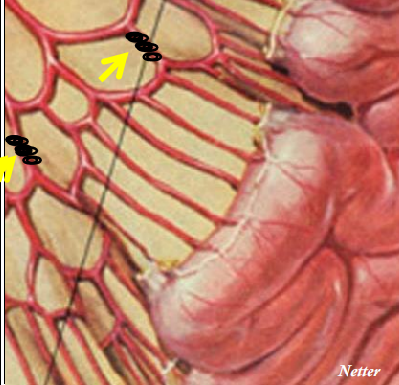
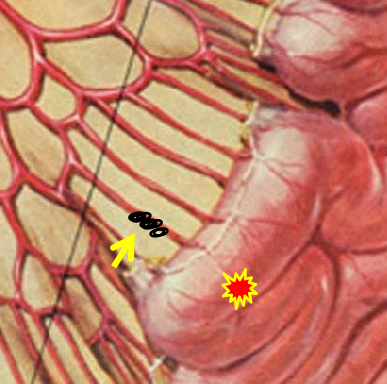
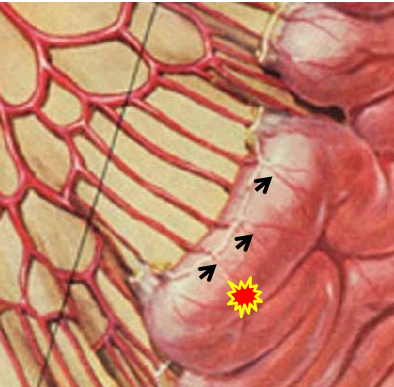
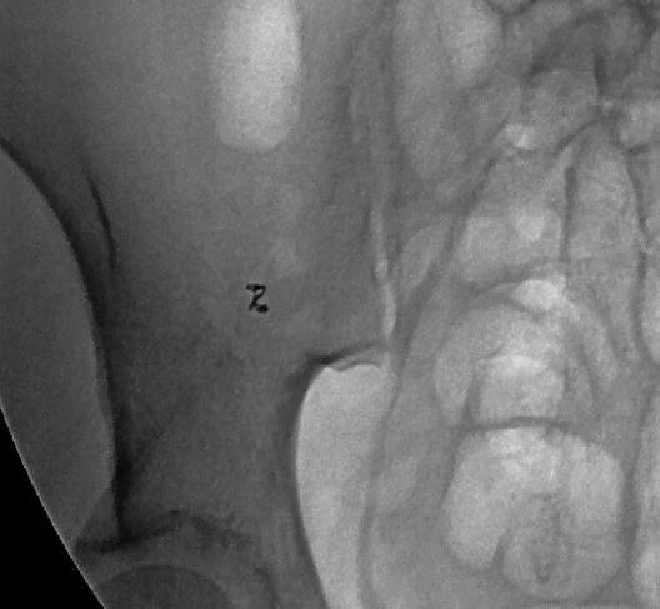
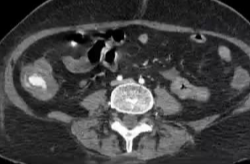
4. 技术要点急性消化道出血,生命体征稳定患者,CTA提示升结肠造影剂外溢
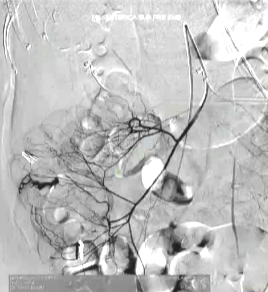
(1)操作流程·诊断性血管造影:用5F导管插管至肠系膜上/下动脉,寻找造影剂外溢(活动性出血)直接或间接征象 · · 超选择插管:通过同轴技术引入3F微导管,尽可能将导管送至直动脉(vasa recta) 或出血点最远端 · · 栓塞:首选微弹簧圈(2-3mm × 20-30mm),放置2-3个即可;也可用聚乙烯醇颗粒(>250μm);禁用液体栓塞剂(如酒精),因其肠坏死率高 · · 终点:造影证实外溢停止,同时保留近端和远端血流(不牺牲侧支循环) · (2)栓塞程度:多少算够?多少算多?理想情况:仅栓塞出血点所在的直动脉 若无法超选至直动脉,可栓塞边缘动脉(marginal artery),但必须确保:
o 近端和远端有足够的侧支血供
o 栓塞长度控制在3-4 cm以内(作者经验),避免过大范围缺血 o 栓塞的目标不是完全阻断血流,而是降低出血点的灌注压,配合局部血管痉挛和患者自身凝血能力形成血栓 5. 微导管远端栓塞临床数据:疗效与安全性一篇发表在2004年的文章汇总了12项研究【Brian Funaki 2004】、超过150例病例,核心数据如下:
结论:微导管栓塞技术安全、有效,已取代血管加压素灌注,成为许多医院处理难治性下消化道出血的首选血管内治疗。 6. 微导管远端栓塞与其他治疗的关系
推荐的分流策略: · 严重活动性出血 → 直接血管造影 + 栓塞 · · 间歇性/慢性出血 → 肠道准备后行内镜 · · 所有血管造影患者均应后续行结肠镜检查(明确病因、排除缺血、发现多发病变) 7. 与其他栏目内容的整合你之前整理的“严重出血稳定→CT;严重出血不稳定→血管造影”是现代更常见的流程。本文发表于2004年,当时CT血管成像尚未普及,因此其流程中“稳定但严重出血”用的是核素显像+靶向血管造影。 若将两者结合,现代流程可整合为:
严重下消化道出血
↓
血流动力学评估
↓
┌───────────────┴────────┐
↓ ↓
不稳定 稳定
↓ ↓
急诊血管造影 CT血管成像(CTA)
(无需核素/CT) (快速定位)
↓ ↓
发现出血点? 阳性(活动性出血)
↓ ↓
微导管栓塞 → 血管造影+栓塞
↓ ↓
成功后 若CTA阴性
↓ ↓
择期结肠镜 考虑核素显像
或择期内镜
8. 微导管远端栓塞临床意义总结这篇文献的价值在于:1. 提供了历史背景:解释了为什么栓塞技术从“弃用”到“复兴”的关键转折点是微导管技术 2. 给出了扎实的数据:多篇研究证实成功率>80%、肠梗死率接近0% 3. 明确了技术细节:栓塞到什么程度、用什么材料、哪些情况要谨慎(如右结肠/盲肠出血) 4. 确立了地位:微导管栓塞是内镜失败或不适用时,处理严重下消化道出血的首选血管内治疗 为什么远端栓塞?下消化道出血栓塞共轴导管选择使导管到达终末支的位置更满意
1. 有效降低出血动脉灌注压
2. 促进出血血管的痉挛和血栓形成
3. 防止侧支循环参与供血的潜在可能
4. 减少出血邻近肠道缺血
用什么栓塞材料做远端栓塞?
1. 微弹簧栓子,更多的人喜欢用,并非因为效果,主要是安全 弹簧栓子/微弹簧栓子消化道出血栓塞应用
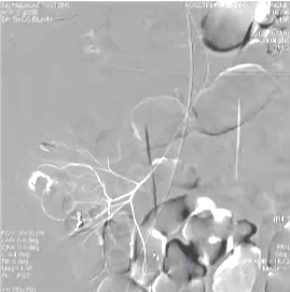
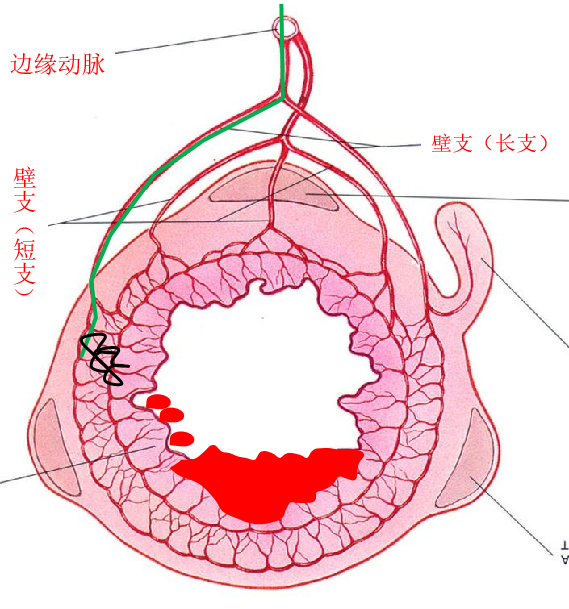
● 弹簧栓子的应用取决于 position of the microcatheter(导管头距出血点距离)
|
 |
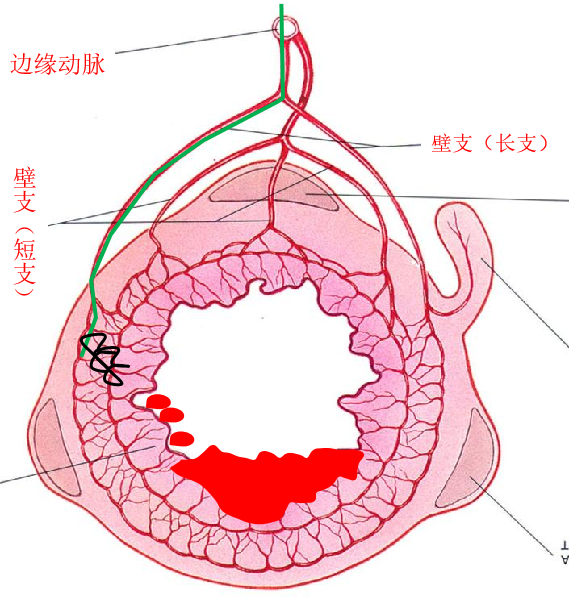 |
| 弹簧栓子位于直小动脉内 |
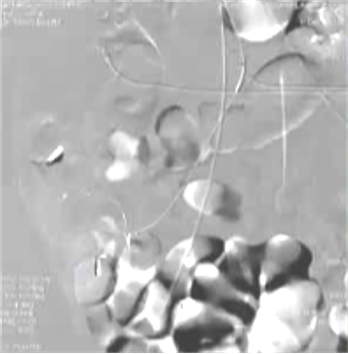
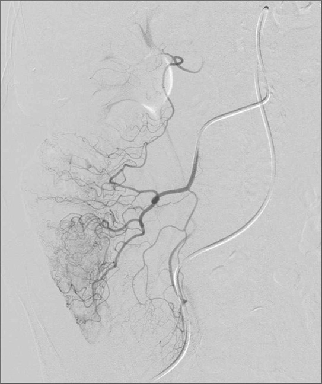
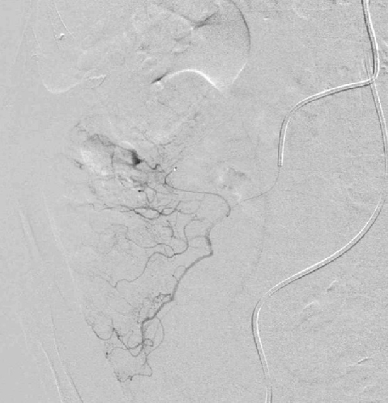
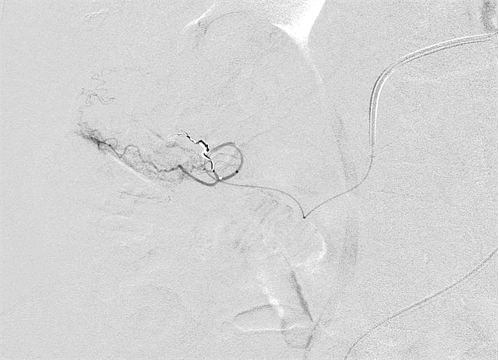
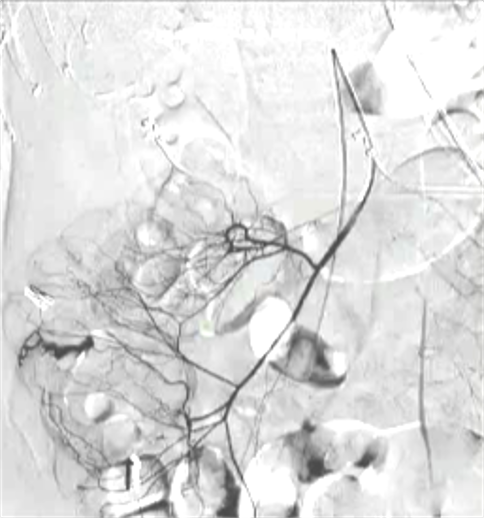
消化道出血弹簧栓子远端栓塞
 |
 |
 |
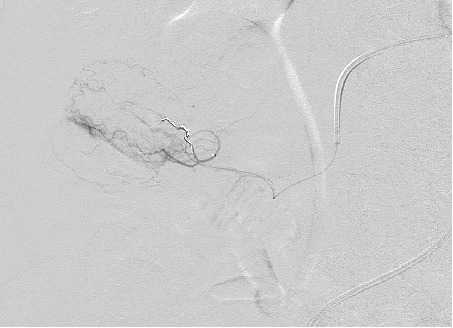 |
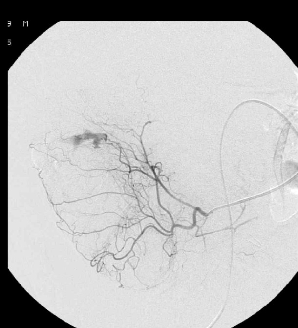
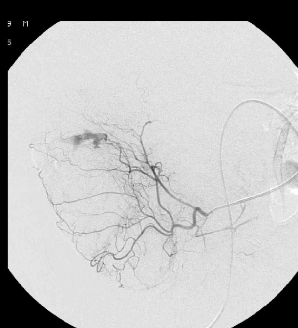
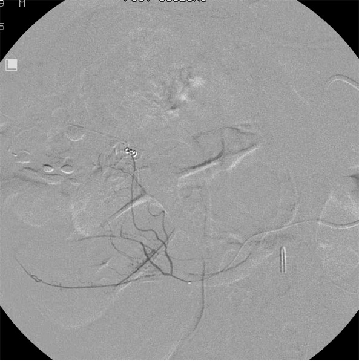
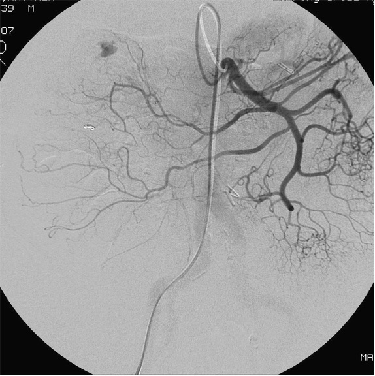
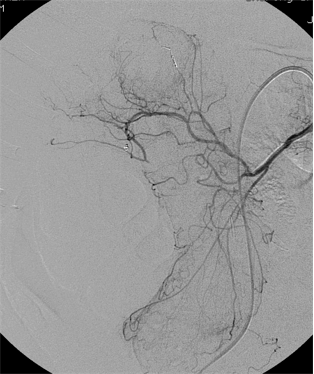
远端栓塞
 |
 |
 |
 |
 |
 |
 |
 |
 |
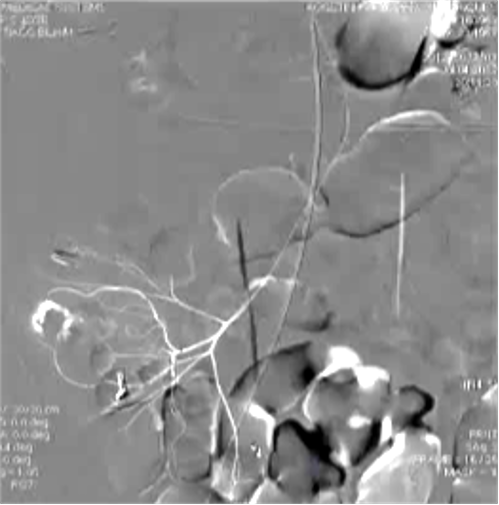
超选择性栓塞术

究竟栓塞几支从边缘动脉发出的直小动脉是可以接受的,但断不能拿人进行实验,所以本文是一篇关于实验研究的论文,旨在评估通过选择性栓塞上腔肠动脉(SMA)分支(在vasa recta水平)使用N-丁基氰丙烯酸酯(NBCA)后,小肠缺血变化的程度。研究对象为六只狗,通过栓塞不同数量的vasa recta分支,并在栓塞后24小时处死动物,以观察和比较不同栓塞程度对小肠组织的影响。
主要观点
研究目的
-
评估小肠缺血变化:研究通过选择性栓塞SMA分支(vasa recta水平)使用NBCA后,小肠缺血变化的程度。
材料与方法
-
实验对象:六只狗。
-
栓塞操作:在五支独立的SMA分支(vasa recta水平)中进行选择性栓塞,使用NBCA。
-
分组标准:
-
组A:栓塞三支或更少的vasa recta。
-
组B:栓塞四支或更多的vasa recta。
-
-
时间点:所有狗在栓塞后24小时被处死。
-
组织学评价:由病理学家对栓塞段的粘膜层、粘膜下层和肌肉层进行组织学评价。
结果
-
组A(n=15):
-
正常发现:7个段(47%)正常。
-
轻度缺血变化:
-
粘膜层:8个段。
-
粘膜下层:4个段。
-
肌肉层:1个段。
-
-
-
组B(n=15):
-
缺血变化:
-
粘膜层:所有15个段。
-
粘膜下层:14个段。
-
肌肉层:10个段。
-
-
-
统计差异:组A和组B之间的缺血损伤差异具有统计学意义。
结论
-
栓塞影响:
-
三支或更少vasa recta:相对可耐受。
-
四支或更多vasa recta:增加显著小肠缺血损伤的风险。
-
-
进一步研究:需要进一步的研究来确定这些发现对人体的临床意义。
总结
本文通过实验研究了选择性栓塞肠系膜上动脉(SMA)分支(vasa recta水平)使用N-丁基氰丙烯酸酯(NBCA)后,小肠缺血变化的程度。研究发现,栓塞三支或更少的vasa recta对小肠的影响较小,而栓塞四支或更多的vasa recta则可能导致显著的小肠缺血损伤。这一发现对于理解该手术技术的安全性和潜在风险具有重要意义,但作者也指出,需要进一步的研究来验证这些发现是否适用于人类患者。核心观点是,选择性栓塞的数量直接影响小肠的缺血损伤程度,临床上应谨慎考虑栓塞的范围。
如果供应肾动脉的三个或更少的肾动脉直小血管未受阻塞,则这种情况相对来说是可以耐受的。
如果血管网数量达到四个或更多,则会增加出现严重缺血性损伤的风险。
这篇《急性消化道出血质量控制》(Quality Improvement Guidelines for Transcatheter Embolization for Acute Gastrointestinal Nonvariceal Hemorrhage)是欧洲心血管与介入放射学会(CIRSE)发布的临床实践指南,旨在规范经导管栓塞治疗在急性非静脉曲张性消化道出血中的应用。
以下是内容概览与核心要点总结:
一、引言
-
急性消化道出血发病率和死亡率高。
-
多数病例可通过内科或内镜治疗控制,但对于大出血或治疗失败者,血管内治疗(栓塞)为首选,因其创伤小、死亡率低。
二、定义
-
技术成功:术中造影剂外渗停止或病变血管完全闭塞。
-
临床成功:术后30天内出血症状缓解。
-
急性大出血:24小时内需输注≥4单位血或出现血流动力学不稳定。
三、影像学评估
-
核素扫描:敏感性高,但定位不准、耗时长。
-
DSA(数字减影血管造影):可检测≥0.5 ml/min的出血,敏感性63–90%。
-
MDCT血管造影:推荐为首选影像方法,敏感性和特异性高(89%/85%),可快速定位并评估血管解剖。
四、适应症与禁忌症
-
适应症:内镜治疗失败或不适用的大出血,尤其是血流动力学不稳定者。
-
禁忌症:相对禁忌包括凝血功能障碍、碘对比剂过敏、肾衰竭、钡剂残留等。
五、操作流程
-
术前准备:纠正凝血、容量复苏、监测生命体征。
-
常用入路:股动脉。
-
栓塞材料:微弹簧圈、PVA颗粒、明胶海绵等,可联合使用。
-
栓塞策略:
-
上消化道:侧支丰富,可采用“三明治法”栓塞。
-
下消化道:终末动脉多,应超选择栓塞,使用较大颗粒(≥700μm)降低缺血风险。
-
六、预后与并发症
-
预后因素:凝血功能障碍是再出血和死亡的主要预测因素。
-
成功率:
-
上消化道:技术成功率93%,临床成功率67%,再出血率33%。
-
下消化道:技术成功率95%,临床成功率76%,再出血率24%。
-
-
并发症:主要为缺血(上消化道<7%,下消化道严重缺血2%),其他包括肝动脉误栓、对比剂反应等。
七、治疗流程算法
-
对急性大出血患者,首选内镜治疗。
-
若失败或无法定位,推荐CT血管造影。
-
CT阳性者行栓塞治疗,阴性者可考虑重复内镜、血管造影或手术。
八、结论
-
经导管栓塞是内镜治疗失败后安全有效的治疗选择,尤其适用于血流动力学不稳定者。
-
应结合多学科团队决策,个体化选择治疗策略。
需要进一步优化或提取为结构化文档(如PPT、流程图、表格)吗?我可以帮你整理。