| 根据最新的国内外权威指南,选择性内放射治疗(SIRT)已成为肝癌介入治疗体系中的核心推荐方式之一,尤其在中期和晚期肝癌的特定患者群体中具有重要的治疗价值。 以下是SIRT在肝癌治疗中的最新指南推荐、适应证与禁忌证、疗效与安全性数据,以及权威机构的推荐意见。 最新指南推荐:SIRT地位的提升· 中国《原发性肝癌诊疗指南(2026年版)》:新版指南首次将SIRT作为独立的治疗方式进行推荐,与经动脉化疗栓塞(TACE)和肝动脉灌注化疗(HAIC)共同构建了更完善的介入治疗体系【卫健委 2026 】。这标志着SIRT在中国肝癌治疗中地位的官方认可和显著提升。 · 2025年EASL指南:欧洲肝脏研究学会(EASL)的2025年指南指出,在符合条件的患者中,SIRT可作为经皮消融的替代方案,用于特定临床情境【EASL 2025】。 · BCLC分期系统:根据巴塞罗那分期(BCLC)的最新更新,SIRT在早期HCC中被定位为一种潜在的根治性治疗选择,尤其适用于不适合消融或手术切除的患者【Paul Vigneron 2024】。 · 2025年FDA批准:2025年7月,美国食品药品监督管理局(FDA)扩大了SIR-Spheres®的适应症,使其成为首个在美国被批准用于原发性HCC一线治疗的SIRT设备,这为SIRT的临床应用提供了强有力的监管支持【Sharon Worcester 2025】。 · NICE指南:英国国家卫生与临床优化研究所(NICE)推荐,对于不适合常规经动脉治疗的Child-Pugh A级肝功能不全的不可切除晚期HCC患者,SIRT可作为一个治疗选择【NICE 2024】。 · 中国专家共识:我国发布了《钇-90微球选择性内放射治疗肝脏恶性肿瘤规范化操作专家共识(2024版)》,这是中国首部针对90Y-SIRT的全面性技术规范文件,为国内该技术的安全、规范开展提供了重要指导【中华消化外科杂志 2024】。 SIRT的主要适应证·不可切除的肝癌:对于因各种原因无法通过手术切除的肝脏肿瘤,SIRT是一个重要的局部治疗选择【NICE 2024 】。 ·肝功能良好(Child-Pugh A级):通常要求患者肝功能储备较好,如Child-Pugh A级,这是保证治疗安全性和有效性的前提【Medscape 2025】。 ·特定分期肝癌:
o 早期(BCLC A期):对于不适合或不愿接受手术/消融的患者,SIRT可作为替代治疗。
o 中期(BCLC B期):对于不符合TACE理想条件的患者,SIRT是一种有效的治疗选择[【Paul Vigneron 2024】。 o 晚期(BCLC C期):特别推荐用于伴有门静脉癌栓(PVT)且无肝外转移的患者,这在TACE等治疗中通常是相对禁忌的。 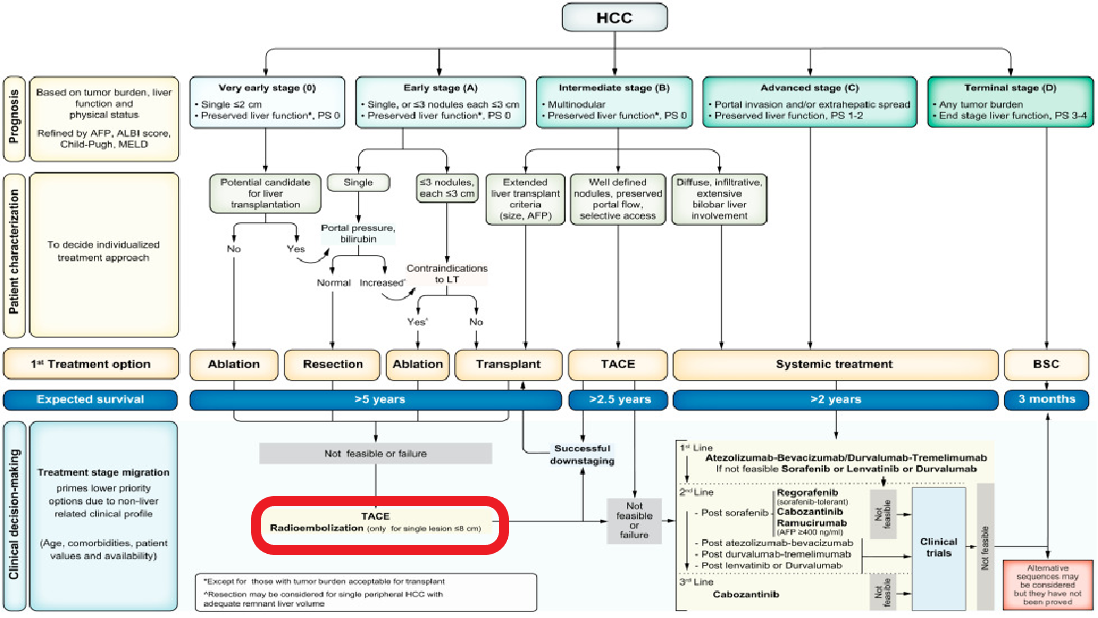 SIRT的主要禁忌证· 肝功能严重失代偿:如存在临床腹水、Child-Pugh评分>B7等。 · 严重肝功能异常:肝功能检查显著异常,例如ALT/AST > 5倍正常值上限、总胆红素 > 2 mg/dL或 > 35 μmol/L。 · 肺分流分数过高:肝肺分流>20%的患者,接受SIRT后发生放射性肺炎的风险显著增加。 · 既往肝外放疗史:曾接受过肝脏外照射放疗的患者(立体定向放疗除外)。 · 肝外显性转移:存在广泛的肝外转移病灶。 SIRT的疗效与安全性数据· 疗效显著:一项2025年的Meta分析显示,与TACE相比,SIRT能显著降低死亡风险(HR 0.68, 95% CI 0.55-0.86)和疾病进展风险(HR 0.54, 95% CI 0.44-0.67)。 · 临床数据:在临床实践中,约75%的患者在接受SIRT后病情稳定;约四分之一的患者肿瘤缩小;成功降期至可手术的比例可达54%;中位总生存期(mOS)达34.8个月。 · 安全性可控:SIRT通常耐受性良好,与TACE相比,其≥3级治疗相关不良事件的发生率呈降低趋势(OR 0.60),但无统计学显著差异。常见不良反应为短暂的发热、乏力、恶心等。 权威机构对SIRT的推荐SIRT(选择性内放射治疗)已进入全球肝癌治疗的主流指南,但其推荐地位会根据患者的肿瘤分期、肝功能及治疗目标有所不同,并非适用于所有人群 · 美国临床肿瘤学会(ASCO):其官方期刊《临床肿瘤学杂志》曾指出,SIRT的独特作用机制使其能为部分患者带来生存获益。 · 美国国家综合癌症网络(NCCN):在HCC指南中,SIRT被列为一种局部治疗选择 。 · 欧洲肿瘤内科学会(ESMO):其指南认为SIRT可用于某些特定的HCC患者群体。 · 欧洲肝脏研究学会(EASL):如前述,2025年指南肯定了SIRT的应用价。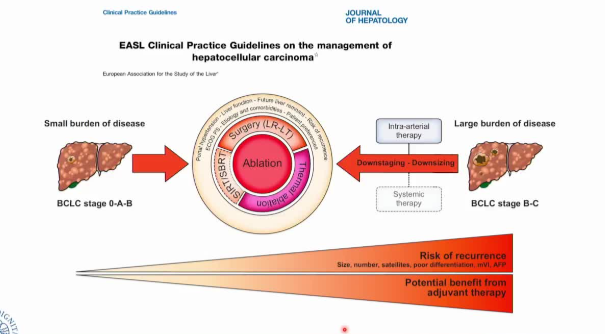 2025年EASL指南治疗策略图详解:,可以清晰地看到,SIRT的定位是“肝内动脉治疗”(Intra-arterial therapy)中的一个选项,用于治疗肿瘤负荷较大(Large burden of disease)的患者,这与我们之前讨论的“放射段切除”用于早期小肿瘤的精准治疗,在理念和应用上是互补的。 这张流程图将肝癌的治疗决策提炼为“小负荷”和“大负荷”两大路径,清晰地勾勒出现阶段的管理框架。 策略图解读:2025年EASL指南的治疗决策路径这张流程图围绕两大核心变量展开决策:肿瘤负荷(Burden of disease) 和肝功能/患者状态。 * 路径一:小负荷肿瘤(Small burden of disease) * 核心目标:根除肿瘤,实现治愈。 * 主流选择:直接导向“手术(肝切除/肝移植,LR-LT)”或“消融(Ablation)”,这是根治性治疗的标准方案。 * 问题聚焦:当肿瘤负荷“小”,但患者因肝功能、位置等原因不适合手术/消融时,路径中提到了“Downstaging -Downsizing”(降期-降负荷)的策略。这正是SIRT中“放射段切除”技术可以大显身手的领域,通过高剂量精准打击,将肿瘤“降期”为可移植或可消融状态。 * 路径二:大负荷肿瘤(Large burden of disease) * 核心目标:控制疾病,延长生存。 * 主流选择:包括“肝内动脉治疗(Intra-arterial therapy)”和“系统治疗(Systemic therapy)”。 * 问题聚焦:SIRT被明确列为“肝内动脉治疗”的一部分。当肿瘤负荷大到不适合手术/消融时,医生需要在TACE(传统动脉化疗栓塞)和SIRT等动脉治疗之间做出选择。 策略背后的考量:指南的决策变量流程图左侧的变量,解释了为何指南会形成上述路径: 1. PS (体能状态) & Elix. & Comorbidities (合并症):这些是评估患者能否耐受侵入性治疗的基础。体力差、合并症多的患者,更倾向于创伤小的治疗。 2. Liver Function (肝功能):这是肝癌治疗的基石,贯穿所有决策。肝功能差的终末期患者(BCLC D期)主要接受支持治疗。 3. Risk of recurrence (复发风险):即使接受根治性治疗,复发风险仍高。流程图底部的提示,点明了影响复发风险的因素,如肿瘤大小、数量、卫星灶、分化差、微血管侵犯和AFP水平,这有助于筛选哪些患者可能从辅助治疗中获益。 总而言之,你提供的这张2025年EASL指南策略图,与我们之前讨论的SIRT发展脉络高度契合:* SIRT并非单一疗法:它既可以作为“肝内动脉治疗”的主力,应对肿瘤负荷大的患者;也可以作为一种“降期/降负荷”的精准武器,处理肿瘤负荷小但不适合标准根治性治疗的患者。 * 决策的核心是“精准”:指南强调的是基于肿瘤负荷、肝功能、患者状态等关键变量进行的个体化决策,这与SIRT技术本身从“泛化”走向“精准”的演变路径完全一致。 上述提及的内容,出自欧洲肝脏研究学会(EASL)于2025年2月发布的《肝细胞癌管理临床实践指南》(*Journal of Hepatology* 2025; 82(2): 315-374)[reference:0][reference:1]。该指南的核心思想是从传统的分期治疗,转向更精细化的基于肿瘤负荷(tumour burden)驱动的个体化决策。 这份指南构建了一个清晰的治疗决策框架,下面对该系统系统继续解读。 基于肿瘤负荷的治疗决策路径指南的治疗决策遵循一个从宏观到微观、从全局到局部的严谨流程【EASL 2025 Mediscape 2025】[reference:4][reference:5]。 第一步:全局评估与精确定位治疗前必须完成以下评估:· 明确肿瘤负荷:通过增强CT/MRI等手段,精确评估肿瘤的大小、数量、位置及有无血管侵犯或肝外转移[reference:6][reference:7]。 · 评估患者全身状况:包括体力状态(ECOG PS)、肝功能(Child-Pugh分级)、病因、合并症等,由多学科团队(MDT)共同讨论决策 第二步:根据肿瘤负荷决定核心治疗路径指南对肿瘤负荷提出了新的二分法,并据此推荐了不同的初始治疗路径:1. 小肿瘤负荷 (Small burden of disease)主要适用于BCLC分期0期、A期和部分B期的患者。此阶段目标为根治性治疗,治疗路径以手术切除、肝移植和消融为核心[reference:11]。具体选择取决于患者是否符合特定条件:· 首选:手术切除:对于无肝硬化的单发肿瘤,或肝功能良好且无临床意义门脉高压(CSPH)的肝硬化患者[reference:12]。微创手术技术是优先选择。 · 可替代:局部消融:对于不适合手术的小肝癌,射频消融(RFA)和微波消融(MWA)是标准治疗。 · 备选方案:肝移植:符合米兰标准等移植标准的患者。降期治疗旨在将超标准的肿瘤通过介入或系统治疗缩小,以符合移植标准 · 探索性治疗:放疗:SIRT和立体定向放疗(SBRT)可作为特定临床情境下的备选方案[reference:15]。 2. 大肿瘤负荷 (Large burden of disease)主要适用于BCLC分期B期和C期。此阶段目标为姑息性治疗,核心是控制肿瘤进展、延长生存并改善生活质量。· 不可切除/多发结节:主要选择动脉内治疗(如TACE)、系统治疗或二者的序贯或联合治疗 。 · 晚期(伴血管侵犯或肝外转移):以系统治疗为核心。所有晚期HCC患者均应接受包含免疫检查点抑制剂(ICI)的联合方案。酪氨酸激酶抑制剂(TKI,如仑伐替尼)可作为一线选择。 第三步:动态调整与辅助治疗决策· 治疗路径转换:指南强调在手术、局部治疗和系统治疗间平稳过渡的策略[reference:20]。· 辅助治疗决策:术后高复发风险因素包括肿瘤大小、数量、卫星灶、低分化、微血管侵犯(mVI)及甲胎蛋白(AFP)水平。目前指南对术后辅助治疗持谨慎态度,虽然不常规推荐,但可考虑用于高风险患者[reference:21]。 EASL 2025版指南构建了一个从全局评估到路径选择、再到动态调整的严密决策体系。其核心思想可概括为:· 小肿瘤负荷→ 追求根治 · 大肿瘤负荷→ 实施控制 · 贯穿全程→多学科协作(MDT)与动态管理 EASL指南中提到的“降期治疗”是实现根治性治疗的重要转化策略。需要我为您展开讲讲降期的具体条件、常用方法和效果评估标准吗? · 英国国家卫生与临床优化研究所(NICE):推荐SIRT用于特定条件的HCC患者。 · 美国食品药品监督管理局(FDA):已批准SIR-Spheres®用于HCC的一线治疗。 SIRT的推荐地位在全球最广泛使用的肝癌分期系统——巴塞罗那分期(BCLC)中有明确界定,并被EASL等权威指南采纳 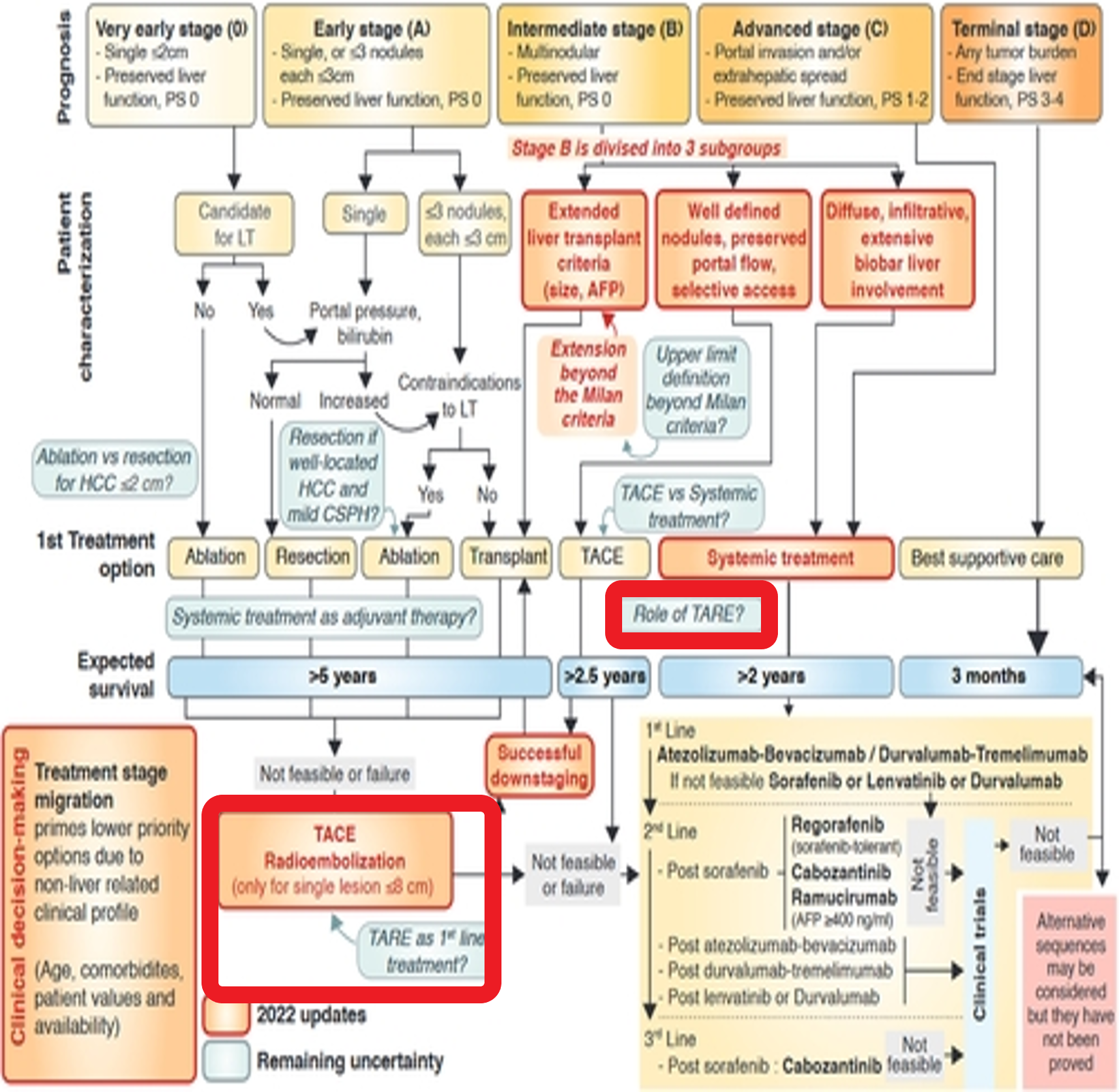 总的来说,SIRT作为一种精准、高效的肝脏局部放射治疗技术,在肝癌的阶梯治疗中占据着关键地位。尤其在2025-2026年间,其获得了中美英及欧洲等多国权威指南与监管机构的高度认可和推荐。鉴于该技术对操作精准性和多学科协作要求极高,建议在有丰富经验的肝癌诊疗中心,由介入科、肝胆外科、核医学科、肿瘤内科等多学科团队共同完成患者筛选、治疗规划与实施。 SIRT的临床应用情况可能因地区医保政策和医疗机构的技术准入而有所不同。如果你想进一步了解SIRT的费用、具体的操作流程,或与其他治疗方式的对比,我可以为你提供更多信息。
最新的临床证据推动了SIRT在指南中地位的演变,主要体现在以下方面:
走向精准根治(“放射段切除”):对于早期、单发的肝癌(如LEGACY研究中肿瘤<8cm的患者),采用高剂量“放射段切除”技术,其3年总生存率可达86.6%。这使SIRT成为不适合手术患者的一种根治性替代方案。
探索联合治疗(“SIRT+”时代):对于晚期肝癌,研究正探索SIRT联合免疫治疗,以期达到“1+1>2”的效果。已有研究证实,SIRT后启动免疫治疗,可能最大化CD8+ T细胞的浸润
|

