中期肝癌(B期)肝移植米兰标准或扩大米兰标准→ 肝移植 → 不可行或失败 → TACE或TARE → 不可行或失败 → 全是一线治疗→ 全身二线治疗 →全身后线临床试验。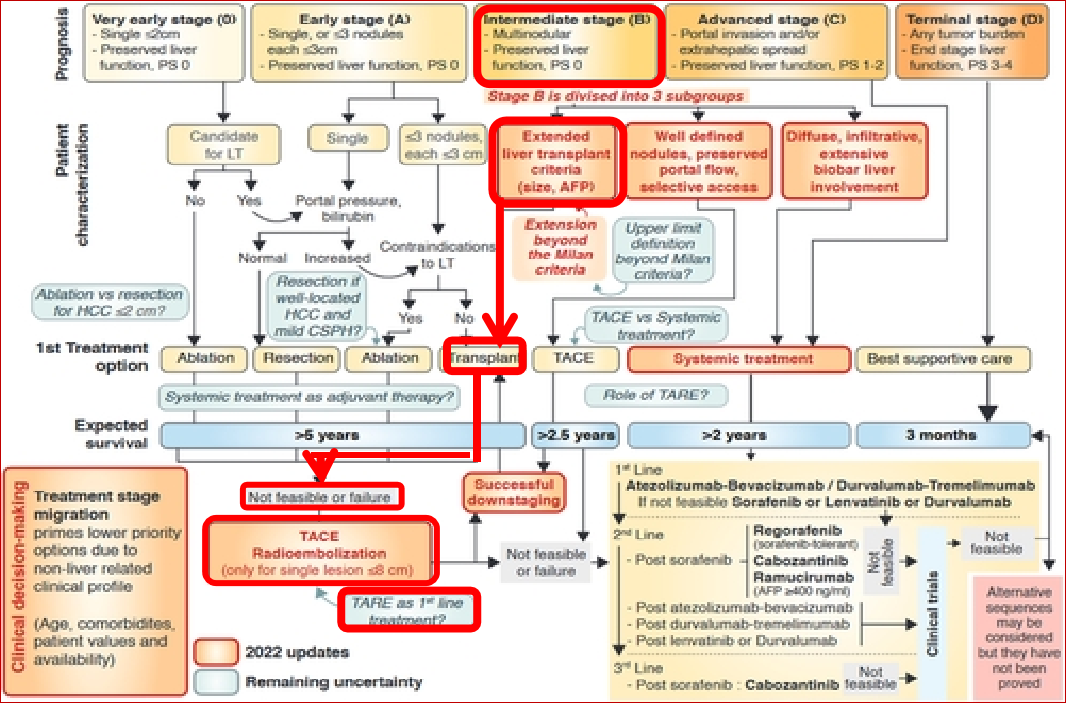 中期肝癌 (B期)边界清楚的结节,门脉血流好,选择性进入路径1:→ TACE>2.5年 → 成功降期治疗 → 肝移植 →如果不行或失败→ TACE 或TARE → 路径2:→ 全身治疗 → >2年 → 全身一线治疗→ 全身二线治疗 → 后线临床试验 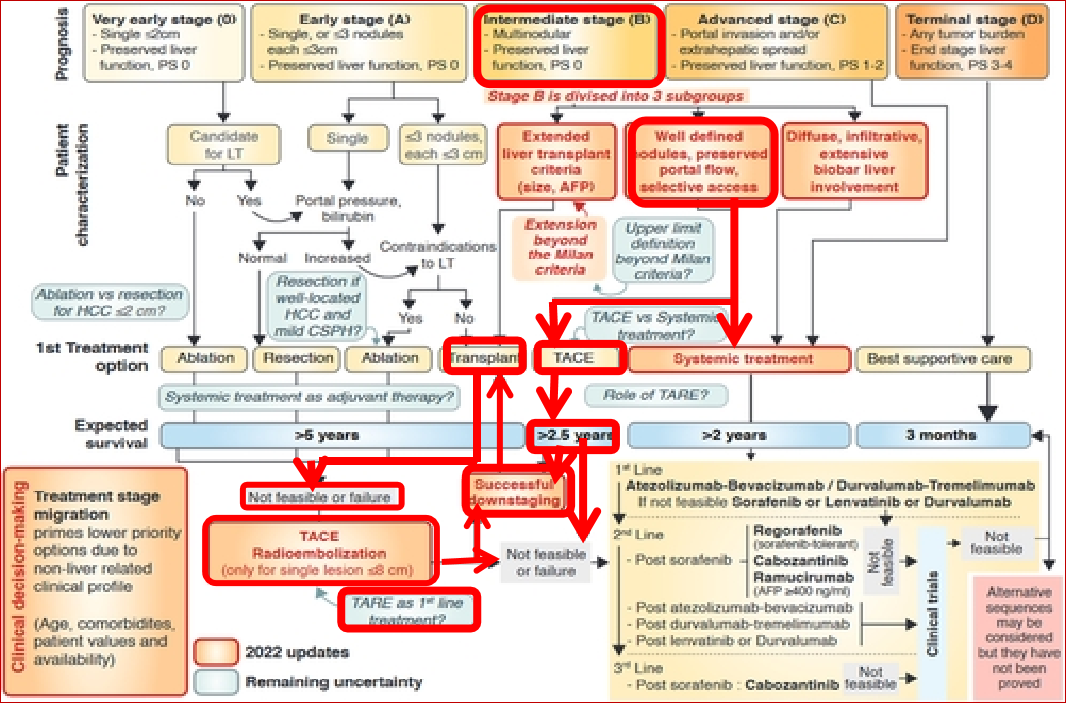 肝癌中期(B期)弥漫性,侵润性,广泛性双叶受累→ 全身治疗 → 一线治疗→ 二线治疗>2年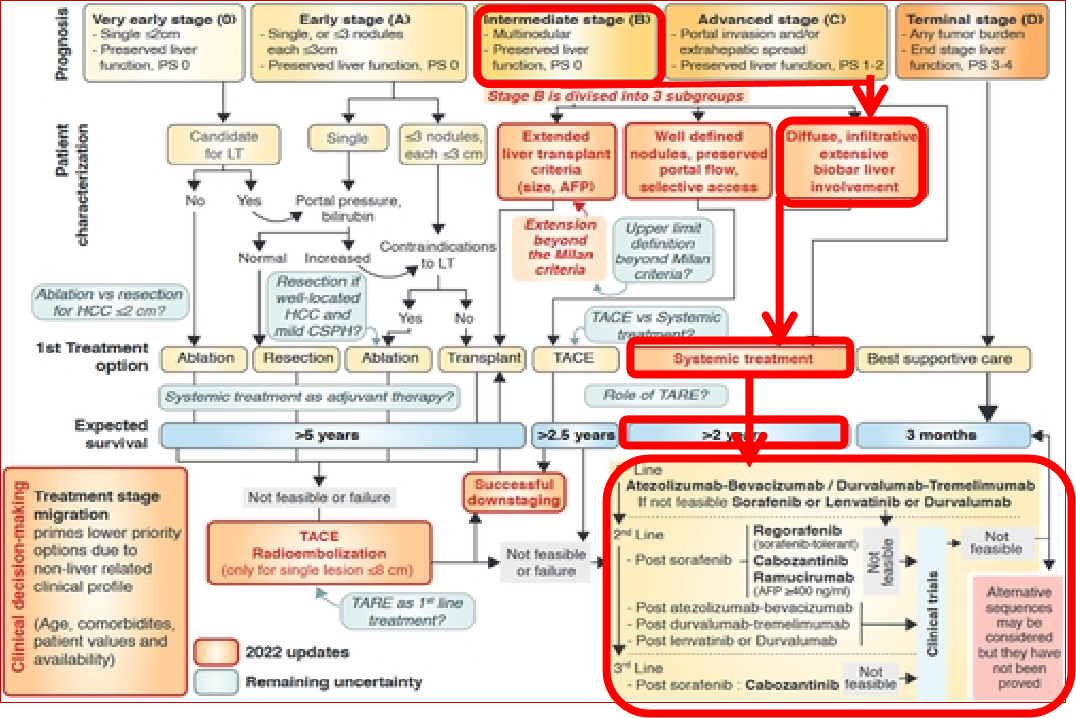 EASL 2024说: In patients with multiple tumours in the intermediate stage who are not fit for TACE/TAE or surgery, TARE cannot currently be recommended as an alternative to systemic therapy, although it is an acceptable option if systemic therapy is contraindicated, provided a lobar approach is possible (LoE 4, weak recommendation) 这句话,正是2024年EASL指南中对TARE/SIRT在中期肝癌(BCLC B)中定位的最核心、最精准的表述。它完美地总结了TARE在这一患者群体中的有限但明确的角色。 下面我将这句话拆解为三个层次,结合我们之前的讨论,为你深度解读。 指南原文拆解“In patients with multiple tumours in the intermediate stage who are not fit for TACE/TAE or surgery, TARE cannot currently be recommended as an alternative to systemic therapy, although it is an acceptable option if systemic therapy is contraindicated, provided a lobar approach is possible (LoE 4, weak recommendation).” 第一层:核心结论——不替代系统治疗“TARE cannot currently be recommended as an alternative to systemic therapy”(目前不推荐TARE作为系统治疗的替代方案) · 原因:对于BCLC B期、多发肿瘤、不适合TACE/手术的患者,当前的标准治疗是系统治疗(如免疫联合抗血管生成药物,例如阿替利珠单抗+贝伐珠单抗、信迪利单抗+贝伐珠单抗类似物等)。这些方案已有大型III期试验证实能显著延长总生存期(OS),证据等级为1。而TARE与这些新型系统治疗从未进行过头对头的随机对照试验。仅有的TARE vs. 索拉非尼的III期试验(SARAH、SIRveNIB)结果为阴性,且索拉非尼已不再是首选。因此,指南无法推荐TARE作为替代。 · 与我们之前讨论的TRACE试验的关系:TRACE试验证明TARE优于DEB-TACE,但那是局部治疗之间的比较,而非与系统治疗比较。对于“不适合TACE”的患者,指南并未直接推荐TARE,而是建议转向系统治疗。 第二层:例外情况——系统治疗禁忌时的备选“although it is an acceptable option if systemic therapy is contraindicated”(但如果系统治疗有禁忌,TARE是可接受的选择) ·何为“系统治疗禁忌”?常见情况包括: o患者有未控制的严重高血压、出血风险高(如食管胃底静脉曲张未处理)、蛋白尿等抗血管生成药物的禁忌。 o患者有活动性自身免疫病、长期使用大剂量激素等免疫检查点抑制剂的禁忌。 o患者拒绝或无法耐受系统治疗的毒性(如手足综合征、腹泻、乏力等)。 o患者肝功能处于临界状态(如Child-Pugh B7),系统治疗风险较高(尽管部分ICI在Child-Pugh B中也有数据,但非标准适应症)。 · 为什么此时TARE可接受?因为对于肝内负荷重、但肝功能尚可(指南虽未明说,但实践中需Child-Pugh A或B7)、且无肝外转移的患者,TARE仍能提供有效的局部控制,延缓肝内进展,可能延长生存。同时,多项真实世界研究和TRACE试验已证明其安全性可控。 第三层:技术前提——必须是叶段(lobar)治疗“provided a lobar approach is possible”(前提是能够进行叶段治疗) · 为什么特别强调“lobar approach”?对于多发肿瘤(multiple tumours),超选择性的“放射段切除”无法覆盖所有病灶。必须采用叶段性治疗(即整叶肝灌注),才能有效控制整个肝叶内的多发病灶。这通常意味着治疗范围至少涉及一个肝叶(左或右),甚至全肝(分次进行)。 · 临床意义:这条技术前提强调了TARE在中期多发肿瘤中的应用方式——它不追求像早期肝癌那样“精准爆破”单个病灶,而是通过大范围的放射性“内照射”来“清扫”整个叶段的微小病灶和卫星灶。这恰恰是TARE相比TACE的一个潜在优势(TACE超选择性插管可能遗漏周边病灶)。 证据等级与推荐强度解读· 证据等级 4 (LoE 4):该推荐基于病例系列、病例对照或历史对照研究,而非随机对照试验。这意味着没有高质量的直接证据(如TARE vs. 系统治疗的RCT),推荐主要来自间接证据、专家经验和共识。 · 弱推荐 (weak recommendation):意味着并非所有患者都应接受TARE,临床决策需高度个体化,充分权衡利弊、患者意愿和中心经验。它不是一个“标准方案”,而是一个“在特定情况下可以考虑的选项”。 临床应用要点总结
与既往讨论的呼应· 这条推荐与我们之前分析的TRACE试验并不矛盾。TRACE试验入组的患者是适合TACE的(多数为BCLC A/B),而本条推荐针对的是不适合TACE的患者。两者处于不同的人群“赛道”。 · 它也与SARAH/SIRveNIB的阴性结果逻辑一致:在晚期(BCLC C)或不宜TACE的中期患者中,TARE不优于旧系统治疗(索拉非尼);而对于新一代更强的系统治疗,指南更不推荐TARE去替代。 · 它反映了指南在缺乏TARE vs. 新型系统治疗RCT情况下的保守立场,同时为临床实践留出了空间——当系统治疗“此路不通”时,TARE仍是一扇“备用之门”。 2025年EASL指南对TARE在中期多发肝癌(不适合TACE)中的定位非常明确:它不能与系统治疗平起平坐,但也不是被完全抛弃。它像一个“替补队员”,只有在系统治疗无法上场(禁忌)时,才会被考虑派上阵,而且必须用“叶段治疗”这种打法才能发挥最大作用。这条推荐既体现了循证医学的严谨(没有证据就不推荐),也体现了临床实践的灵活性(为个体化治疗留出空间),是我们在制定治疗策略时需要深刻理解并遵循的。 |

