SIRT 的放射剂量估算,可以理解为一个从粗略评估到精准计算,并最终导向个性化治疗策略的完整流程。它主要依赖于特定的计算模型和专用软件来精确计算所需的放射性活度。 模型基石:从经验到精准的剂量计算目前临床主要应用三种剂量计算模型,它们构成了剂量估算的基础。
计算流程:从影像到活度的三步递进剂量估算是一个多步骤递进的过程,从影像采集开始,到最终确定处方活度结束。 1. 术前模拟:图像采集与参数计算灌注扫描:术前,医生会通过微导管向肝脏注入锝-99m标记的大颗粒聚合白蛋白(99mTc-MAA),其分布可高度模拟后续钇-90(90Y)微球的沉积位置。参数获取:随后进行SPECT/CT扫描,获得以下关键参数: 肺分流率(Lung Shunt Fraction, LSF):评估有多少放射性微球会“分流”到肺部,这对保障治疗安全至关重要。 肿瘤/正常组织比(Tumor-to-Normal Ratio, T/N):衡量肿瘤组织吸收放射性物质的能力相对于正常肝组织的比值,是剂量计算的核心参数。 肝脏及肿瘤体积:精确勾画肿瘤和肝脏的轮廓,计算出其体积。 2. 核心计算:确定处方活度o 基于上述参数,医生会使用特定模型计算出“处方活度”(即注入患者体内的90Y总放射性量,单位:GBq)。3. 术后验证:确认实际剂量o治疗完成后,会通过PET/CT或SPECT/CT进行成像。利用获得的图像,医生可以反推计算实际输送到肿瘤和正常肝脏的辐射吸收剂量(单位:Gy),从而验证治疗是否达到预期,并用于指导后续治疗。辅助工具:专用软件与AI的应用当前临床实践中,已有多种专用软件可辅助完成上述复杂的计算。
实战应用:SIRT剂量估算的临床路径以临床最常用的分区模型为例,剂量估算的完整流程如下: 1. 参数测量:通过术前99mTc-MAA的SPECT/CT扫描,精确测量:肺分流率 (LSF)、肿瘤/正常组织比 (T/N)、肝脏总体积、肿瘤体积。 2. 活度计算:将上述参数代入分区模型的特定公式,计算处方活度。 3. 剂量分析:利用软件生成剂量-体积直方图(DVH),直观展示肿瘤和正常肝组织分别接收的辐射剂量。 4. 临床决策: o若肿瘤剂量远低于目标值(如<100 Gy):治疗很可能效果不佳,应考虑更换治疗方案。 o若肿瘤剂量达标而正常肝脏剂量过高:肝损伤风险增加,需考虑调整治疗策略,如采用更超选择的靶区。 o若肿瘤剂量理想且正常肝脏剂量安全:可按计划执行SIRT,并预期获得良好的治疗反应。 o若为再次治疗:需基于累积剂量评估风险,因为肝脏对辐射的损伤是不可逆的。 核心目标:迈向个性化SIRT治疗SIRT剂量估算的最终目标,是实现“量体裁衣”式的个性化精准治疗。 · 精准化是趋势:当前共识和指南均强烈推荐采用更精准的个性化剂量计算方法,以提高疗效并降低并发症风险。 · 确定性与策略:目前研究数据已能为临床决策提供量化参考。当肿瘤吸收剂量达到100-120 Gy时,可获得较佳的肿瘤控制率,这与SARAH研究的发现(肿瘤吸收剂量≥100 Gy的患者中位总生存期更长)一致。同时,国际共识建议将正常肝脏的平均吸收剂量控制在50 Gy以下,以确保治疗的安全性。 总而言之,SIRT剂量估算是一个由**模型驱动、流程规范、工具辅助**的精准医疗实践。其核心价值在于,通过精确的术前规划与术后验证,为患者制定出个体化的治疗策略,确保在安全的前提下最大化治疗效果。 

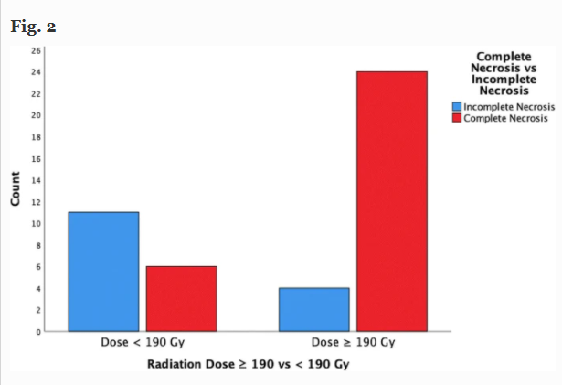
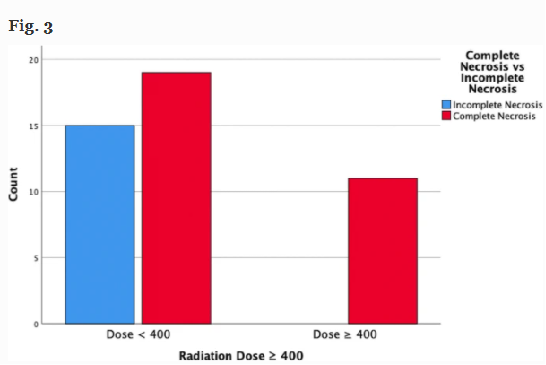
采用消融剂量Y90治疗早期HCC的放射肝段切除术与完全病理坏死(CPN)有关。新的阈值剂量建议>400Gy 以最大限度地提高获得CPN的患者百分比
|