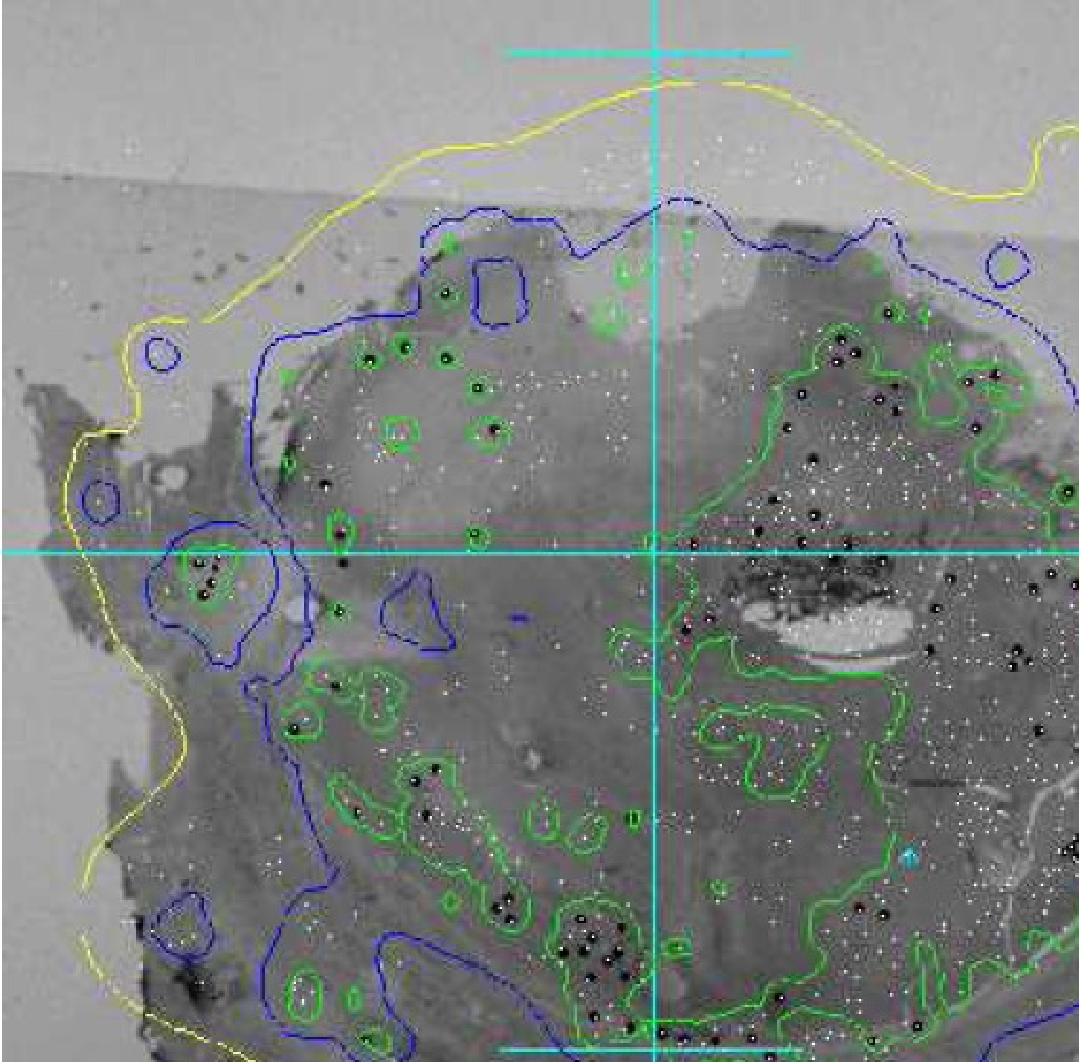
**SIRT 等剂量曲线**,在临床和物理层面可以理解为两把“标尺”,一把衡量疗效,一把衡量风险。 简单来说,给肿瘤的辐射剂量越高,杀死癌细胞的可能性(即“肿瘤控制概率”,TCP)就越大;但与此同时,给正常肝脏的剂量越高,发生放射性肝损伤的风险(即“正常组织并发症概率”,NTCP)也越高[reference:0]。SIRT治疗的理想目标,就是在两者之间找到那个最佳的“治疗窗”。 一把衡量“疗效”的标尺:肿瘤控制概率 (TCP) 剂量曲线这条曲线描述的是肿瘤吸收剂量与肿瘤被杀灭概率之间的关系。许多研究都试图找到那个能最大可能杀死肿瘤的“最佳剂量点”,但由于肿瘤的异质性和研究方法的差异,目前对最佳剂量尚无统一标准[r【Bastiaannet R 2018】。 ·普遍认可的剂量阈值:
多项研究表明,当肿瘤吸收剂量达到约100-120 Gy时,是一个有效提升肿瘤控制率的关键节点。
o SARAH 试验:SARAH 试验的剂量分析发现,当肿瘤吸收剂量达到或超过100 Gy时,患者的中位总生存期显著延长(14.1 个月 vs 6.1 个月)。
o 其他研究:一些研究也给出了更精确的数值,例如 50% 肿瘤控制概率 (TCP50) 所需剂量为110–120 Gy 【Bastiaannet R 2018】,或平均吸收剂量为160 Gy 【Bastiaannet R 2018】。
o 玻璃微球:有研究显示,为了达到理想的肿瘤反应,所需的剂量可能更高,例如205 Gy[reference:4]或215 Gy[reference:5]。
o 个性化预测:最新的研究正在尝试利用更复杂的模型和人工智能,预测患者的个体化剂量-反应关系,以实现真正的“量体裁衣”式治疗【Zahra Mansouri 2025】。 另一把衡量“风险”的标尺:正常组织并发症概率 (NTCP) 剂量曲线这条曲线描述的是正常肝组织吸收剂量与发生放射性肝损伤概率之间的关系。保护正常肝脏是SIRT治疗成功的关键。 ·核心原则:正常肝脏的平均剂量需严格限制。
o 放射性肝损伤(RILD)的风险随正常肝脏吸收剂量的增加而急剧升高。多项研究通过NTCP模型计算,认为将正常肝脏的平均剂量控制在50 Gy以下是相对安全的选择 【Stefan Müller 2010】。
o 临床上,医生会基于患者的具体情况(如肝功能、肝硬化程度等)设定一个可接受的NTCP阈值(如15%),并据此来规划和调整处方剂量[reference:8]。 剂量曲线的临床应用:治疗计划制定在实际临床操作中,医生会综合运用这两条曲线,为患者制定个体化的治疗方案。这通常分三步走: 1. 目标设定:首先设定一个治疗目标,例如“力求肿瘤控制概率达到90%”或“确保正常肝脏并发症概率低于5%”。 2. 个体化计算:通过术前99mTc-MAA SPECT/CT影像,模拟放射性微球在患者体内的分布,并计算达到目标所需的剂量[reference:9]。值得注意的是,即使是相同的处方剂量,使用不同的计算模型(如标准模型与分区模型)所预测的肿瘤控制效果也 可能存在显著差异(例如,肿瘤控制概率预测值可能从降低26%到增加81%不等),这更凸显了个体化评估的重要性【Benjamin J. Van 2021】 3. 精准投送:根据计算结果,计算出需要注射的放射性总活度,并通过微导管将SIRT微球精准注入肿瘤供血动脉。 当前挑战与未来方向:从“经验”到“精准”尽管剂量曲线的概念清晰,但其临床应用仍面临挑战。不同研究报道的“最佳剂量”差异较大,反映了SIRT剂量学的复杂性【 Benjamin J. Van 2021】 未来的发展方向,是通过以下手段,实现更精准的个性化治疗: · 更精准的预测模型:利用放射组学和剂量组学等新技术,从影像中挖掘更多信息,预测患者的个体化剂量反应【Benjamin J. Van 2021】。 · 新型放射性核素:如钬-166 (¹⁶⁶Ho),它兼具治疗和显像功能,可实现真正的治疗剂量验证,从而进行更精确的剂量调整[【】reference:13]。 等剂量曲线
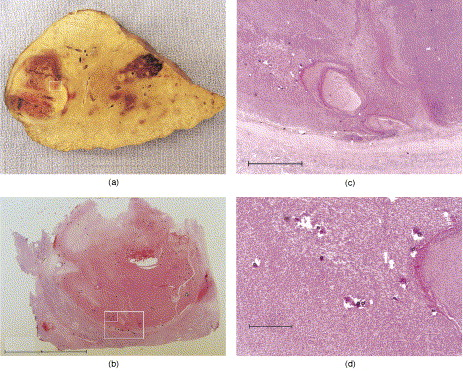
移植肝微剂量测定(Micro-Dosimetry in Explanted Livers)
| ||||||||||