|
| 特征维度 | 之前讨论的III期试验 (SARAH/SIRveNIB等) | LEGACY研究 (2021) |
| 患者人群 | 晚期肝癌(BCLC C期为主,或B期不适合TACE) | 早期肝癌(BCLC A期为主,占60.5%) |
| 肿瘤特征 | 多结节、大肿瘤、常伴血管侵犯 | 孤立性、小肿瘤(中位2.7cm, ≤ 8cm) |
| 肝脏功能 | Child-Pugh A或B7 | Child-Pugh A级(肝功能储备好) |
| 治疗策略 | 非选择性/ lobar灌注(大范围) | 超选择性/ “放射段切除”(精准打击) |
| 剂量目标 | 经验性、基于体表面积 | 高剂量、消融级别(中位410 Gy) |
| 主要终点 | 总生存期 (OS) | 客观缓解率 (ORR) 和缓解持续时间 (DoR) |
核心发现:惊艳的疗效与持久的控制
LEGACY研究的结果,用“惊艳”来形容并不为过。它清晰地展示了在“对的人群”中用“对的技术”能达到的效果。
1. 极高的肿瘤控制率:
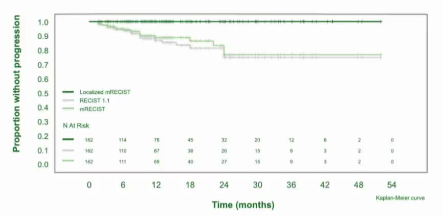
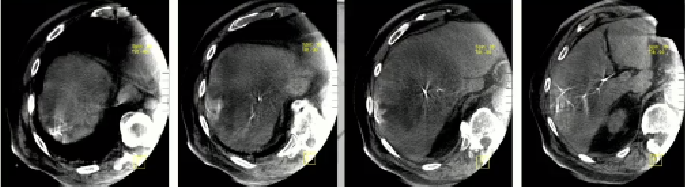
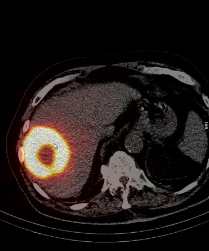
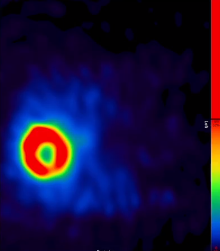
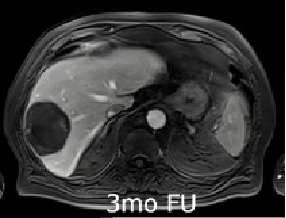
主要终点达成:客观缓解率(ORR)高达88.3%,远高于预设的40%阈值。其中84%的患者达到了完全缓解(CR),意味着影像学上肿瘤完全消失。持久的反应:62.2%的患者的缓解持续时间(DoR)超过了6个月,中位DoR为11.8个月。这表明TARE带来的肿瘤缩小不是短暂的,而是持久的。
2. 优异的长期生存:
o3年总生存率(OS)高达86.6%。对于不可手术的单发小肝癌,这个生存数据极具竞争力,可与手术切除或消融治疗相媲美。o作为桥接治疗:在研究中有45名患者通过TARE成功桥接到肝移植或手术切除,这部分患者的3年生存率更是高达92.8%。
3. 完美的局部控制:
o在接受治疗的肿瘤区域内,2年局部进展率为0%。这意味着,只要被TARE精准覆盖的肿瘤,几乎没有原位复发的可能。所有“进展”都表现为肝内新发灶或肝外转移。与剂量学的关联:高剂量是“消融”的关键
LEGACY研究的结果,与我们之前深入讨论的 **“剂量决定疗效”** 原则完美契合,并为其提供了最高级别的临床证据。
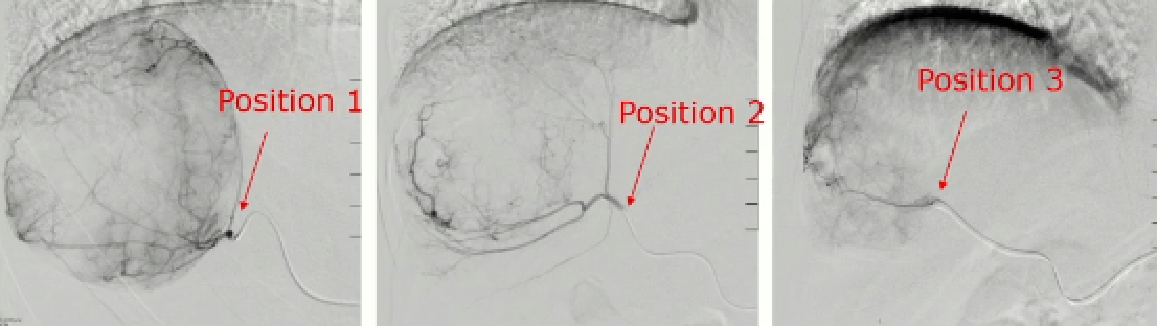
· “放射段切除” (Radiation Segmentectomy):这是LEGACY研究采用的核心技术。它不是对半个肝脏进行大范围照射,而是通过超选择性插管,将微导管精准插入肿瘤的供血动脉分支,只对肿瘤及其周边极窄的边缘(一个肝段)进行超高剂量的放射。
· 消融级别剂量:研究中,肿瘤所接收的中位吸收剂量高达410 Gy。这远超我们之前讨论的100-120 Gy的“有效阈值”,进入了“消融剂量”的范围。这种剂量足以彻底摧毁目标区域内的所有细胞,达到与物理消融(射频、微波)或手术切除相似的效果。
· 病理证实:研究引用了一项子分析,发现在接受手术/移植的LEGACY患者中,当肿瘤吸收剂量超过400 Gy时,手术切除的病理标本显示100% 的完全坏死率。这从病理层面证实了“高剂量”与“根治”的直接关系。
LEGACY的历史意义:TARE/SIRT的最终精准定位
综合我们讨论的所有文献,可以清晰地看到TARE/SIRT的历史地位演变,而LEGACY研究为这条演变之路画上了一个阶段性的、积极的句号。
1. 2012年指南时代:“有潜力,但证据不足,非标准治疗。”(一个探索性的技术)
2. 2015-2018年III期试验时代:“在晚期肝癌中,不优于标准治疗索拉非尼。”(一个被证伪的“银弹”)
3. 2020-2021年剂量学分析时代:“疗效高度依赖于剂量,毒性可能抵消获益。”(一把需要精准使用的“双刃剑”)
4. LEGACY研究时代 (2021):“在精选的早期、单发、小肝癌中,通过高剂量精准打击,可以实现媲美根治性治疗的效果。”(一个被正名的“精锐武器”)
**总结来说,LEGACY研究的核心贡献在于:它将TARE/SIRT从一个主要用于中晚期肝癌的“姑息或备选方案”,提升为早期、不可手术或不愿手术的孤立性小肝癌的一个**强效的、独立的、具有根治潜力的治疗选项 **。它标志着TARE/SIRT技术已经发展成熟,能够在经验丰富的中心,通过精准的患者筛选和精湛的介入技术,实现从“控制”到“治愈”的飞跃。**
 |
 |
 |
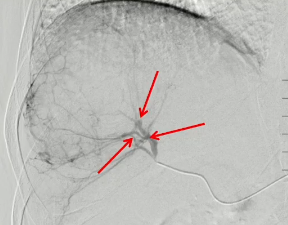 |
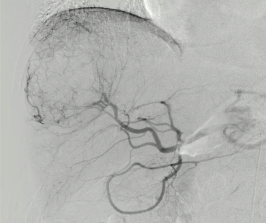
超选择插管
 |
 |
 |
 |
 |
 |
 |
精准地提炼出 **LEGACY 研究**的核心数据。这些数据正是证明 TARE/SIRT 在特定早期肝癌患者中价值的“压舱石”。
为了让你更清晰地看到这些数据的里程碑意义,我将它们与之前讨论的、代表 TARE/SIRT 用于晚期肝癌的“阴性”III 期试验(如 SARAH)进行一个直观对比:
| 核心维度 | LEGACY 研究 (2021) | SARAH 试验 (2017) |
| 研究性质 | 单臂、回顾性、多中心 | 随机、开放、III 期、多中心 |
| 患者人群 | 孤立性、不可切除 HCC | 局部晚期或不可切除 HCC (BCLC B/C) |
| 肿瘤特征 | ≤ 8 cm (中位 2.7 cm) | 中位肿瘤直径更大,常伴多结节或血管侵犯 |
| 肝功能 | Child-Pugh A 级 | Child-Pugh A 或 B7 |
| 治疗技术 | 超选择性“放射段切除” | 主要为非选择性/叶段灌注 |
| 中位剂量 | 410 Gy (消融级别) | 未明确,但远低于此 (通常 < 150 Gy) |
| 最佳客观缓解率 (ORR) | 88.3%(其中 84% 完全缓解) | 19%(TARE 组) |
| 中位缓解持续时间 (DoR) | 11.8 个月(确认缓解者) | 未报告或更短 |
| 3 年总生存率 (OS) | 86.6%(全人群) | 未直接报告,但中位 OS 约 11-14 个月 |
这些数据如何改变 TARE 的历史地位?
你总结的这组数据,清晰地回答了之前所有争议,并最终确立了 TARE 的精准角色:
1. 从“阴性”到“阳性”的赛道转换:
oSARAH 等研究证明 TARE不是晚期肝癌的“通用型”标准治疗。oLEGACY 则证明 TARE可以成为早期、单发、小肝癌的“精锐型”根治手段。
2. 从“姑息剂量”到“消融剂量”的跨越:
o过去 TARE 疗效不佳,核心原因之一是剂量不足(< 150 Gy)。oLEGACY 中410 Gy的中位剂量,实现了病理上的100% 完全坏死。这证实了“高剂量”是走向“根治”的关键。
3. 从“肿瘤控制”到“持久缓解”的升级:
o88.3% 的 ORR和11.8 个月的中位 DoR表明,TARE 带来的不是昙花一现的肿瘤缩小,而是高比例、持久的影像学消失。这为患者提供了宝贵的“无瘤”或“带瘤长期稳定”状态。之前关注问题的直接回答
·TARE 是“银弹”吗?
o 对 LEGACY 中的这类患者(孤立、小、肝功能好)来说,它非常接近“银弹”—— 一次治疗,极高概率让肿瘤完全坏死并长期不复发。
o 对晚期、多发、肝功能差的患者,它不是“银弹”,甚至可能有害。
·剂量学计算重要吗?
o 至关重要。LEGACY 的成功直接验证了“高剂量、精准投送”的剂量学原则。如果没有410 Gy的剂量目标,就不可能实现84% 的完全缓解率。
这组数据,是 TARE 发展史上最有力的“正名”证据。它标志着 TARE 已经从一个主要用于中晚期肝癌的“姑息或备选方案”,正式演变为一种在**高度精选的早期肝癌患者**中,能够实现**高概率、高持久性、近似根治效果**的成熟技术。
从此,TARE 的临床决策不再是“能不能用”,而是“**对谁用、怎么用才能达到 LEGACY 这样的效果**”。