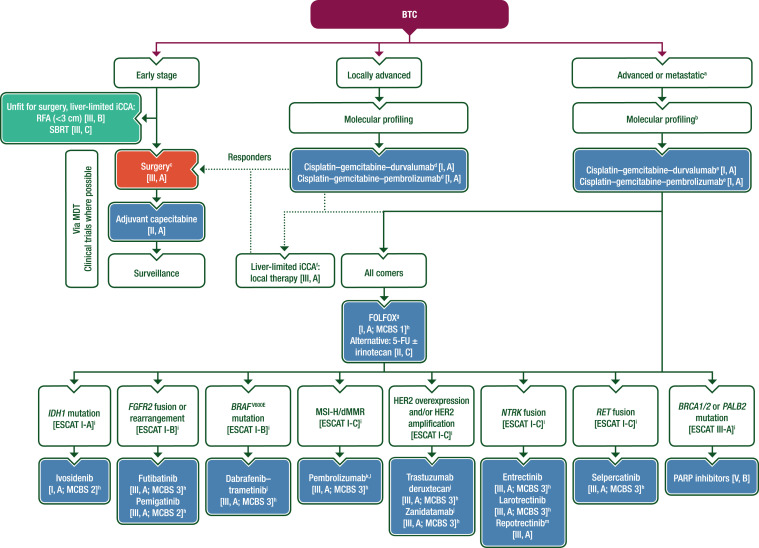
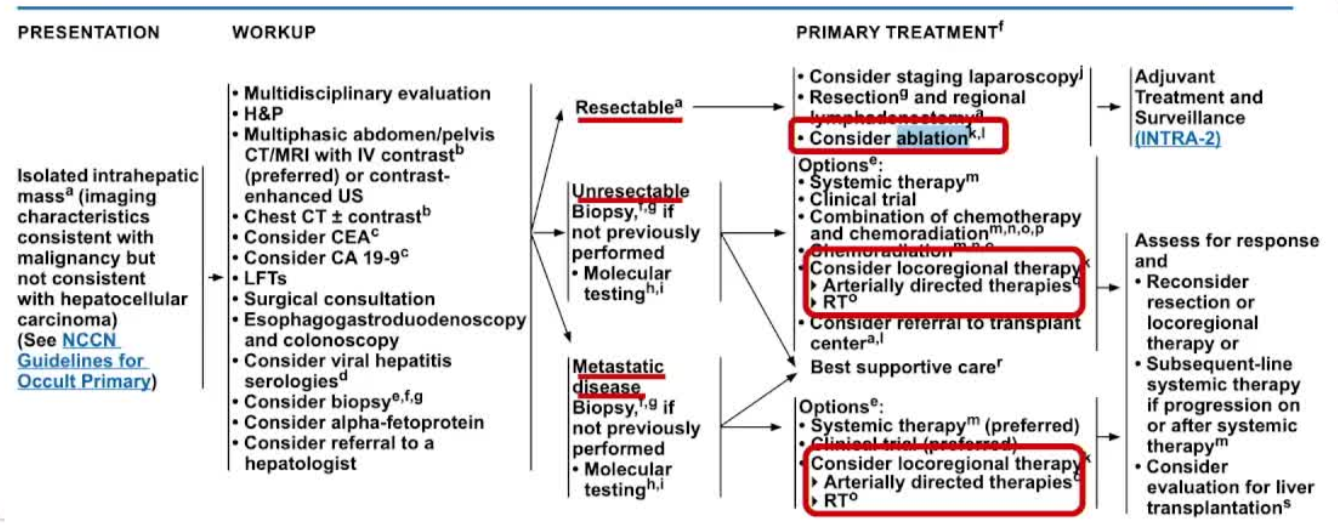
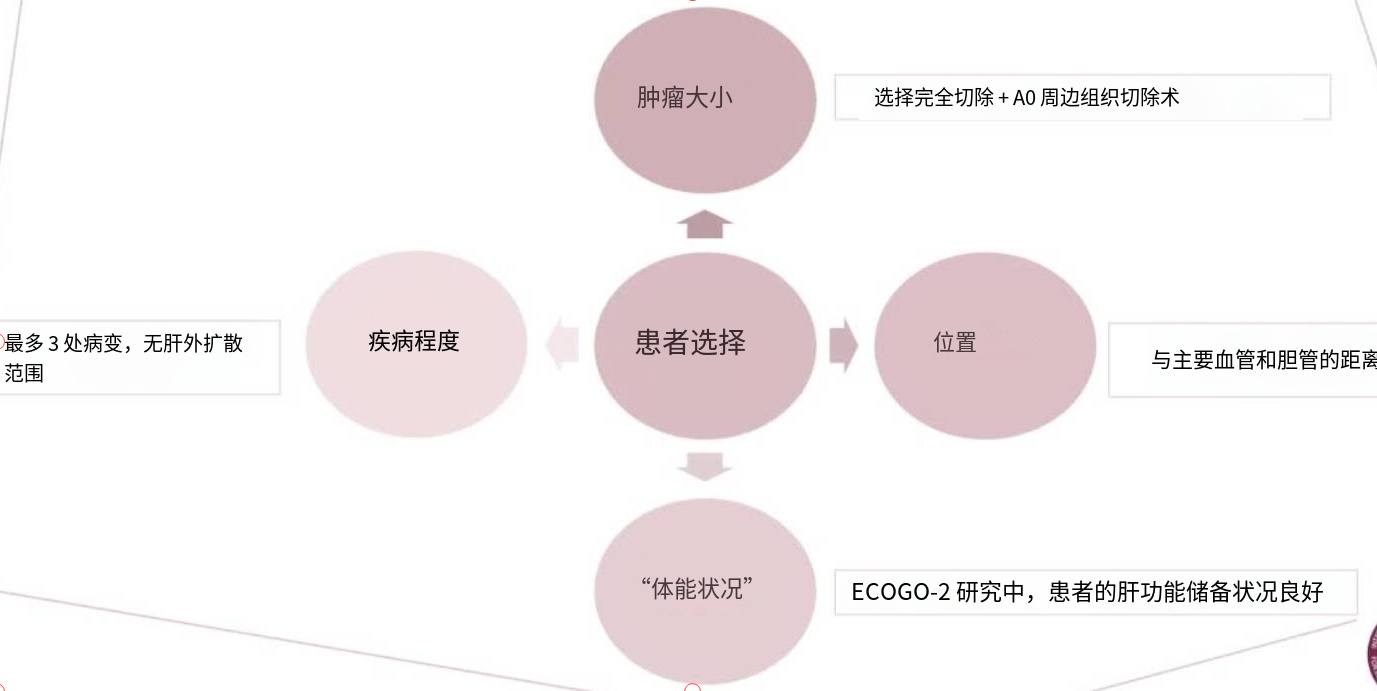
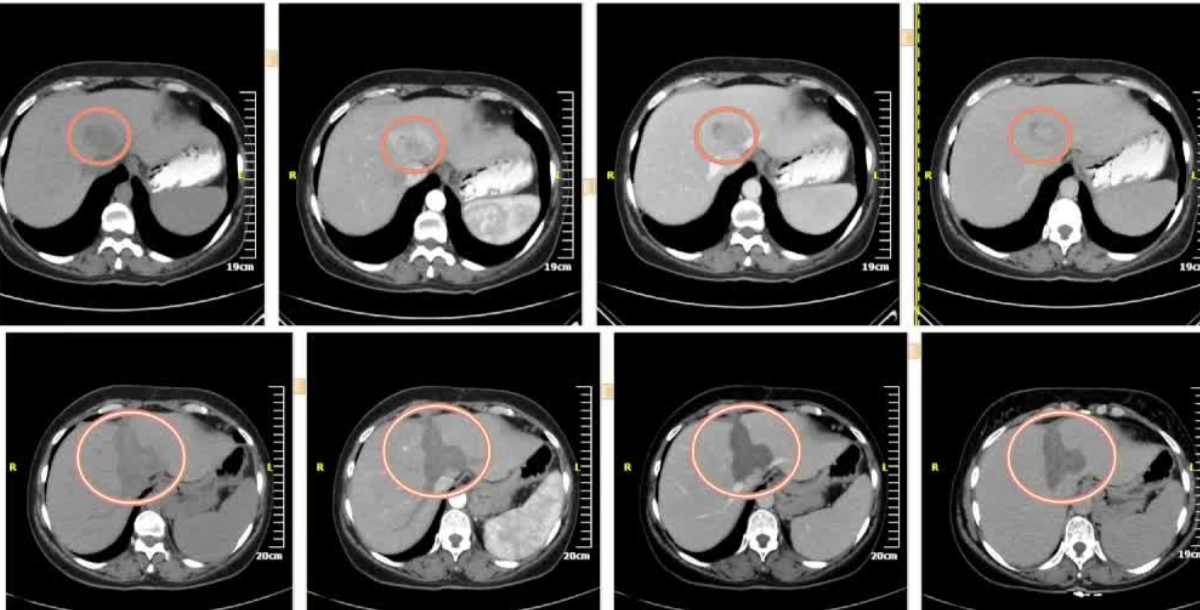
肝内胆管细胞癌i 本站已有定义  肝内胆管癌只占全部胆管癌的10%【Diaz-Gonzales A et al JVIR 2020 Thornblade LW 2021 Chiou YY et al Med Sci 2005】
发病率增加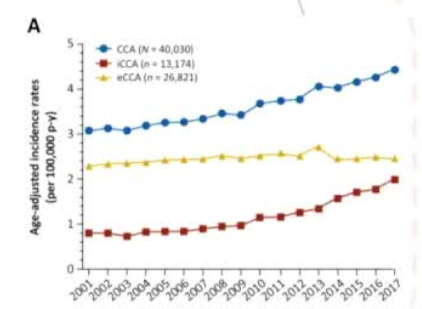 局限性肝内胆管癌(iCCA)的经皮消融治疗,是指通过皮肤将一根细针穿刺到肝脏肿瘤部位,利用高温或高压电脉冲来“烧掉”或“电死”癌细胞的一种微创技术。它主要适用于因年龄、身体状况或肿瘤位置等原因无法接受外科手术切除的患者【Antonio Giorgio 2025】。 主要消融技术分类目前用于肝内胆管癌的经皮消融技术主要可以分为两大类:热消融和非热消融。
临床效果与指南建议
·疗效数据:临床研究显示,对于无法手术的早期肝内胆管癌患者,经皮消融是一种安全有效的替代方案。
在一项针对射频消融的研究中,初治患者的中位总生存期为26个月,中位无复发生存期为11个月。【Clémentine Alitti 2025】
·指南推荐:基于现有证据,德国S3指南已明确建议,对于直径不超过3厘米的不可切除肝内胆管癌,可将经皮热消融(射频或微波消融)作为初治或复发肿瘤的治疗方案之一。【M Mizandar 2018】
创新前沿:值得一提的是,消融技术仍在不断进步。最新的不可逆电穿孔(IRE)技术,特别是被称为“微纳刀”的新一代设备,实现了重要突破。它不仅能在消融肿瘤时完美保护血管和胆管,解决了热消融的“禁区”问题,而且最新的临床实践已成功在局部麻醉下完成手术,患者全程清醒、无痛苦,极大地降低了手术门槛和风险。 总结来说,经皮消融为无法手术的肝内胆管癌患者提供了重要的治疗选择。具体选择射频消融、微波消融还是不可逆电穿孔,需要由经验丰富的多学科团队根据肿瘤的大小、位置、数量以及患者的全身状况来综合决定。 你是主要想了解特定消融方式(如微波消融 vs. 射频消融)的疗效差异,还是对“纳米刀”这类新技术更感兴趣?告诉我你的关注点,我再帮你针对性地整理信息。 -CCA(肝内胆管细胞癌)手术切除——首选治疗方法 切除术后复发率:70% ~ 85% 的所有原发性肝癌患 者将无法进行手术治疗。 消融 回顾性研究— —小型患者样本组 -- 通常会涉及之前接受过手术治疗的患者 非局限性(多发或弥漫) i-CCA• 肝动脉灌注50% 的客观缓解率,中位无进展生存期为 10 个月,中位总生存期为 22 个月。【Veenstra MMK 2024 Franssen S, 2024】 • Y-90 + 全身性治疗 客观缓解率 41%,中位无进展生存期 14 个月,中位总生存期 22 个月。【Julien Edeline 2020 】 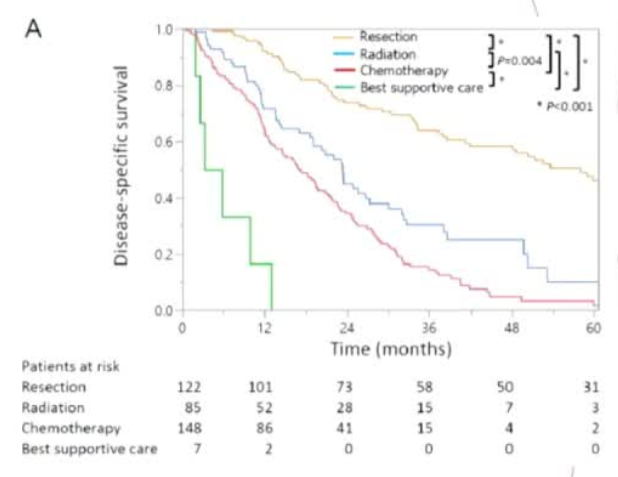 《EASL-ILCA 关于肝内胆管癌治疗的临床实践指南》欧洲肝脏研究协会:热消融技术是否能作为针对直径小于 2 厘米的单发肝内胆管癌的手术治疗的可靠替代方案? 紫建议 对于无法进行切除或手术治疗且单个肿瘤直径小于 2 厘米的不可切除性肝癌患者,热消融治疗可被视为一种较好的替代方案,因为这种方法是可行且安全的(证据级别 4,弱推荐,共识意见)。 局部区域治疗 对于无法手术、局部晚期的肝内胆管细胞癌(iCCA)患者,采用经动脉治疗手段(选择性内照射治疗、化疗栓塞以及动脉内化疗)进行局部区域治疗,是否相较于全身性治疗能带来更长的生存期? 建议 经动脉治疗(选择性内放射治疗、化疗栓塞和动脉内化疗)是可行且安全的,对于某些无法进行手术治疗的患者而言,这种治疗方法可能是合理的替代选择(证据等级 4 级,弱推荐,共识)。 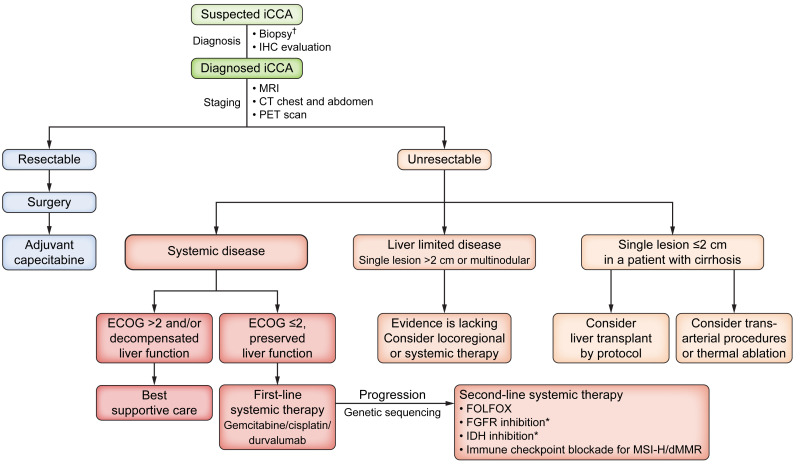 根据您提供的《EASL-ILCA肝内胆管癌临床实践指南》PDF文件,以下是关于肝内胆管癌消融治疗的相关内容整理: 消融治疗在肝内胆管癌中的应用关键问题:对于单发、<2 cm 的肝内胆管癌,热消融是否可作为手术治疗的可靠替代方案? 推荐意见:· 对于无法切除或不适合手术的单发 <2 cm 的肝内胆管癌患者,可考虑热消融作为一种良好的替代治疗方案。、 · 证据级别:LoE 4(低质量证据,基于回顾性研究) · 推荐强度:弱推荐 · 共识程度:共识
|
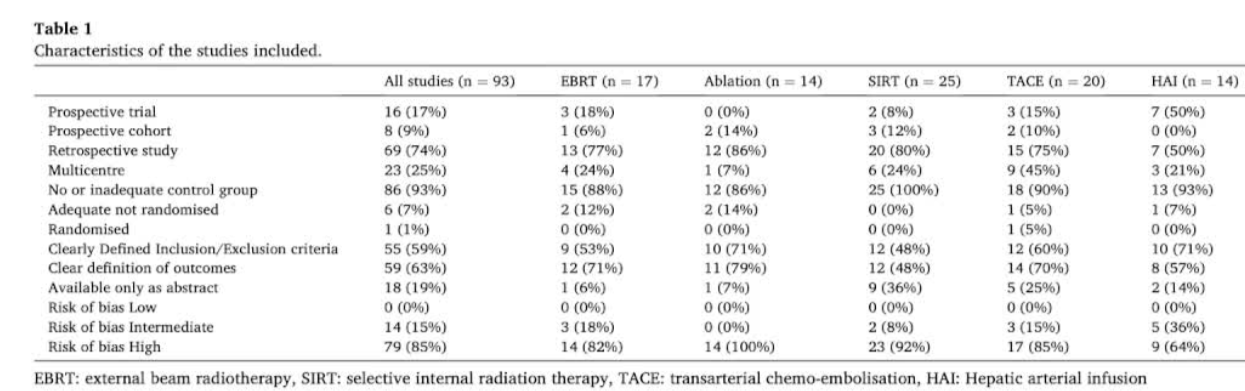
| 治疗方式 | 汇总中位OS月) | 客观缓解率 | 备注 |
| 消融 | 30.2 | 完全缓解率 93.9% | 结果一致,异质性低 |
| 外放疗 | 18.9 | - | 2年局部控制率 69.1% |
| SIRT | 14.1 | 23.4% | 异质性高 |
| TACE | 15.9 | 26.3% | 异质性高 |
| HAI | 21.3 | 41.3% | 异质性高 |
| IAT整体 | 15.7 | 28.6% | 一线+全身化疗者OS达25.2个月 |
亚组分析
·一线治疗 + 全身化疗(IAT):
o 汇总OS:25.2个月
o 客观缓解率:52%
o 二次切除率:14.0%
·提示联合治疗在特定人群中可能带来更好的预后。
研究局限
· 多数研究为单中心回顾性,缺乏对照
· 报告标准不一,许多关键变量(如肝硬化、PS评分)缺失
· 异质性高,限制了对不同治疗方式的直接比较
· 缺乏分子分型数据,无法进行精准分层
结论与建议
· 消融在不可手术患者中表现优异,可推荐使用
· 动脉介入治疗(IAT)在联合全身化疗或化疗耐药患者中具有潜力,但证据质量有限
· 外放疗可在特定患者中考虑,尤其是在消融不可行时
· 呼吁未来开展多中心、前瞻性、随机对照试验,并采用标准化报告体系
 |
 |
| 【Julien Edeline 2021】 |
于肝内胆管癌患者而言,局部区域治疗在治疗中的当前作用的建议。
 |
 |
 |
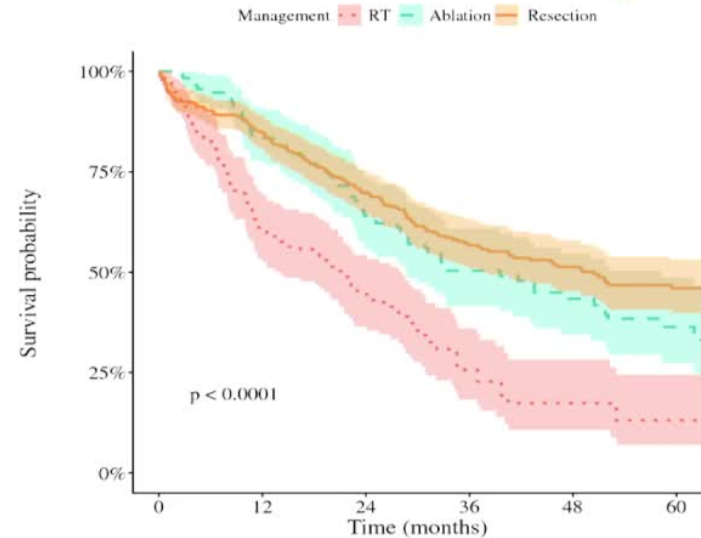
这是一个非常前沿且具有重要临床意义的课题。对于小肝内胆管癌,通常指直径≤3cm或≤5cm、局限于肝内、无血管侵犯及肝外转移的肿瘤,其治疗策略的选择直接影响患者的长期生存。
核心结论速览
1. 肝切除:仍是首选的金标准治疗方案。对于可耐受手术的小ICC,手术切除通常提供最长的无瘤生存期和最佳的总生存期。
2. 局部消融:是不可切除或不能耐受手术患者的最佳替代方案。对于极早期(如≤2-3cm)的肿瘤,消融的疗效在局部控制和长期生存上已非常接近手术,且创伤小、并发症少。
3. 放射治疗:包括立体定向体部放疗,主要适用于不能手术且不适合消融(如位置高风险)的患者,或作为转化治疗/综合治疗的一部分。对于小肿瘤,SBRT也能取得良好的局部控制率,但作为一线根治手段的证据强度弱于前两者。
1. 肝切除
生存数据:
对于早期(I期)小ICC,手术切除后的5年总生存率通常可达40% - 70%,中位生存期往往超过5年。R0切除(切缘阴性)是实现长期生存的关键。
优势:
· 病理分期:手术能获取完整的病理标本,明确淋巴结状态、切缘情况、微血管侵犯等关键预后因素,指导后续辅助治疗。
· 根治性最高:完整切除肿瘤及可能存在的微小卫星灶,理论上复发率最低。
局限性:
· 创伤大:术后并发症发生率(如胆漏、肝衰)相对较高,尤其是对于肝硬化背景或残肝体积不足的患者。
· 肝功能要求高:需要良好的肝功能储备。
2. 局部消融
主要包括射频消融和微波消融。这是与小手术直接竞争的主要手段。
生存数据:
针对小肿瘤:
· 对于≤2cm的肿瘤:多项回顾性研究及Meta分析显示,射频消融的5年OS和RFS与手术切除无显著统计学差异。消融的5年OS可达 40%-60%。‘’
· 对于2-3cm的肿瘤:手术切除在长期生存上通常仍优于消融。虽然消融的局部控制率很高,但手术在清除微转移灶方面更具优势。
· 对于3-5cm的肿瘤:消融的完全消融率下降,局部复发风险显著增高,手术的优势非常明显。
优势:
· 微创:恢复快,住院时间短,并发症发生率低。
· 保留实质:对肝功能影响小,尤其适合肝硬化重或位于肝中央(紧贴大血管、胆管)但技术可及的情况。
局限性:
· 热沉效应:靠近大血管的肿瘤消融不完全。
· 无法评估淋巴结:无法处理潜在的肝门部淋巴结转移。
· 尺寸限制:随着肿瘤增大,疗效断崖式下跌。
3. 放射治疗
特指立体定向体部放疗,以其高精度、高剂量、少分次的特点,在ICC治疗中地位逐渐上升。
生存数据:
缺乏直接比较SBRT与手术的随机对照试验数据,多为单臂研究或与消融的间接比较。
· 局部控制率:对于小肿瘤,SBRT的1年或2年局部控制率可达 80%-90% 以上。中位生存期根据患者群体不同,约为 17-30个月(通常入组的是不能手术的患者,因此生存期数据存在偏倚)。
· 与消融的比较:对于消融困难的部位(如临近大胆管、膈肌、大血管),SBRT显示出独特的适形优势,能安全地递送根治剂量。
20.9% 消融 2
4.6% SBRT 研究期间:
入选标准:I - III 期肝细胞癌(肿瘤直径小于 3 厘米)
优势:
· 非侵入性:完全无创。
· 位置不限:可处理高风险位置的肿瘤(如肝门部、靠近下腔静脉),这是消融的禁忌或难点。
· 免疫调节:可能激发远隔效应。
局限性:
· 放射性肝损伤:存在一定的放射性肝病风险,对肝硬化患者需严格评估。
· 长期随访数据不足:缺乏大样本的10年长期生存数据来佐证其根治效果。
· 无法获取病理:同样无法评估淋巴结状态。
临床决策逻辑图
在选择三种方式时,临床医生通常遵循以下逻辑:
1. 第一步:评估可切除性及手术风险
o 如果适合手术(Child-Pugh A, 残肝体积足够,无合并症):首选肝切除。
2. 第二步:如果不适合手术或拒绝手术
o 评估肿瘤位置和大小:
肿瘤≤3cm,且位置适合(远离大血管/胆管):首选局部消融。疗效近似手术,创伤最小。
肿瘤≤3cm,但位置高危(紧贴胆管/血管):首选SBRT。
肿瘤3-5cm:如果仍不能手术,可尝试大范围消融联合TACE,或SBRT。如果消融困难,SBRT是重要选项。
3. 第三步:综合考量
o如果存在可疑肝门部淋巴结转移,手术切除+淋巴结清扫的价值远高于消融或放疗,因为后者无法处理淋巴结。
未来方向
目前缺乏针对这三种疗法比较的前瞻性随机对照试验。随着放疗技术的进步和消融范围的扩大,未来对于极早期(≤2cm)的ICC,非手术疗法的地位可能会进一步提升。但对于可手术的2-5cm肿瘤,手术切除依然是衡量所有其他疗法的“标尺”。
总结:在小肝内胆管癌的治疗中,手术切除提供最高的根治机会;局部消融是手术的最佳替代;而SBRT则是填补那些“手术不能做、消融做不了”的空缺,并为特定患者提供无创的根治可能。
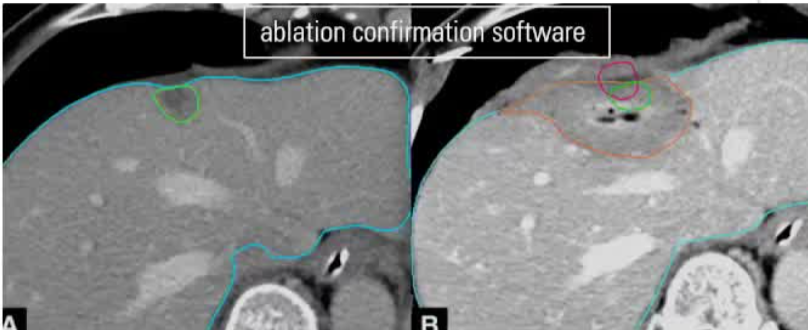
MORFEUS 技术
它目前正由MD安德森癌症中心等顶级机构进行临床研究,旨在使用Morfeus 软件 提高消融手术的精准度
通过生物力学形变配准技术,将术前与术后的CT影像进行三维融合,帮助医生精准判断肿瘤是否被彻底“消融”干净
 |
 |
研究时期:2005 年 - 2023 年 患
者群体:44 名患者,共 78 例肝内胆管细胞癌病例
技术组合:82% 的微波消融技术和 18% 的射频消融技术
1 年生存率:92.7%;2 年生存率:62.2%;3 年生存率:53%
“Software-Aided Imaging (Morfeus) for Confirming Tumor Coverage With Ablation in Patients With Liver Tumors, the COVER-ALL Study”是一项正在进行的临床研究。它的核心目的是测试一种名为“Morfeus”的软件辅助成像技术,能否帮助医生在肝肿瘤消融手术中更精确、更彻底地摧毁肿瘤。
这项研究由知名的MD安德森癌症中心发起,属于第三期临床试验,意味着该技术已经在前期证明有潜力,现在需要在更大范围的患者中验证其效果是否优于当前的标准方法 。
研究背景:
· 治疗现状:对于不能或不宜手术的肝肿瘤患者,消融治疗是一种重要的根治性手段。医生会用一根细针精确插入肿瘤,通过加热或冷冻来“烧掉”或“冻死”癌细胞。
· 核心挑战:手术成功的关键在于“消融边界”,即不仅要消灭可见的肿瘤,还要确保肿瘤周围一圈(通常目标是至少5毫米)的健康组织也被一并清除,以杜绝残留的癌细胞。目前,医生主要依靠肉眼观察手术前后的CT影像来判断,但这并不完全精确,很难保证三维空间上每个方向都达到了安全边界 。
解决方案:
为了应对这一挑战,研究者开发了名为“Morfeus”的软件辅助成像系统。它本质上是一个先进的图像处理工具,能够解决手术中的一个关键难题。
简单来说,Morfeus的核心能力是进行生物力学可变形配准。肝脏是柔软、会变形的器官,手术前和手术中的CT影像因为患者呼吸、体位变化或穿刺针的影响,肿瘤位置会发生位移。Morfeus能将术前带有肿瘤标记的增强CT,与术中放置好消融针后的非增强CT进行高精度地对齐和融合,从而准确地判断消融范围是否完全覆盖了肿瘤 。
研究如何设计
为了科学评估Morfeus的效果,研究采用了随机对照设计,将参与者分为两组进行对比 :
· 第一组 (对照组):接受当前标准的消融治疗。医生依据常规的影像和经验进行手术。
· 第二组 (实验组):接受标准消融治疗 + Morfeus软件辅助。医生在Morfeus提供的三维图像分析指导下进行手术。
研究要评估什么?
研究的主要目的是通过对比两组的数据,来验证Morfeus能否带来实际的临床获益。评估标准包括 :
·主要目标:评估使用Morfeus后,医生是否能在三维空间中实现更大的“最小消融边界”。这是衡量手术彻底性的关键指标。
·次要目标:观察使用Morfeus能否带来更长远的益处,比如:
o降低局部复发率:肿瘤在原来位置复发的可能性是否更低?
o提高生存率:患者的总体生存时间、无进展生存时间是否延长?
o评估安全性:使用新技术是否会增加并发症,或影响患者的生活质量和肝功能?
这项研究预计在2026年1月完成,届时将为我们揭示这种智能化影像技术能否成为提高肝肿瘤消融精准度的有力工具 。

本文是2015年的一篇关于射频消融(Radiofrequency Ablation, RFA)在治疗不可切除的肝内胆管癌(Intrahepatic Cholangiocarcinoma, ICC)中的临床疗效和安全性的系统评价和荟萃分析,文章发表的比较早。研究通过检索Ovid MEDLINE和EMBASE数据库,收集了描述RFA用于治疗ICC的研究,并对总体生存率、局部肿瘤进展和并发症的数据进行了汇总分析。
主要观点
研究目的
- 系统评价与荟萃分析:旨在评估RFA在治疗ICC中的临床有效性和安全性。
文献检索与纳入标准
-
数据库检索:从Ovid MEDLINE和EMBASE数据库中进行全面文献搜索。
-
研究类型:纳入描述RFA用于治疗ICC的观察性研究。
-
患者数量:共纳入7项研究,涉及84名患者。
生存率数据
-
1年生存率:82%(95%置信区间:72%–90%)
-
3年生存率:47%(95%置信区间:28%–65%)
-
5年生存率:24%(95%置信区间:11%–40%)
并发症情况
-
主要并发症:4项研究中出现1或2例主要并发症。
-
严重并发症案例:1名患者因肝脓肿和继发性败血症死亡,尽管接受了经皮引流和抗生素治疗。
核心结论
- RFA作为局部治疗选择:RFA是一种有效的局部治疗方法,可以延长不适合手术的ICC患者的生存期。
总结
本文通过对7项观察性研究的系统评价和荟萃分析,展示了射频消融(RFA)在治疗不可切除的肝内胆管癌(ICC)中的显著效果。研究结果显示,RFA能够显著提高患者的生存率,1年、3年和5年的生存率分别为82%、47%和24%。尽管存在一定的并发症风险,但RFA作为一种局部治疗手段,为那些无法接受手术的患者提供了重要的治疗选择,延长了他们的生存时间。因此,RFA在ICC治疗中具有重要的临床价值。
SBRT 治疗 iCCA 的中位总生存期 1 年、2 年和 3 年的总生存率分别为 51.2%、32.6% 和 23.3%

本文是一篇关于评估肝内胆管癌(Intrahepatic Cholangiocarcinoma, ICC)患者在接受超声引导下的经皮微波消融(Microwave Ablation, MWA)治疗后预后的研究论文。研究旨在确定白蛋白-胆红素(Albumin-Bilirubin, ALBI)分级是否可以用来预测这些患者的治疗结果。该研究是一项回顾性研究,涵盖了2011年4月至2018年3月期间接受MWA治疗的52名初治患者及其74个肿瘤病变。
主要观点
研究目的
- 确定ALBI分级是否能预测ICC患者在超声引导下经皮微波消融后的预后。
研究方法
-
研究设计:回顾性研究,获得机构审查委员会批准,免除知情同意要求。
-
研究对象:52名未接受过治疗的ICC患者,共74个肿瘤病变,符合米兰标准。
-
随访时间:中位随访时间为21.2个月(范围3.2-78.7个月)。
-
分析方法:使用log-rank检验比较Child-Pugh评分和ALBI分级分组的整体生存率(OS)和无复发生存率(RFS),并用Cox比例风险回归分析确定影响生存的预后因素。
研究结果
-
生存率:
-
总体生存率(OS):1年、3年和5年的累积OS率分别为87.4%、51.4%和35.2%。
-
无复发生存率(RFS):1年、3年和5年的累积RFS率分别为68.9%、56.9%和56.9%。
-
-
并发症:主要并发症发生率为3.8%(2/52)。
-
ALBI分级的影响:
-
ALBI 1级患者的1年、3年和5年OS率分别为95.5%、72.4%和72.4%。
-
ALBI 2级患者的1年、3年和5年OS率分别为62.5%、40.6%和36.3%,两者之间存在显著差异(P = 0.006)。
-
-
多变量分析:
-
年龄较大(HR: 1.67, 95% CI: 1.11-2.82; P = 0.002)
-
肿瘤直径≥3厘米(HR: 11.33, CI: 2.24-34.52; P = 0.021)
-
ALBI分级(HR: 8.23, CI: 1.58-58.00; P = 0.004)
-
研究结论
- ALBI分级被证实为预测米兰标准内ICC患者在MWA治疗后生存的重要生物标志物。
总结
本文通过一项回顾性研究,探讨了ALBI分级在预测肝内胆管癌患者接受超声引导下经皮微波消融治疗后预后中的作用。研究结果显示,ALBI分级能够显著区分不同患者的生存率,且多变量分析表明ALBI分级、年龄和肿瘤大小是影响患者总体生存率的关键预后因素。因此,ALBI分级被验证为预测此类患者生存的一个重要生物标志物。这一发现对于临床实践中选择合适的治疗策略和评估患者预后具有重要意义。

本文报道了一项多中心回顾性研究,探讨了在肝恶性肿瘤直径大于3厘米的患者中,结合使用球囊阻断微波消融(b-MWA)和球囊阻断经动脉化疗栓塞(b-TACE)的综合治疗方法。研究重点在于评估坏死区的外观和体积、安全性以及肿瘤学结果。
主要观点
球囊辅助微波消融术 + DEB-TACE 技术
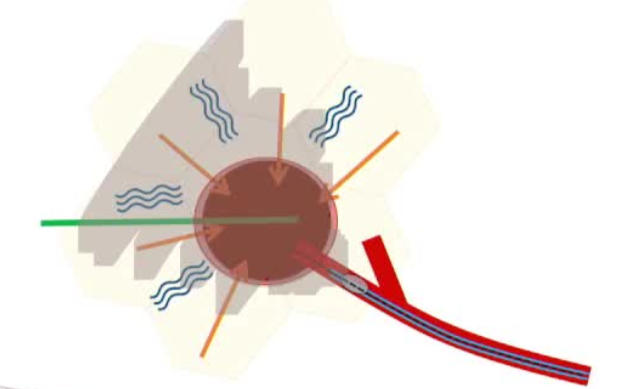
研究目的
- 目标:报告在肝恶性肿瘤患者中使用b-MWA后继以b-TACE的多中心回顾性经验,重点关注坏死区的外观和体积、安全性和肿瘤学结果。
材料与方法
-
患者群体:共纳入23名患者,其中原发性肝癌(HCC)18例,肝内胆管癌(iCC)2例,转移性肿瘤(结直肠癌转移1例,肉瘤转移1例,乳腺癌转移1例)。
-
病变特征:最大平均直径为4.4厘米(±1厘米)。
-
治疗流程:采用单一步骤方法,先进行b-MWA,然后进行b-TACE(使用表柔比星或伊立替康)。
1. 肝动脉造影术
2. 微球囊导管定位
3. 球囊充盈阻塞肝动脉
4. 流量重新分配
5. 超声引导下的穿刺定位
6. 热消融
-
评估指标:术后CT评估坏死区形状和体积与供应商消融图表预期体积的差异;根据CIRSE分类评估并发症;使用m-RECIST(HCC)和RECIST v1.1(转移性肿瘤/iCC)评估1个月和3-6个月的肿瘤学结果。
研究结果
-
坏死区体积:平均坏死区体积为75立方厘米(±36),与供应商图表相比,坏死区体积增加中位数为103.2%(±99.8%)。
-
坏死区形状:22/23名患者(95.7%)的坏死区呈非球形。
-
并发症:无严重并发症发生,12/23名患者出现术后栓塞综合征。
-
肿瘤学结果:
-
完全缓解:1个月时为91.3%(21/23),3-6个月时为85.7%(18/21)。
-
部分缓解:1个月时为8.7%(2/23),3-6个月时为9.5%(2/21)。
-
疾病进展:3-6个月时,1/21名患者出现远处转移。
-
肿瘤体积减小:部分反应者的平均肿瘤体积减小率为78.8%(±9.8%)。
-
结论
-
主要发现:b-MWA后继以b-TACE的单一步骤程序导致的坏死区体积大于供应商消融图表所建议的体积,且呈非球形,与消融期间阻断的血管段相吻合。
-
安全性与疗效:该方法能够安全地在大于3厘米的肿瘤患者中获得令人鼓舞的肿瘤学结果。
总结
本文通过一项多中心回顾性研究,展示了在肝恶性肿瘤患者中使用b-MWA后继以b-TACE的综合治疗方法的有效性和安全性。研究结果显示,这种单一步骤程序不仅能够产生比供应商消融图表预期更大的坏死区,而且能够显著提高肿瘤的完全缓解率和部分缓解率,同时保持良好的安全性。核心观点是,这种方法为治疗大于3厘米的肝恶性肿瘤提供了一种有效的新选择。