 这篇CIRT研究的预设亚组分析是对结直肠癌肝转移SIRT预后因素的深入挖掘,为我们之前讨论的CIRT主研究(2020年)提供了更精细的临床筛选工具。 核心结论:APRI是预测SIRT疗效的最强独立因子,分区剂量学改善OS CIRT:转移性结直肠癌预后 - APRI 评分这项分析(2022年发表于《Clinical Colorectal Cancer》)聚焦于CIRT研究中的237例结直肠癌肝转移患者,旨在寻找能够预测SIRT(树脂微球)疗效的独立预后因素。主要发现:
名词解释:风险比
风险比(Hazard Ratio, HR) 是医学研究中衡量两组患者发生某个事件(如死亡、疾病进展)速度差异的统计指标。它回答了这样一个核心问题:与对照组相比,试验组患者在任意时间点发生事件的风险是更高还是更低?
1. HR的核心解读
- HR = 1:两组发生事件的风险无差异。
- HR < 1:试验组风险更低,有利于试验组。例如HR=0.69意味着试验组的风险降低了31%。
- HR > 1:试验组风险更高,不利于试验组。例如HR=1.04意味着试验组的风险增加了4%。
2. 结合你提供的文献实例解读
为了更好地理解,我们来看你之前文件中提到的两个具体案例:
- 之前FOXFIRE研究(HR=1.04):该研究评估在一线化疗基础上加用SIRT。HR=1.04,95%置信区间(CI)为0.90-1.19。这表示SIRT组的死亡风险比单纯化疗组高4%,但置信区间范围从低风险(-10%)到高风险(+19%)。由于区间包含1(无差异)且p=0.61,统计上无显著差异。结论是:加用SIRT没有带来生存获益。
- EPOCH研究(HR=0.69):该研究评估在二线化疗基础上加用SIRT。HR=0.69,95% CI为0.54-0.88。这表示SIRT组患者的疾病进展或死亡风险比化疗组降低了31%。置信区间整个小于1,p=0.0013,有显著统计学差异。结论是:加用SIRT显著延长了无进展生存期。
3. HR与中位生存时间的区别
- 中位生存时间:描述的是一个时间点,即“50%的患者死亡或进展的时间点”。它直观,但只看一个点。
- HR:描述的是整个生存曲线上的平均风险比。它利用了所有时间点的数据,信息量更大。即使两组中位生存时间接近,如果其中一组早期事件更多,HR也能捕捉到这种差异。
4. 如何从HR和置信区间快速判断研究结果?
在论文中,会看到类似这样的报告:`HR 0.69 95%CI,0.54to0.88;P=.0013`
- 核心估值 (0.69):这是对风险比的最佳估计值。
- 95% 置信区间 (0.54, 0.88):这是一个可信范围。有95%的把握认为真实的HR值落在这个区间内。
- 判断标准:如果整个95% CI都大于1,说明试验组风险显著更高(有害);如果整个95% CI都小于1,说明试验组风险显著更低(有益);如果95% CI跨过1(例如0.90-1.19),则结果没有统计学显著性(p > 0.05)。
5. HR的优势
- 处理删失数据:临床试验中,有些患者可能因失访、退出或研究结束时仍存活而无法观察到事件终点。HR能有效利用这些“删失”数据,而中位生存时间等简单指标则不能。
- 不受时间点选择影响:不依赖于像“6个月生存率”这样人为选定的时间点,而是评估整个研究期间的风险。
- 提供更多信息:两组的中位生存时间可能相同,但HR能揭示更早或更晚发生的事件模式差异。
总结
在解读之前提供的文献时,可以这样理解:
- EPOCH研究:HR=0.69 (PFS),意味着在任意时间点,SIRT联合化疗组的进展或死亡风险比单纯化疗组低31%,这是有统计学意义的获益。
- FOXFIRE研究:HR=1.04 (OS),意味着SIRT联合化疗组的总死亡风险略高于化疗组,但统计上无显著差异。
希望这个解释能帮助你更清晰地理解HR。如果你对具体的统计公式或应用还有疑问,随时可以继续交流。
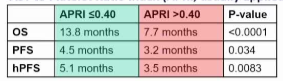
什么是APRI、ALBI、INR?(临床可及性极强)这三个指标均为常规血检可得的肝功能/储备指标,无需额外检查:
临界值:
- APRI ≤ 0.40 为正常/低风险,> 0.40 为高风险(研究中最强预测因子)
- ALBI 分为1级(最佳)、2级、3级(最差) - INR ≤ 1 为正常,> 1 为异常
白蛋白与血小板比值指数(APRI,通常用于评估纤维化和肝硬化情况)
 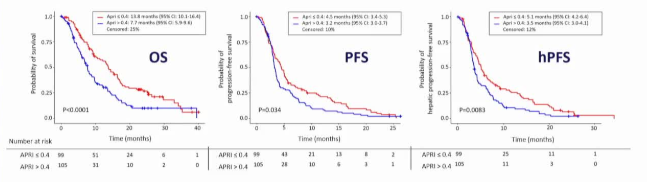 为什么分区模型在多因素分析中显著改善OS(HR 0.45, p=0.012),但在倾向性评分分析中却不显著了(p=0.0792)。深层需求是理解这些不同统计方法得出的结论之间是否存在矛盾,以及在实际临床或科研中应该如何解读和权衡这些证据。 这很可能是因为倾向性评分分析虽然能校正混杂因素,但需要足够的样本量。原文提到只有42/237例(17.7%)使用了分区模型,样本量小可能导致倾向性评分分析效能不足,统计把握度不够,所以p值只是边缘显著。而多因素分析是更标准的方法,结果更可靠。
结论:综合两项分析,分区模型很可能改善OS。多因素分析提供了有力证据,倾向性评分分析结果不显著可能与样本量小有关。 关键困惑:为什么PM改善OS,却不改善PFS/hPFS? 这是你提供的第二个核心问题:OS P=0.0080(多因素分析中PM的p值),但PFS P=0.4144,hPFS P=0.9788,后两者完全不显著。 这个“OS阳性,PFS阴性”的现象在肿瘤局部治疗研究中并非罕见,可能的原因如下:
为什么APRI如此重要?(机制探讨)研究者提出了合理解释:
1. 化疗相关性肝损伤的标志:奥沙利铂、伊立替康等一线化疗药物可导致肝窦损伤、脂肪性肝炎,APRI升高反映了这种潜在的肝脏损伤。
2. 肝纤维化的非侵入性指标:APRI已广泛用于预测肝纤维化程度,而肝纤维化会影响SIRT后的肝功能恢复。 3. 血小板减少的意义:慢性肝病中血小板减少与促血小板生成素产生减少相关,反映了肝细胞功能储备下降。 临床启示:APRI是一个简单、廉价、可重复的预测工具,应纳入SIRT前的常规评估。 分区模型剂量学 vs 体表面积法(BSA)这是另一个关键发现:
解读:使用分区模型进行剂量计算的患者,总生存期显著优于BSA法(死亡风险降低55%)。这与肝细胞癌中“个体化剂量优于标准剂量”的DOSISPHERE-01试验结论一致,首次在结直肠癌肝转移中得到验证。 本研究中CIRT mCRC亚组的基线数据 本研究中CIRT mCRC亚组的基线数据
PFS低于EPOCH的原因:本研究患者更晚期(65%为≥2线,EPOCH为严格的二线),且未要求同步化疗(EPOCH为SIRT+化疗)。 安全性(本亚组)
任何不良事件:40.1%(95/237)
≥3级不良事件:11.8%(28/237)
o 腹痛 1.7%
o 胃肠道溃疡 0.8% o 胃炎 0.8% o 放射性胆囊炎 0.4% o 恶心 0.4%
·其他≥3级不良事件:7.6%(18/237,29起事件)
与既往研究的对比
差异解读:CIRT子分析聚焦于肝功能/储备指标,而EPOCH聚焦于分子/肿瘤特征(KRAS、原发瘤位置)。两者互补——前者评估“肝脏能否承受SIRT”,后者评估“肿瘤是否对SIRT敏感”。 本研究的局限性
1. 观察性设计:存在选择偏倚,非随机对照。
2. 剂量学数据不完整:仅42/237(17.7%)使用分区模型,样本量较小。 3. 无中心影像学评审:PFS/hPFS由各中心研究者评估,可能存在偏倚。 4. 未收集分子标志物:无KRAS/NRAS/BRAF状态、原发瘤位置(右半/左半)等信息。 5. 失访率较高:26.2%的OS数据被删失。 6. 后续治疗影响:36.7%的患者在SIRT后接受了进一步全身治疗,可能影响OS分析。 临床实践意义
1. APRI应纳入SIRT前常规评估:APRI > 0.40的患者SIRT预后显著更差,应考虑替代治疗或更谨慎的患者选择。
2. ALBI 3级患者需谨慎:肝内进展风险增加429%,提示肝功能储备极差的患者不适合SIRT。 3. INR > 1是独立风险因子:反映肝脏合成功能下降,应纳入综合评估。 4. 分区模型剂量学优于BSA:本研究首次在mCRC中证实分区模型可改善OS,建议在有条件的中心采用个体化剂量计算。 5. 既往局部治疗史是保护因素:提示对肝脏定向治疗反应良好的患者,再次接受SIRT效果更佳。 临床筛选流程图(整合本研究发现)  这项CIRT子分析为SIRT的患者筛选提供了重要的工具:- APRI > 0.40 是最强的负面预测因子(死亡风险增加125%) - ALBI 3级 患者肝内进展风险极高(增加429%),应避免SIRT - 分区模型剂量学 可显著改善OS(死亡风险降低55%),应作为技术标准 对临床的指导:在考虑SIRT之前,应常规检测APRI、ALBI、INR。APRI ≤ 0.40、ALBI 1-2级、INR ≤ 1的患者是理想的候选者。同时,应优先采用分区模型进行剂量计算,而非传统的BSA法。 |

