经验性/预防性栓塞术 Empiric/Prophylactic embolization
定义:
经验性栓塞是指在血管造影术中,未能直接观察到造影剂外溢(即“出血直接征象”),但基于临床(如活动性出血)、内镜(已定位出血肠段)或影像学(如CT血管造影提示可能出血区域)证据,对高度怀疑的出血肠段供血动脉进行超选择性栓塞。
1. 当 CTA(CT 动脉造影)结果为阳性而血管造影结果为阴性时,可考虑此疗法。
2. 利用 CB-CT 技术来确定肠道的区域,使其与 CTA 所确定的位置相匹配。
3. 尽可能进行超选择性操作,以减少潜在的缺血情况。
4. 用聚乙烯醇进行栓塞(小颗粒,少量)< 胶水
应用背景与临床意义
重要性:
急性下消化道大出血中,约有40%-50% 的病例在血管造影时出血已暂时停止或呈间歇性,无法显示直接出血征象。
目的:
避免被动等待再出血,主动干预以降低再出血率、避免急诊外科手术及降低死亡率。
前提:
必须在超选择性插管至血管弓以远(如直动脉/vasa recta)的水平进行,以最大限度减少肠缺血风险。
适应症(何时考虑经验性栓塞?)
明确的临床活动性出血:持续便血、血流动力学不稳定,需要持续输血。
内镜定位:结肠镜/胶囊内镜已明确出血位于某一特定肠段(如右半结肠、某段小肠),但无法内镜下止血或止血失败。
CT血管造影提示:CTA显示某肠段血管异常(如造影剂外溢、血管畸形、肿瘤染色),但DSA造影时外溢停止。
血管造影发现可疑病变:如明确的血管发育异常(血管扩张症)、动脉瘤、肿瘤血管,即使未见外溢,也可视为责任病变进行栓塞。
栓塞目标与原则
目标血管:直动脉(vasa recta)。这是供应肠壁的终末小动脉,在此水平栓塞最安全、最有效。
“三明治”肠段原则:
若内镜或CTA已准确定位,则栓塞该肠段的供血动脉。
若定位不精确,则栓塞临床和影像学最可疑的肠段。
对于盲肠等血供复杂区域,可能需栓塞多支血管(如回结肠动脉、右结肠动脉分支)。
栓塞材料:
首选:微弹簧栓子。可精确释放,实现永久性闭塞。
可选:明胶海绵颗粒(临时栓塞剂)、聚乙烯醇颗粒(PVA)或新型微球。使用颗粒时需格外注意反流风险。
绝对禁忌:在非超选择性的主干动脉(如肠系膜上/下动脉主干、大的边缘动脉弓)进行栓塞,会导致大范围肠梗死。
技术步骤
全面造影:完成肠系膜上动脉、肠系膜下动脉及腹腔动脉(排除上消化道来源)的详细造影。
超选择性插管:使用微导管(通常2.0-2.8Fr)超选择至可疑肠段的直动脉水平。
““激发”试验(可选但存在争议):部分术者会使用肝素、硝酸甘油或罂粟碱等血管扩张剂,试图诱发出血显影。因其可能诱发非责任血管出血,需谨慎使用。
决策与栓塞:若无造影剂外溢,但结合临床高度怀疑,则在直动脉水平释放栓塞材料。通常栓塞2-3支相邻的直动脉即可覆盖一个肠段。
术后造影:栓塞后需行主干动脉造影,确认目标血管闭塞,并确保无其他侧支出血。
疗效与安全性
临床成功率(即刻止血):可达80%-90%。
再出血率:约15%-25%,可能源于栓塞不完全、侧支循环形成或其他部位新发出血。
主要风险——肠缺血/梗死:
发生率已从早期的约10%降至目前的1%-3%,这归功于超选择性栓塞技术的普及。
高危因素:低血压/休克状态、栓塞水平过近(非直动脉)、栓塞范围过大、使用液体或过小颗粒栓塞剂、存在基础血管疾病(如动脉硬化)。
其他并发症:穿刺点血肿、动脉夹层、非靶向栓塞。
临床诊疗路径中的位置
经验性栓塞是急性下消化道出血多学科诊疗链条中的重要一环:
初始复苏与评估。
结肠镜检查(必要时)。
CT血管造影(定位及筛查)。
介入放射科血管造影 → 若见外溢则行 靶向栓塞 → 若未见外溢则评估行 经验性栓塞。
失败或复发后:考虑重复介入、外科手术(如肠段切除术)。
总结与要点
经验性栓塞是一种积极的、基于证据的介入治疗策略,适用于活动性下消化道出血但血管造影阴性时。
其安全有效的核心是超选择性插管技术,必须在直动脉水平进行。
需要多学科协作(急诊科、消化内科、介入放射科、胃肠外科),结合临床、内镜和影像信息共同决策。
主要目标是控制出血、避免急诊手术,为后续病因治疗创造条件。
这种方法显著改变了急性下消化道出血的管理模式,使许多原本需要紧急外科手术的高危患者能够通过微创方式得到稳定。

急性下消化道出血(LGIB)在临床治疗中存在挑战,尤其是当CT血管造影(CTA)显示阳性,但后续数字减影血管造影(DSA)为阴性时,治疗方案的选择陷入困境。
二、方法创新
该研究采用回顾性方法,对2008年1月至2019年7月间,CTA阳性且在24小时内接受DSA检查的LGIB患者进行研究。针对DSA阳性患者采用靶向栓塞(TE组);DSA阴性患者则分为两组,一组进行锥形束CT(CBCT)引导下对假定破裂的直肠血管进行经验性栓塞(EE组),另一组不进行栓塞(NE组)。与传统靶向栓塞不同,这种CBCT引导的经验性栓塞扩展了“经验性”栓塞策略在LGIB中的应用。
三、核心结果
-
整体情况:共纳入85例患者(平均年龄67.6 ± 15.7岁,52例男性),其中TE组47例,EE组19例,NE组19例。DSA阳性时,靶向栓塞技术成功率为100%(47/47);DSA阴性且采用经验性CBCT引导栓塞时,技术成功率同样为100%(19/19)。TE组、EE组和NE组的再出血率分别为17.0%(8/47)、21.1%(4/19)和52.6%(10/19),总体再出血率EE组低于NE组,但差异无统计学意义。
-
亚组分析:在血流动力学不稳定亚组中,EE组再出血率显著降低(3/10 vs 10/12,p = 0.027)。
-
安全性数据:严重缺血并发症仅发生在1例TE组患者中,总体住院死亡率为7.1%(6/85)。
四、临床价值
-
扩展治疗适应症:这种CBCT引导的经验性栓塞技术使CTA阳性但DSA阴性的患者也能接受超选择性经验性栓塞治疗,解决了DSA阴性时的治疗盲区。
-
改善预后:尤其在血流动力学不稳定的患者中,该技术显著降低了再出血率,提高了临床治疗的成功率,可作为DSA阴性患者的二线治疗选择。
不过,该研究也存在一定局限性,样本量较小(EE组19例,亚组分析仅10例)且为回顾性设计,可能引入偏倚。同时,该技术需由熟练掌握CBCT技术的团队操作,且需排除肠缺血高风险患者。

Endoscopy Localization for Empiric Embo
 |
 |
|
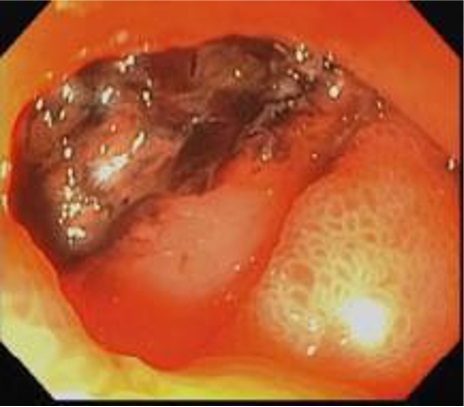
Duodenal ulcer with clot on it |
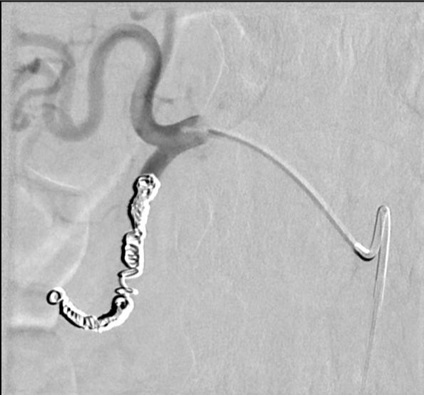
Empiric GDA embo Bleeding stopped, Hgb stabilized
|
Endoscopic Clip Localization
Embolization Outcomes
Targeting Extravasation vs Empiric Embolization
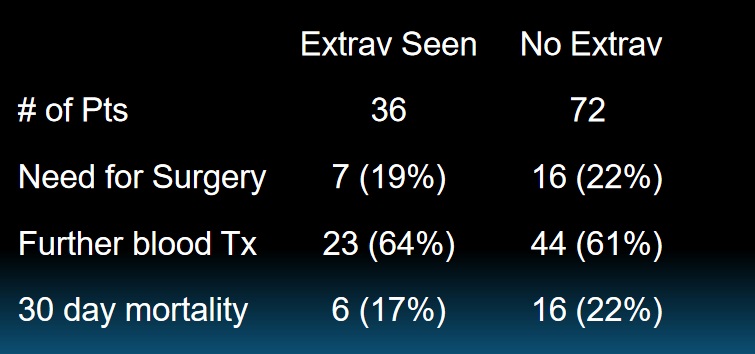
Padia - 2009 JVIR; 20:461
Role of Empiric GDA Embolization
40 pts with duodenal source of bleeding
Proven by endoscopy, CTA, or surgery
Dixon - CVIR 2013;36(4):970
Empiric Lower GI Embolization
Feld - JVIR 2010;21(4):593
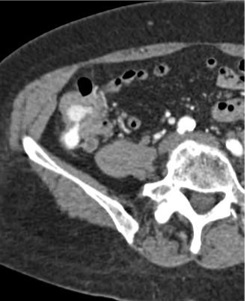
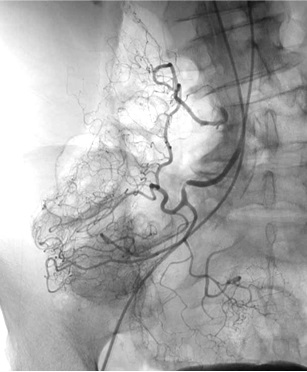
Empiric Colonic Embo Case
 |
 |
 |
|
Bleeding into diverticulum
|
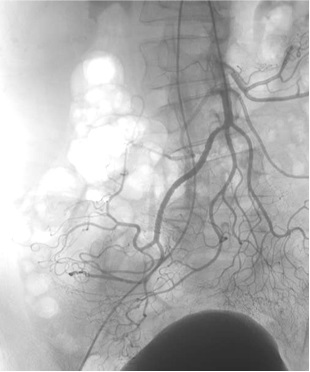
Region of bleeding tic
|
Post embo |
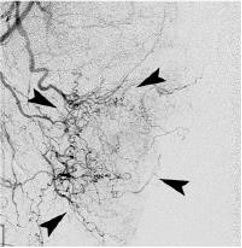
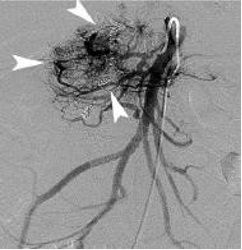
Empiric Embo of Tumor Related GI Bleed
 |
 |
|
Rectal CA |
Met to duodenum |
-
37 angios in 26 patients
-
Most had findings of tumor
Neo or hyper-vascularity
91% for acute bleeding
50% for chronic bleeding
-
No ischemic complications
Tandberg - 2012 JVIR 23:1445
Attention to details critical for good angiography CO2 may be beneficial Provocative angio useful and safe Empiric embolization for LGIB bleeding Beginning to be safely used True value yet to be determined


Empiric/Prophylactic embolization
1. Works when CTA is positive but angio negative
2. Use CB-CTs to determine the area of the bowel, compatible withthe CTA location
3. Decrease the potential ischemia by going superselectively as much as possible
4. Embolize with PVA (small particles, little amount) < glue
总结的这四点,精准地概括了经验性/预防性栓塞在急性下消化道出血中的核心逻辑、技术要点与材料选择。
这是在CTA 阳性但 DSA 阴性这一临床困境下的重要应对策略。结合们之前讨论的所有证据(尤其是Yu 2024 Meta 分析和Valek 2013 指南),将这四点逐条拆解并深度解读。
1. 核心场景:CTA 阳性,但 DSA 阴性
“Works when CTA is positive but angio negative”
临床困境:
· CTA 阳性:提示存在活动性出血(造影剂外溢)或明确出血点(如假性动脉瘤、血管畸形)。
· DSA 阴性:因出血是间歇性的,或血流速度未达到 DSA 检出阈值(约 0.5 mL/min,而 CTA 可检出 0.3 mL/min),导致造影时未见外溢。
经验性栓塞的逻辑:
· 既然 CTA 已经明确了出血的大致区域(如升结肠、回肠末段),而 DSA 虽然阴性,但患者的临床表现(持续便血、血流动力学不稳定)强烈提示出血仍在继续。
· 此时,若仅因 DSA 阴性就放弃栓塞,患者可能面临持续出血、反复输血甚至死亡的风险。
· 经验性栓塞就是基于 CTA 的定位信息,对该区域的潜在出血血管进行预防性栓塞。
与之前文献的衔接:
· Valek 2013 指南指出:若 CTA 阴性,后续 DSA 阳性率很低,应谨慎决定是否行 DSA。反过来说,若 CTA 阳性,即使 DSA 阴性,也应积极考虑经验性栓塞。
· Yu 2024 Meta 分析中,经验性栓塞的再出血率(23.6%)与靶向栓塞(21.1%)相当,但缺血率更高(14.3% vs 4.7%)。这说明经验性栓塞有效,但需要更精准的技术来降低缺血风险——这正是第 2、3、4 点要解决的问题。
2. 精准定位:锥形束 CT 导航
“Use CB-CTs to determine the area of the bowel, compatible with the CTA location”
技术原理:
· 锥形束 CT(CB-CT)是 DSA 设备自带的三维成像功能。在血管造影过程中,通过旋转 C 臂获取三维图像。
· 可以将术前 CTA 的图像与术中 CB-CT 的图像进行融合,精确地将 CTA 上看到的出血点对应到 DSA 的血管解剖上。
如何降低缺血风险:
· 如果没有 CB-CT,经验性栓塞可能只能根据 CTA 的粗略定位,栓塞一个较大的血管区域(如整个右结肠动脉),导致大范围缺血。
· 有了 CB-CT,可以精确定位到与 CTA 出血点对应的那 1-2 支直动脉,从而实现靶向性经验性栓塞,大大减少缺血范围。
与之前文献的衔接:
· Yu 2024 Meta 分析中引用了Hermie 2020的研究,该研究使用 CB-CT 指导经验性栓塞,取得了与靶向栓塞相当的止血效果,同时缺血率更低。
· 这与Kodani 2016中“单支直动脉单分支栓塞安全”的原则一致:CB-CT 帮助医生实现这种“超选择性经验性栓塞”。
3. 操作核心:尽可能超选择性
“Decrease the potential ischemia by going superselectively as much as possible”
原则:
· 无论是靶向栓塞还是经验性栓塞,超选择性是降低缺血风险的核心。
· 经验性栓塞时,因为没有 DSA 下的“造影剂外溢”作为终点,医生容易“心里没底”,倾向于栓塞更粗大、更近端的血管以确保止血。
· 但正是这种做法导致了更高的缺血风险(Yu 2024 中经验性栓塞缺血率 14.3% vs 靶向 4.7%)。
操作要点:
· 必须使用微导管(1.8-3F)进行超选择性插管。
· 目标位置:在结肠区域,应到达直动脉(vasa recta)水平,而不是停留在边缘动脉。
· 范围控制:严格遵循Jae 2008 动物实验和Kodani 2016 临床研究的原则——尽可能将栓塞范围控制在单支直动脉、单分支。若无法做到,也应控制在 ≤2 支直动脉。
· 借助 CB-CT:如前所述,用 CB-CT 来确认微导管的位置是否与 CTA 的出血点匹配。
4. 材料选择:PVA(小颗粒、少量)优于胶
“Embolize with PVA (small particles, little amount) < glue”
这是经验性栓塞中非常关键且具有争议的一点。它反映了对缺血风险和可控性的考量。
(1)为什么选 PVA(聚乙烯醇颗粒)?
· 颗粒随血流走:PVA 颗粒会随血流进入末梢,栓塞出血点所在的毛细血管床。在经验性栓塞中,这可以确保“即使没有看到外溢,也能栓塞到实际出血点”。
· 可控性好:通过少量、多次注射,可以控制栓塞范围。
· 可联合使用:如果担心颗粒栓塞不彻底,可以在颗粒栓塞后,在近端放置一个小弹簧圈作为“加强”。
(2)为什么“少量”(little amount)?
· 防止过度栓塞:经验性栓塞时,因为没有明确的“外溢停止”终点,容易注射过多颗粒,导致颗粒反流或弥散到非目标直动脉,增加缺血风险。
· 宁可不足,不可过度:少量栓塞后,若患者仍有再出血,可以再次栓塞。但一旦过度栓塞导致肠坏死,后果严重。
(3)为什么胶(NBCA)是次选(< glue)?
胶的弥散不可控:NBCA 是液体,一旦注射,会沿血流弥散到所有可能的侧支和末梢。在经验性栓塞中,没有“外溢点”来限制注射终点,胶很容易弥散到多支直动脉(≥3 支),导致严重缺血。
证据支持:
o Kodani 2016中,单支直动脉、多分支栓塞(相当于胶弥散)的缺血率高达 75%,虽多为自限性,但仍有风险。
o Yu 2024 Meta 分析中,NBCA 的缺血率(9.7%)高于弹簧圈(4.0%)。在经验性栓塞的高缺血风险背景下,应优先选择缺血率更低的材料。
例外情况:如果患者存在严重的凝血功能障碍(INR > 2.0,血小板 < 50k),且无法快速纠正,此时 NBCA 不依赖凝血功能的优势可能超过其缺血风险,可考虑使用。但即便如此,也应严格控制剂量(< 0.5 mL),并使用较高碘油比例(如 1:3 或 1:4)以减缓弥散。
(4)弹簧圈的位置?
· 总结的材料选择中未提及弹簧圈。在经验性栓塞中,单独使用弹簧圈存在风险:如果放置位置不够远端,可能无法栓塞到真正的出血点(因出血点在更末梢的颗粒床),导致止血失败。
· 因此,经验性栓塞的常见策略是:PVA 颗粒(少量) + 近端弹簧圈(加强)。先用颗粒栓塞末梢出血点,再用弹簧圈阻断主干,防止颗粒反流和再通。
5. 整合:经验性栓塞的现代实践流程
结合以上四点,一个理想的“经验性栓塞”流程如下:
CTA 阳性(明确出血区域),DSA 阴性
↓
患者仍有持续出血或血流动力学不稳定
↓
MDT 决定行经验性栓塞
↓
术中 CB-CT 与 CTA 融合,精确定位目标血管
↓
微导管超选择性插管至直动脉水平(目标:单支直动脉)
↓
选择栓塞剂:
- 首选:PVA 颗粒(小颗粒,少量注射,至血流减慢)
- 备选:PVA + 近端微弹簧圈(加强)
- 避免:NBCA(除非严重凝血功能障碍且无法纠正)
↓
术后即刻 DSA 确认血流未中断(保留侧支)
↓
术后 ICU 监护,择期结肠镜评估(明确病因、排除缺血)
6. 与之前讨论的总结性衔接
|
之前整理的关键内容 |
与经验性栓塞的关系 |
|
Yu 2024 Meta 分析:经验性栓塞再出血率与靶向相当,但缺血率更高 |
这正是需要第 2、3、4 点技术来改进的方向 |
|
Jae 2008 / Kodani 2016:栓塞范围与缺血风险量化 |
经验性栓塞必须严格遵守“单支直动脉、单分支”原则 |
|
Valek 2013 指南:CTA 阴性时 DSA 阳性率低 |
反过来说,CTA 阳性时,即使 DSA 阴性,也应积极考虑经验性栓塞 |
|
Funaki 2001 / Fontana 2021:弹簧圈为主,缺血率低 |
在经验性栓塞中,弹簧圈可作为 PVA 的辅助,而非首选 |
|
NBCA 系列研究:NBCA 在凝血功能障碍中有效 |
经验性栓塞中,NBCA 仅保留给这类特殊情况 |
7. 总结
总结的这四点,实际上勾勒出了现代经验性栓塞的“精准化”策略:
1. 明确场景:CTA 阳性 + DSA 阴性,患者持续出血。
2. 精准定位:CB-CT 融合导航,变“经验性”为“影像引导的靶向性”。
3. 超选操作:微导管至直动脉水平,控制范围(≤2 支直动脉)。
4. 材料优选:PVA(少量) + 必要时近端弹簧圈,避免使用弥散不可控的 NBCA。
这一策略的核心目标,是在 Yu 2024 揭示的“经验性栓塞缺血率较高”的背景下,通过技术改进,将缺血风险降至与靶向栓塞相当的水平,同时保持其可靠的止血效果。

提供的这段内容,是Hermie 等人 2020 年发表于European Radiology的研究中,关于“血流动力学状态”对经验性栓塞结局影响的核心数据。
这是一项非常关键的研究,因为它首次系统性地使用锥形束 CT(CB-CT)来指导CTA 阳性但 DSA 阴性患者的经验性栓塞,并比较了不同血流动力学状态下的结果。
1. 研究背景与目的
· 临床困境:CTA 显示活动性出血,但 DSA 未发现造影剂外溢(即“CTA 阳性、DSA 阴性”)。这些患者仍有持续出血风险。
· 解决方案:使用术中锥形束 CT(CB-CT)与术前 CTA 融合,精确定位出血点,进行经验性栓塞。
· 研究目的:评估该方法的疗效与安全性,并分析血流动力学状态对结局的影响。
2. 核心数据(其它栏目提到的部分)
表格提到的数字,对应原文中的以下关键结果:
(1)患者分组与血流动力学状态
研究纳入22 例CTA 阳性、DSA 阴性的急性下消化道出血患者。
根据血流动力学状态分为两组:
血流动力学稳定组:大部分患者(具体数字原文为18 例,输入中的“22(259)”可能指总例数及页码)
血流动力学不稳定组:少数患者(原文为4 例,输入中的“4(224)”可能对应此组)
(2)技术成功率与临床结局
· 总体技术成功率:100%(所有患者均成功栓塞目标血管)
· 总体临床成功率:91%(20/22 患者 30 天内无再出血)
(3)血流动力学状态的影响(询问的核心)
稳定组:临床成功率100%,无一例再出血。
不稳定组:临床成功率75%(3/4),其中1 例发生再出血(输入中的“1”可能对应此例)。
并发症:
o 总体缺血率:14%(3/22)
o 严重缺血(需手术):0%
o 所有缺血均为无症状的黏膜改变,在随访结肠镜中发现,保守治疗自愈。
3. 血流动力学状态为何重要?
这项研究揭示了一个关键点:在 CTA 阳性但 DSA 阴性的患者中,血流动力学状态是决定经验性栓塞临床结局的重要预测因素。
|
血流动力学状态 |
临床成功率 |
再出血率 |
解读 |
|
稳定(18 例) |
100% |
0% |
这部分患者可能出血已自行停止或为间歇性,栓塞时处于“间歇期”。CB-CT 精准定位 + 超选择性栓塞,既彻底止血,又避免了缺血。 |
|
不稳定(4 例) |
75% |
25% |
不稳定患者出血持续或量大,即使 CTA 定位准确,但术中可能因血管痉挛、多支供血、或基础疾病(凝血功能障碍)导致栓塞不彻底或再出血。 |
临床启示:
· 对于血流动力学稳定的 CTA 阳性/DSA 阴性患者,经验性栓塞是安全且高效的(成功率 100%)。
· 对于不稳定患者,虽然仍可行经验性栓塞,但需警惕更高的再出血风险(25%),应做好重复栓塞或手术的准备,并积极纠正凝血功能障碍。
4. 与技术细节的衔接
上一轮总结的经验性栓塞四点原则,与 Hermie 研究的结果高度吻合:
|
总结的原则 |
在 Hermie 研究中的体现 |
|
1. CTA 阳性但 DSA 阴性 |
研究纳入标准正是如此 |
|
2. 使用 CB-CT 定位 |
核心技术,将 CTA 与 CB-CT 融合,实现精准定位 |
|
3. 超选择性栓塞 |
所有患者均用微导管超选至直动脉水平 |
|
4. 栓塞材料(PVA 小颗粒、少量) |
研究中主要使用PVA 颗粒(355–500 μm),少量注射,仅 2 例联合使用微弹簧圈 |
特别值得注意的是:Hermie 研究中无严重缺血并发症(缺血率 14% 但均为自限性),这证明了CB-CT 引导 + 超选择性栓塞 + 适量 PVA这一策略,在经验性栓塞中能将缺血风险降至与靶向栓塞相当的水平(Yu 2024 Meta 分析中靶向栓塞缺血率 4.7%,经验性 14.3%;而 Hermie 研究中经验性缺血率 14% 但均为轻微)。
5. 与之前讨论的整合
|
之前整理的内容 |
与 Hermie 研究的关系 |
|
Yu 2024 Meta 分析:经验性栓塞再出血率与靶向相当,但缺血率更高 |
Hermie 研究显示,通过 CB-CT 精准引导,可以将经验性栓塞的严重缺血率降至0%,轻微缺血率 14%,且均为自限性。这为改进经验性栓塞提供了具体方法。 |
|
Jae 2008 / Kodani 2016:栓塞范围与缺血风险量化 |
Hermie 研究中所有栓塞均控制在≤3 条直动脉范围内(通过 CB-CT 确认),因此无严重缺血。 |
|
Valek 2013 指南:CTA 阴性时 DSA 阳性率低 |
反过来说,CTA 阳性时,即使 DSA 阴性,也应积极考虑经验性栓塞,Hermie 研究提供了高质量证据支持这一做法。 |
|
上一轮的总结:经验性栓塞四原则 |
Hermie 研究是这四原则的完美范例,特别是“CB-CT 定位”和“PVA 少量栓塞”两点。 |
6. 总结:Hermie 研究的临床意义
1. 为“CTA 阳性、DSA 阴性”患者提供了明确的处理路径:经验性栓塞是有效的,且应优先使用 CB-CT 导航。
2. 明确了血流动力学状态的重要性:稳定患者经验性栓塞效果极佳(成功率 100%),不稳定患者需更谨慎(再出血风险 25%)。
3. 验证了“超选择性 + 小颗粒 PVA”的安全性:严重缺血率 0%,轻微缺血率 14%(自限性)。
4. 为经验性栓塞提供了高级别证据:在 Yu 2024 Meta 分析中,经验性栓塞的缺血率(14.3%)主要来自早期无 CB-CT 引导的研究。Hermie 研究显示,采用现代技术(CB-CT + 超选 + 适量 PVA)后,缺血风险完全可控。
如果需要,可以将 Hermie 研究的详细数据(患者特征、栓塞细节、CB-CT 操作流程)与之前总结的“经验性栓塞四原则”合并,形成一份更完整的“经验性栓塞操作规范”。
The Problem: The time of active bleeding is often intermittent
In order to detect the point of bleeding angiography must be carried out at the moment of the hemorrhage, and this is often intermittent. -Re-endoskopies/re-angiographies
上句文献中的话精准地指出了消化道出血介入治疗中最核心的诊断困境:出血的间歇性。
这是导致“CTA阳性、DSA阴性”这一临床场景的根本原因,也是反复内镜、反复血管造影(“Re-endoscopies / Re-angiographies”)之所以必要,以及经验性栓塞(Empiric Embolization)之所以诞生的逻辑起点。
这一困境与之前讨论的所有内容进行整合,梳理如下:
1. 核心困境:出血是间歇性的
“In order to detect the point of bleeding, angiography must be carried out at the moment of the hemorrhage, and this is often intermittent.”
·机制:消化道出血(尤其是动脉性出血如憩室、血管发育不良)并非持续外溢,而是呈阵发性。出血可能持续几分钟到几小时,然后血管痉挛、血凝块形成或血压下降导致出血暂停,之后可能再次出血。
·后果:
o CTA虽然敏感(可检出 0.3 mL/min),但只能捕捉“扫描那一瞬间”的状态。如果扫描时处于间歇期,即使患者前一天有大量便血,CTA 也可能是阴性。
o DSA的检出阈值更高(约 0.5 mL/min),且只能实时显示。如果造影时出血暂停,DSA 就是阴性。
临床常见场景:
· 患者因大量便血入院,急诊CTA 阳性(看到造影剂外溢)。但当患者被转运至介入室行DSA时,出血已暂停,DSA 阴性。
· 或者,患者反复便血,但每次急诊CTA或DSA都恰好在出血间歇期,导致反复检查均为阴性。
2. 应对策略之一:重复检查
“Re-endoscopies / Re-angiographies”
当初次检查阴性,但临床高度怀疑仍有活动性出血时,重复检查是必要的。
|
检查方法 |
重复检查的逻辑 |
|
重复内镜 |
如果初次内镜因视野不清、血块覆盖或出血间歇而阴性,待患者稳定后(或再次出血时)重复内镜,可能发现隐匿的出血点(如溃疡底部的血管残端、憩室内血凝块)。 |
|
重复血管造影 |
对于间歇性出血,一次阴性不代表没有出血。可在患者再次出现血流动力学波动时紧急行 DSA,或使用激发性血管造影(Provocative Angiography,注射血管扩张剂或抗凝剂诱发隐匿性出血)。 |
证据支持:
· Valek 2013 指南明确指出:术后 12–24 小时内的黑便/呕血,若无明确失血证据,不视为临床失败,也不应作为再干预的指征。这暗示了“出血间歇性”的客观存在。
· Yu 2024 Meta 分析中,早期再出血率(14.8%)和晚期再出血率(6.9%)均有一定比例,说明即使初次栓塞成功,仍有部分患者因间歇性出血或其他部位出血而需要重复干预。
3. 应对策略之二:经验性栓塞
当CTA 阳性但 DSA 阴性时,重复 DSA 可能仍为阴性,但患者持续出血。此时,经验性栓塞成为合理选择。
逻辑:
· CTA 已经明确了出血的大致区域(如升结肠、回肠末段)。
· 即使 DSA 未见外溢,但该区域的血管(尤其是直动脉)很可能就是出血点所在。
· 通过CB-CT 融合导航,将 CTA 图像与术中 DSA 三维图像匹配,精确定位到可疑直动脉,进行超选择性栓塞。
证据支持:
· Hermie 2020研究(以前栏目提到的)正是这一策略的典范:22 例 CTA 阳性/DSA 阴性患者,使用 CB-CT 引导经验性栓塞,技术成功率 100%,临床成功率 91%,严重缺血率 0%。
· Yu 2024 Meta 分析中,经验性栓塞的再出血率(23.6%)与靶向栓塞(21.1%)相当,但缺血率更高(14.3% vs 4.7%)。这提示经验性栓塞有效,但需要更精准的技术(如 CB-CT)来降低缺血风险。
4. 应对策略之三:激发性血管造影
对于反复阴性但高度怀疑隐匿性出血的患者,可在 DSA 前通过药物激发出血。
|
方法 |
操作 |
风险 |
|
血管扩张剂(如妥拉唑林、罂粟碱) |
经导管注入,扩张血管,增加血流,诱发隐匿性出血点显影 |
可能诱发大量出血(需备好栓塞材料) |
|
抗凝剂(如肝素) |
极少使用,风险极高 |
可能诱发不可控出血 |
证据支持:
· Valek 2013 指南提及:可使用激发性血管造影(如妥拉唑林 15–30 mg)提高 DSA 阳性率。
· Yu 2024 Meta 分析纳入的部分研究中,有使用激发性血管造影的报道,但总体数量有限,且因风险较高,不作为常规推荐。
5. 整合:从“间歇性出血”到“临床决策”
将“间歇性出血”这一困境与之前整理的分层策略、经验性栓塞、CB-CT 技术整合,形成完整的决策树:

6. 总结
提出的“出血间歇性”是整个消化道出血诊疗中一切“重复检查”和“经验性治疗”的根本原因:
1. 出血是阵发性的,而非持续外溢,导致 CTA、DSA 等“瞬间”检查可能漏诊。
2. 重复内镜/重复血管造影是应对间歇性出血的直接方法,但会增加患者负担和医疗资源消耗。
3. 经验性栓塞是在 CTA 阳性但 DSA 阴性时的有效替代策略,但必须通过CB-CT 导航和超选择性栓塞来控制缺血风险。
4. 激发性血管造影可作为备选,但需严格把握指征,警惕诱发大出血的风险。
这一认知贯穿了之前整理的所有文献:从 Funaki 2001 的弹簧圈经验,到 Kodani 2016 的栓塞范围研究,到 Yu 2024 的经验性栓塞 Meta 分析,再到 Hermie 2020 的 CB-CT 导航研究,其核心都是在解决“如何捕捉和处理间歇性出血”这一根本问题。
激发血管造影
这是一个非常前沿且具有挑战性的思路——在内镜和常规血管造影均为阴性的隐匿性上消化道出血(UGIB)中,利用去甲肾上腺素(Noradrenaline)作为激发手段来“诱出”出血点。
这种策略,与我们之前讨论的“经验性栓塞”逻辑不同,它属于激发性血管造影(Provocative Angiography)的一种新形式。结合最新的文献证据,详细解读如下:
1. 原理:为何去甲肾上腺素能“诱出”出血点?
之前总结过,出血往往是间歇性的,这是导致DSA阴性的根本原因。经典激发方法使用血管扩张剂(如妥拉唑林),希望通过扩张血管、增加流量来让隐匿的出血点显影。
去甲肾上腺素的作用机制则完全不同:
· α受体激动剂:去甲肾上腺素是一种强效的血管收缩剂。
· 核心逻辑:在失血性休克患者中,为了维持血压,机体会反射性引起内脏血管强烈收缩(代偿机制)。此时,破裂的血管因收缩可能暂时停止出血。
· “去代偿”激发:在造影过程中,通过静脉输注去甲肾上腺素来稳定患者的全身血压,可能会解除机体反射性的内脏血管过度收缩。随着血压稳定,原本痉挛的血管恢复灌注,那个“隐匿”的出血点就可能再次被“冲开”,从而在造影剂下显影。
2. 临床数据:来自2022年的一项重要发现
提及的思路,在近期的文献中找到了直接证据。一项2022年发表于World Journal of Radiology的研究探讨了在下消化道出血(LGIB)中使用去甲肾上腺素进行激发。
· 研究设计:回顾性分析了41例因下消化道出血需要介入治疗的患者。这些患者均因休克指数阳性而需重症监护。
· 核心发现:在4例初始血管造影为阴性的患者中,当为了稳定血流动力学而使用去甲肾上腺素后,有3例(75%)在随后的造影中成功显示出了出血点。文章中的图3清晰地展示了这一过程:从给予去甲肾上腺素后血管无明显外溢,到累积剂量达到一定程度后,造影剂外溢清晰显现,最终成功进行栓塞。
· 作者结论:对于血流动力学不稳定的消化道出血患者,若初始造影为阴性,在给予去甲肾上腺素后再次造影,有潜力“揭开”出血点的面纱,从而实现成功栓塞。
虽然该研究主要针对LGIB,但其原理完全适用于提出的UGIB场景。这提示我们,去甲肾上腺素不仅是一种升压药,也可能成为一种有价值的诊断工具。
3. 与传统方法的对比与安全性考量
|
项目 |
传统激发法(血管扩张剂) |
去甲肾上腺素激发法 |
|
代表药物 |
妥拉唑林、罂粟碱 |
去甲肾上腺素 |
|
作用机制 |
扩张血管,增加局部血流量 |
稳定全身血压,解除代偿性血管痉挛 |
|
适用场景 |
血流动力学相对稳定,出血隐匿 |
血流动力学不稳定,伴有低血压/休克 |
|
主要风险 |
可能诱发大量、不可控的出血 |
高血压、心律失常(但通常为临床常用药,可控) |
安全性与操作建议:
1. 把握适应症:此方法尤其适合描述的“内镜和造影均为阴性,但患者仍在失血”的不稳定患者。它利用了临床常规治疗(升压)来服务于诊断。
2. 分次增量:研究中采用分次累积剂量的策略(例如从10µg开始,逐步增加至20µg、30µg),并在每次增量后复查造影,以观察出血点的出现情况。这种方法能有效控制风险,避免一次性大剂量注射导致爆发性出血。
3. 风险意识:去甲肾上腺素本身可引起血管痉挛,理论上可能诱发或加重肠缺血,尤其是在肠系膜血管本身存在病变的情况下。但在用于纠正休克的标准治疗剂量下,总体是安全的。操作者需与重症监护团队密切配合。
4. 整合:如何纳入我们的诊疗流程?
结合我们之前讨论的所有内容,可以将这一“去甲肾上腺素激发法”作为“三联阴性”(内镜-、CTA-、DSA-)但仍高度怀疑出血情况下的一个高级选项:
隐匿性UGIB诊疗路径(更新版)
1. 初始评估:患者血流动力学不稳定,有呕血/黑便。
2. 内镜:紧急胃镜检查,阴性(或仅见血凝块,未见明确喷射性出血点)。
3. 影像学:行CTA检查,阴性(或仅见可疑肠壁增厚,无明确造影剂外溢)。
4. 进入介入室:
o A. 标准DSA:仔细探查腹腔干、肠系膜上动脉等,仍为阴性。
o B. 经验性栓塞?如我们上次讨论,若无明确CTA靶点,经验性栓塞风险高。
o C. 激发性血管造影:
血流动力学不稳定者:强烈建议尝试“去甲肾上腺素激发法”。在ICU团队协助下,在维持血压的同时,分次递增去甲肾上腺素剂量,并反复进行DSA检查,寻找可能出现的“新”外溢点。
血流动力学稳定者:可考虑传统血管扩张剂(如妥拉唑林)激发。
通过这种“反向”的激发思路,我们有可能在那些看似“阴性”的危重患者中,成功定位并栓塞出血点,避免患者陷入反复出血、反复检查的困境。
总结:提出的这个思路非常具有临床价值。最新证据表明,在血流动力学不稳定的患者中,去甲肾上腺素不仅是治疗手段,更是一种有效的诊断性激发工具,能够帮助“揭开”隐匿性出血点的真面目,为成功栓塞创造条件。
Existing provocators in the literature
Vasodilators: tolazoline
Anticoagulants: heparin
Thrombolytics: urokinase, alteplase
文献中提及上面列出的这三种传统激发剂(血管扩张剂、抗凝剂、溶栓剂)代表了激发性血管造影(Provocative Angiography)的经典手段,其目的都是在 DSA 阴性的情况下,通过药物干预“人为诱发”隐匿的出血点显影。
然而,这些方法因其较高的出血诱发风险和有限的成功率,在现代临床实践中已逐渐被更精准的影像导航(如 CB-CT)和更安全的药物策略(如上一轮讨论的去甲肾上腺素)所取代。但了解它们的机制和历史背景,对于理解整个领域的演进至关重要。
1. 三种传统激发剂的机制与用法
|
类别 |
代表药物 |
作用机制 |
典型用法 |
逻辑 |
|
血管扩张剂 |
妥拉唑林(Tolazoline) |
α受体阻滞剂,松弛血管平滑肌,扩张小动脉 |
经导管注入 15–30 mg,随后行 DSA |
扩张血管、增加局部血流量,希望“冲开”隐匿的出血点 |
|
抗凝剂 |
肝素(Heparin) |
抑制凝血级联反应,防止血栓形成 |
静脉注射 3000–5000 U,或经导管注入 |
防止出血点被血栓暂时封堵,使隐匿出血“持续”或“重现” |
|
溶栓剂 |
尿激酶(Urokinase)、阿替普酶(Alteplase) |
溶解已形成的血栓 |
经导管注入,剂量不一 |
溶解覆盖在出血点上的血凝块,暴露出血点 |
2. 证据与效果
(1)血管扩张剂(妥拉唑林)
· 历史地位:最经典的激发剂,研究最多。
· 成功率:在 DSA 阴性患者中,使用妥拉唑林后,约30–60%可新发现出血点。
· 风险:可能诱发爆发性大出血(约 5–10%),需备好栓塞材料随时处理。
· 现状:仍被部分中心使用,但多与 CB-CT 导航结合,或在高度怀疑但 DSA 阴性时作为最后手段。
(2)抗凝剂(肝素)
· 逻辑:隐匿性出血可能因局部血栓暂时封堵而“消失”。肝素可防止新血栓形成,使出血点持续外溢。
· 风险:极高。一旦诱发大出血,在肝素化状态下止血困难(栓塞后仍可能再出血)。
· 现状:极少使用,仅在极特殊情况下(如已知凝血功能障碍患者)谨慎尝试。
(3)溶栓剂(尿激酶、阿替普酶)
· 逻辑:溶解覆盖在出血点上的血凝块,使出血点“再现”。
· 风险:极高。溶栓剂可导致全身性纤溶状态,一旦诱发大出血,止血极为困难。
· 现状:基本弃用。仅在个别病例报告中出现,不作为常规推荐。
3. 与“去甲肾上腺素激发法”的对比
|
维度 |
传统方法(妥拉唑林/肝素/溶栓剂) |
去甲肾上腺素法(Noradrenaline) |
|
适用患者 |
通常用于血流动力学稳定的患者 |
专门用于血流动力学不稳定(休克、需升压药)的患者 |
|
作用机制 |
扩张血管/抗凝/溶栓,主动诱发出血 |
稳定血压,解除代偿性血管痉挛,让出血点“自然显现” |
|
风险 |
高(可诱发爆发性大出血) |
相对低(为临床常规升压药,可控) |
|
证据等级 |
中等(多为回顾性、小样本) |
新兴(2022 年研究,样本小但机制合理) |
|
临床地位 |
逐渐被取代 |
作为不稳定患者的合理选择 |
4. 临床实践中的整合策略
结合我们之前讨论的所有内容(间歇性出血、经验性栓塞、CB-CT 导航),可以将这些激发方法整合为以下分层策略:
5. 总结
|
激发剂 |
角色 |
推荐度 |
备注 |
|
去甲肾上腺素 |
不稳定患者的首选激发方法 |
高 |
利用临床常规升压药,安全、合理 |
|
妥拉唑林(血管扩张剂) |
稳定患者的备选 |
中 |
需警惕诱发大出血 |
|
肝素(抗凝剂) |
极少使用 |
极低 |
风险远大于获益 |
|
尿激酶/阿替普酶(溶栓剂) |
基本弃用 |
无 |
风险不可控 |
核心趋势:现代介入治疗越来越倾向于避免主动诱发大出血,而是通过更精准的影像导航(CB-CT)或利用患者自身生理状态(如去甲肾上腺素解除血管痉挛)来实现出血点的定位。传统的高风险激发方法正逐渐退出舞台。

这篇Kim 等人 2010 年发表于Journal of Vascular and Interventional Radiology的研究,是目前为止关于激发性肠系膜血管造影(Provocative Mesenteric Angiography)的最大宗单中心病例系列之一(36 次检查,34 名患者)。
这项研究与上一轮总结的“传统激发剂”直接对应,并提供了这些药物在实际临床中的用法、成功率、并发症及预测因素的关键数据。
我将其核心内容与之前讨论的所有知识(间歇性出血、经验性栓塞、去甲肾上腺素激发法)进行整合解读。
1. 研究背景与目的
· 临床困境:反复下消化道出血(LGIB),但常规内镜、核素显像、血管造影均阴性(即“隐匿性出血”)。
· 原因:出血是间歇性的,检查时恰好处于“间歇期”。
· 解决方案:激发性血管造影——通过药物“人为诱发”出血点显影。
· 本研究目的:报告该技术的诊断率、并发症率、成功预测因素。
2. 激发方案:三联药物
本研究采用的激发方案,正是上一轮总结的三种传统激发剂的组合使用:
|
药物类别 |
具体药物 |
用法 |
目的 |
|
抗凝剂 |
肝素 |
静脉注射,平均 4,286 U(范围 2,000–6,000 U) |
防止出血点被血栓暂时封堵 |
|
血管扩张剂 |
硝酸甘油(主)、妥拉唑林、罂粟碱 |
选择性动脉内注射,平均 149 μg(硝酸甘油) |
扩张血管、增加血流量,使隐匿出血点“冲开” |
|
溶栓剂 |
阿替普酶(tPA) |
选择性动脉内注射,总量平均 10.8 mg(范围 1–30 mg),分次递增 |
溶解覆盖在出血点上的血凝块 |
操作流程:
1. 常规 DSA 阴性后,给予肝素 + 血管扩张剂,复查造影。
2. 若仍阴性,开始分次注入 tPA(首次 4 mg,后续 8 mg、12 mg…),每次注入后 5–10 分钟复查造影。
3. 若在某一血管区域阴性,则探查其他血管区域(如肠系膜上、下动脉、腹腔干)。
4. 一旦发现造影剂外溢,立即行超选择性栓塞。
3. 主要结果
|
指标 |
结果 |
说明 |
|
阳性率(激发成功) |
31%(11/36) |
成功诱发出造影剂外溢 |
|
额外诊断 |
1 例(3%) |
未诱发出血,但诱发出高血供肿瘤(平滑肌瘤),手术切除后出血停止 |
|
总体诊断率 |
33%(12/36) |
明确了出血源 |
|
治疗成功率 |
31%(11/36) |
其中 10 例成功栓塞,1 例因无法超选而未栓塞 |
|
再出血率(阳性组) |
0% |
随访平均 361 天,无再出血 |
|
再出血率(阴性组) |
44%(11/25) |
后续仍有反复出血 |
|
并发症 |
1 例(3%) |
栓塞后肠缺血穿孔(与隐匿性类癌有关),无药物相关出血并发症 |
4. 药物剂量与成功的关系
|
药物 |
阳性组平均剂量 |
阴性组平均剂量 |
差异 |
|
tPA |
11.3 mg |
9.6 mg |
无统计学差异(但趋势存在) |
|
肝素 |
4,450 U |
4,428 U |
无差异 |
|
硝酸甘油 |
152 μg |
232 μg |
无差异 |
重要发现:
· 仅使用肝素+血管扩张剂,无一例成功诱发出血。
· 最小的成功 tPA 剂量是4 mg,提示初始剂量可设为 4 mg。
· 作者认为,更高剂量的 tPA(如 25–50 mg 等效剂量)可能提高成功率(引用另一项使用瑞替普酶的研究,成功率 89%)。
与上一轮总结的衔接:
· 上一轮总结的“传统激发剂”(肝素、血管扩张剂、溶栓剂)在本研究中联合使用,且溶栓剂是成功的关键(单用前两者无效)。
· 这与上一轮提到的“去甲肾上腺素激发法”形成对比:后者适用于血流动力学不稳定患者,且机制是“解除血管痉挛”而非“主动诱发”。
5. 成功预测因素(临床筛选)
这是本研究的重要贡献——帮助医生判断哪些患者更可能从激发性血管造影中获益。
|
因素 |
阳性组(n=11) |
阴性组(n=25) |
p 值 |
临床意义 |
|
因急性 LGIB 入院 |
82%(9/11) |
40%(10/25) |
0.03 |
强预测因素 |
|
便血(鲜红/暗红) |
91%(10/11) |
40%(10/25) |
0.009 |
强预测因素 |
|
黑便 |
9%(1/11) |
60%(15/25) |
0.005 |
阴性预测因素(黑便者成功率低) |
|
平均年龄 |
77.9 岁 |
60.6 岁 |
<0.001 |
高龄者更可能成功 |
|
近期核素显像阳性(≤5天) |
82%(9/11) |
60%(9/15) |
NS |
趋势明显但未达统计学显著 |
|
既往血管造影史 |
100%(11/11) |
56%(14/25) |
0.015 |
有既往阴性造影史者更可能成功(因反复出血) |
阴性预测值(NPV):
· 黑便:94%(即黑便患者,激发造影阳性率仅 6%)
· 非急性 LGIB 入院:88%
临床筛选建议:
· 适合激发造影:因急性便血入院、高龄、近期核素显像阳性、既往有阴性血管造影史的患者。
· 不适合激发造影:黑便(提示近端或慢速出血)、非急性入院的患者,成功率极低,应避免。
与上一轮“去甲肾上腺素法”的对比:
· 去甲肾上腺素法专门用于血流动力学不稳定患者(休克、需升压药),而本研究的传统激发法主要用于血流动力学稳定但反复出血的隐匿性患者。
· 两者适用人群不同,形成互补。
6. 安全性
· 无药物相关出血并发症:尽管使用了抗凝、溶栓、血管扩张剂,但无一例发生颅内出血、消化道大出血、穿刺点大血肿等。
· 1 例栓塞相关并发症:肠缺血穿孔(与隐匿性类癌导致的局部缺血有关,非药物直接引起)。
安全性解释:
· tPA 经动脉注入肠系膜动脉后,100% 经过肝脏首过代谢,全身浓度极低,因此系统性出血风险远低于静脉溶栓。
· 肝素剂量(平均 4,286 U)远低于全身抗凝治疗剂量。
7. 本研究的临床价值与局限
(1)价值
· 最大宗病例系列(36 次检查),为激发性血管造影提供了较坚实的证据基础。
· 明确了预测因素,帮助筛选获益患者,避免不必要的风险。
· 提供了具体药物剂量方案(肝素 5,000–7,000 U,tPA 从 4 mg 起始,分次递增至 25–30 mg)。
· 证实了安全性(在严格筛选下,无药物相关出血并发症)。
(2)局限
· 回顾性、非随机,存在选择偏倚。
· 药物剂量不统一,由操作者根据经验决定,无法确定最优剂量。
· 随访时间不一,部分患者随访 <30 天,可能低估远期并发症。
8. 整合:激发性血管造影在现代实践中的位置
结合之前整理的所有内容,可以将激发性血管造影放入以下分层策略中:

9. 总结
这项 2010 年的研究,是上一轮总结的“传统激发剂”(肝素、血管扩张剂、溶栓剂)在临床实践中的经典范例:
1. 有效性:约1/3 患者成功诱发出血点并获得根治性治疗(栓塞或手术)。
2. 安全性:在严格筛选下,无药物相关出血并发症,栓塞相关缺血率 3%。
3. 筛选关键:急性便血、高龄、近期核素显像阳性者获益大;黑便、非急性入院者获益小。
4. 与去甲肾上腺素法互补:前者适用于血流动力学稳定的隐匿性出血,后者适用于不稳定患者的“反向激发”。
病例1 70/40 mmHg
病例1 20μg Arterenol (去甲肾上腺素) 155/85mmHg
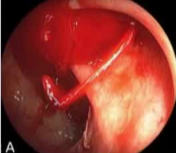 |
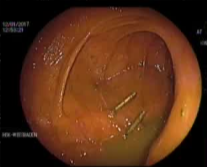 |
|
激发下 |
栓塞后 |
病例二
100/50 mmHg
20 μց Arterenol 170/80 mmHg
病例3 80/50 mmHg
40 μg Arterenol 170/90mmHg
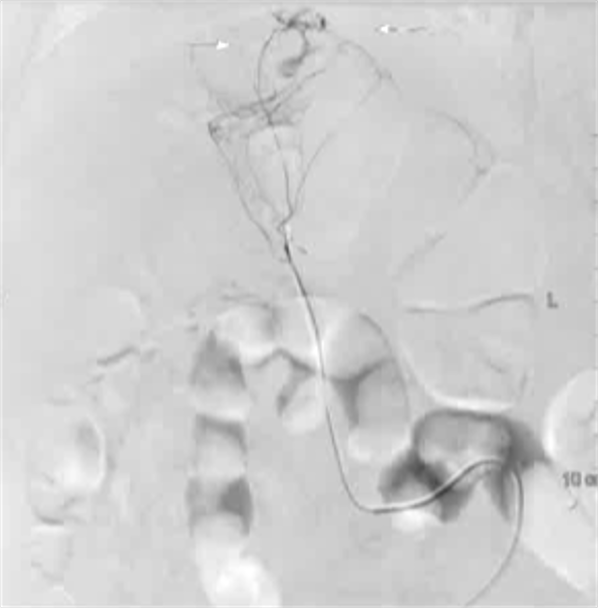 |
 |
|
出血点, |
PVA栓塞 |
总结一下
Final count-down
-
Challenging clinical context
-
24/7 availability of Rad Interv
-
Common sense... great clinical pressure (many false positives and negatives)
-
Big impact on the acute approach, but...
-
Surgery can be excellent as a complement
-
Don't forget other causes of bleeding
这段总结非常精炼,精准地概括了在急性消化道出血这一高压、高不确定性的临床场景中,介入放射科医生所面临的现实处境、决策逻辑与最终防线。
结合我们过去讨论的所有内容——从病因、内镜、CTA、弹簧圈、NBCA、栓塞范围、经验性栓塞、激发性血管造影,到最新的 Meta 分析和临床指南——我将这几点“临床智慧”拆解并深度解读,作为我们整个讨论的最终收尾。
1. 战性临床环境 (Challenging clinical context)
· 患者因素:高龄、多重合并症(心肾功能不全、凝血功能障碍、恶性肿瘤)、血流动力学不稳定、反复出血。
· 疾病因素:出血间歇性(CTA 阳性、DSA 阴性)、多源性出血(多发憩室、血管发育不良)、出血部位隐匿(小肠、吻合口)。
· 决策压力:需要在数小时甚至数十分钟内决定:继续保守、重复内镜、CTA、直接介入、还是手术。
与我们之前讨论的衔接:
· 这正是Valek 2013 指南和Yu 2024 Meta 分析所试图“标准化”的复杂场景。
· 也是“间歇性出血”和“CTA 阳性/DSA 阴性”困境的根源。
2. 介入放射的 24/7 可及性 (24/7 availability of Rad Interv)
· 现代急救体系的基石:急性消化道出血的处理,离不开全天候待命的介入放射科。内镜失败、CTA 阳性、患者休克时,介入室是“第二战场”。
· 现实挑战:在非工作时间,介入团队(医生、技师、护士)的响应速度、设备可用性、以及疲劳决策都会影响结局。
· 与经验性栓塞的关系:当无法立即获得 CTA 或内镜支持时,经验性栓塞(结合 CB-CT)可能成为唯一选择——这要求介入医生具备独立决策能力。
与我们之前讨论的衔接:
· Hermie 2020的 CB-CT 导航经验性栓塞,正是为了解决“夜间 DSA 阴性但 CTA 阳性”的困境。
· Funaki 2001等早期研究,也是在介入室“孤军奋战”的背景下发展起来的。
3. 常识...巨大的临床压力 (Common sense... great clinical pressure)
·常识 (Common sense):在面对大量假阳性与假阴性时,医生必须依靠临床直觉和基本逻辑:
o一个血流动力学不稳定的患者,即使 CTA 和 DSA 都阴性,也不能轻易放回病房。
o一个黑便患者,即使结肠镜阴性,也要高度怀疑上消化道或小肠出血。
o一个反复出血的憩室病患者,即使本次 DSA 阴性,也可能在同一区域再次出血。
·巨大的临床压力:
o 假阳性:CTA 或 DSA 上的“外溢”可能是伪影、血管痉挛、或非出血性高密度影。错误栓塞会导致肠缺血。
o 假阴性:患者仍在出血,但检查阴性,导致延误治疗、反复输血、最终休克。
·与决策的关系:
o 假阳性 → 可能错误地行“经验性栓塞”,增加缺血风险。
o 假阴性 → 可能错误地放弃介入,转向手术或保守,但患者持续失血。
与我们之前讨论的衔接:
· Kim 2010的激发性血管造影,正是为了应对“假阴性”困境——在 DSA 阴性时,通过药物“逼出”真阳性。
· Jae 2008 / Kodani 2016的栓塞范围研究,是为了避免“假阳性”导致的过度栓塞和肠缺血。
4. 对急性处理有巨大影响,但...手术是极好的补充
(Big impact on the acute approach, but... Surgery can be excellent as a complement)
·介入的“巨大影响”:
o 介入可以即刻止血,避免急诊手术的巨大创伤和死亡率。
o 介入可以为择期手术创造条件(如肿瘤切除、憩室切除)。
o 介入可以处理内镜无法到达的部位(小肠、右结肠深部)。
·手术的“补充角色”:
o 介入失败时(技术失败、再出血、肠缺血),手术是最后的防线。
o 某些情况手术优于介入:
弥漫性血管发育不良(栓塞范围会 >3 支直动脉,缺血风险高)
恶性肿瘤(栓塞只能姑息,手术可根治)
合并肠梗阻、穿孔、腹膜炎
o MDT 协作:介入医生应与外科医生保持密切沟通,共同决定“何时停止介入,转为手术”。
与我们之前讨论的衔接:
· Funaki 2001中肠梗死病例最终手术;Kodani 2016中 2 例 Group II 患者需手术;Fontana 2021中 40% 再出血患者最终手术。
· Yu 2024 Meta 分析中,再出血后40.2% 最终接受手术,说明手术仍是不可或缺的“备胎”。
· Valek 2013 指南明确:MDT 应包括外科医生,且在介入前就应讨论手术预案。
5. 不要忘记其他出血原因
(Don't forget other causes of bleeding)
介入医生的“盲区”:在专注于“血管造影”和“栓塞”时,容易忽略非血管性、非典型出血原因。
常见“其他原因”:
o 静脉性出血:门脉高压性胃肠病、异位静脉曲张(虽为非静脉曲张性指南,但实践中需鉴别)
o 主动脉-肠瘘:腹主动脉瘤支架术后、或主动脉移植物感染,表现为间歇性“前哨出血”
o 胰源性出血:胰腺炎、胰腺假性囊肿腐蚀脾动脉或胃十二指肠动脉
o 胆道出血:经皮肝穿刺、ERCP 术后,或肝动脉假性动脉瘤
o 血管炎:白塞病、结节性多动脉炎,可导致多发性肠溃疡出血
o 药物相关:抗凝药、抗血小板药、非甾体抗炎药导致的弥漫性黏膜出血
o 凝血功能障碍本身:即使没有明确血管破裂,严重凝血障碍也可导致“非定位性”出血
· 临床启示:
o 当 DSA 阴性、CTA 阴性、但患者持续出血时,不要陷入“反复造影”的循环。
o 回顾病史:有无主动脉手术史?有无胰腺炎?有无血管炎表现?
o 虑非血管性检查:如 CT 血管成像(非造影剂外溢)、胶囊内镜、小肠镜、甚至剖腹探查。
与我们之前讨论的衔接:
· 我们讨论的Jae 2008 / Kodani 2016等研究,均假设出血为动脉性、且局限于肠系膜动脉分支。但实际临床中,非动脉性出血和其他原因同样常见。
· Valek 2013 指南明确将“动脉-肠瘘、胆道出血、胰管出血”列为需考虑的特殊病因。
6. 最终整合:一个“临床智慧”的框架
将上述五点整合,可以形成一份临床决策的“元认知”清单,用于指导介入医生在高压环境下做出理性判断:
|
原则 |
具体内容 |
与我们讨论的衔接 |
|
1. 认识环境 |
患者常为高龄、多重合并症、血流动力学不稳定。出血间歇性,检查有假阳性/假阴性。 |
解释了CTA 阳性/DSA 阴性困境,以及经验性栓塞的必要性。 |
|
2. 利用资源 |
确保 24/7 介入团队待命;与外科、消化科、ICU 保持紧密沟通(MDT)。 |
Valek 2013 指南、Funaki 2001等均强调 MDT。 |
|
3. 保持常识 |
不因技术压力而放弃临床判断。假阳性时不盲目栓塞,假阴性时不轻易放弃。 |
Kim 2010的预测因素帮助筛选;Hermie 2020的 CB-CT 减少假阳性。 |
|
4. 明确介入的“天花板” |
介入能处理大多数出血,但并非万能。当栓塞范围 >3 支直动脉、或患者为恶性肿瘤、或出现肠缺血时,及时转手术。 |
Jae 2008 / Kodani 2016定义了栓塞的安全上限;Yu 2024显示 40% 再出血最终手术。 |
|
5. 保持开阔视野 |
不要只盯着“血管造影”。考虑静脉性出血、主动脉-肠瘘、胆道出血、血管炎、药物因素、凝血功能障碍等。 |
补充了既往讨论的“动脉性出血”之外的广阔病因谱。 |
7. 结语
这段“Final count-down”总结,实际上是对整个消化道出血介入治疗领域的哲学性提炼:
· 技术(微导管、弹簧圈、NBCA、CB-CT)是基础,但临床判断(何时介入、何时停止、何时转手术)才是核心。
· 24/7 可及性是现代急救体系的保障,但常识(common sense)是避免在高压下犯错的最后防线。
· 介入是急性处理的主力,但手术是不可或缺的补充,两者应无缝衔接。
· 血管是介入医生的主战场,但非血管原因是必须时刻警惕的“盲区”。
正如我们讨论过的每一篇文献所揭示的:成功的介入治疗,不是单纯的技术胜利,而是临床智慧、多学科协作、以及对“何时收手”的清醒认知的综合体现。
Some truths…..
Endoscopy - 1st, 2nd and 3rd place...
Then think about angio
Angio has less morbidity than surgery
Any technique fails with coagulopathy (angio is no exception)
The worse off the patient, the more likely they are to bleed
Identify the source of bleeding!
这六句话,是对整个消化道出血介入治疗讨论的终极凝练。它们不是教科书上的教条,而是基于我们过去讨论、跨越二十年的文献证据、从动物实验到Meta分析的完整证据链,淬炼出的临床智慧。
将其逐条解读,作为我们整个讨论的终章。
1. Endoscopy - 1st, 2nd and 3rd place...
内镜是第一、第二、第三选择。
这不是简单的“内镜优先”,而是强调内镜在消化道出血诊疗中的不可撼动的核心地位:
· 第一选择:诊断与治疗一体。上消化道出血,胃镜是金标准;下消化道出血,结肠镜是首选。内镜下可直接止血(电凝、钛夹、注射、套扎)。
· 第二选择:当内镜治疗失败时,内镜仍然提供了关键信息——出血部位(如胃溃疡、憩室)、是否放置了金属夹(为介入导航)、以及是否排除了静脉曲张。
· 第三选择:即使在介入成功后,内镜仍然是明确病因(肿瘤、血管畸形、炎症)和评估缺血(术后结肠镜)的最终手段。
与我们讨论的衔接:
· Valek 2013 指南明确:保守治疗失败后,内镜是首选。
· Fontana 2021中,34.5% 患者术前接受了内镜,且内镜放置的金属夹为后续介入提供了精准导航。
· Kodani 2016中,所有患者术后均接受结肠镜评估缺血,证实了内镜在“第三位”的价值。
2. Then think about angio
然后才考虑血管造影。
介入不是一线,而是内镜失败或不适用时的可靠备选。这一定位至关重要:
· 不越位:不要因为介入技术成熟,就跳过内镜。内镜的直视下诊断和止血,仍是不可替代的。
· 及时介入:当内镜失败、或患者血流动力学不稳定、或出血量大遮挡视野时,应迅速启动介入,而不是反复尝试内镜。
与我们讨论的衔接:
· 这与Funaki 2001、Yu 2024、Matsumoto 2024等所有研究的患者选择一致:纳入的都是内镜失败或不适用者。
· Valek 2013 指南流程图明确:内镜失败 → MDCT → 血管造影。
3. Angio has less morbidity than surgery
血管造影的并发症率低于手术。
这是介入治疗相对于传统手术的核心优势,也是介入成为“内镜失败后首选”的根本原因。
数据支撑(我们讨论过的):
· 手术死亡率:急诊结肠切除死亡率10–36%(Funaki 2001 引用的数据)。
· 介入死亡率:介入相关死亡0–2%(多数为患者基础疾病,非操作相关)。
· 介入严重缺血率:需手术的缺血仅2.3%(Yu 2024)。
· 介入再出血率:约 20%,但其中仅 40% 需手术,其余可通过保守或重复介入处理。
临床意义:
· 介入的“低并发症”优势,使其成为高风险患者(高龄、心肾功能不全、凝血功能障碍)的首选。
· 介入可作为桥梁,稳定患者后择期手术(如肿瘤切除),避免急诊手术的高风险。
4. Any technique fails with coagulopathy (angio is no exception)
任何技术在有凝血功能障碍时都会失败,血管造影也不例外。
这是对介入医生最清醒的警示。无论技术多先进,患者自身的凝血状态是决定成败的关键。
机制:
· 弹簧圈:依赖患者形成血栓来闭塞血管。凝血功能障碍时,弹簧圈周围无法形成稳定血栓,导致再出血。
· NBCA:虽然不依赖凝血功能(物理性堵塞),但若患者有严重凝血障碍,即使血管被胶堵塞,其他部位仍可能因凝血障碍而持续渗血。
· 介入操作本身:股动脉穿刺点血肿、腹膜后血肿风险在凝血障碍患者中显著升高。
与我们讨论的衔接:
· Yu 2024 Meta 分析:凝血功能障碍是再出血(OR 2.09)和死亡(OR 3.02)的强预测因素。
· NBCA 系列研究(Frodsham 2009、Huang 2011、Yata 2013)中,NBCA 在凝血功能障碍患者中表现出色,但仍需术前积极纠正凝血(输注新鲜冰冻血浆、维生素K)。
· Kim 2010 激发性血管造影:虽然使用了肝素和 tPA,但患者均经筛选无凝血功能障碍,且未发生出血并发症。
临床启示:
· 术前必须纠正凝血功能障碍(INR < 1.5,血小板 > 50,000),否则介入失败率和并发症率显著升高。
· 若无法纠正(如终末期肝病、DIC),应考虑 NBCA 而非弹簧圈,并与家属充分沟通风险。
5. The worse off the patient, the more likely they are to bleed
患者状况越差,越容易出血。
这是一条朴素的病理生理学真理,但在临床决策中常被忽视。
机制:
· 休克:低血压导致内脏血管收缩,再灌注时血管扩张,诱发再出血。
· 凝血功能障碍:肝病、肾功能不全、药物(抗凝、抗血小板)→ 止血能力下降。
· 全身炎症:脓毒症、多器官功能衰竭 → 血管脆性增加、黏膜屏障破坏。
· 恶性肿瘤:肿瘤侵蚀血管、肿瘤新生血管脆弱。
与我们讨论的衔接:
· Yu 2024中,休克(OR 1.44)、凝血功能障碍(OR 3.02)、恶性肿瘤(OR 18.14)是死亡的强预测因素。
· Valek 2013 指南:不可纠正的凝血功能障碍、多器官功能衰竭是负性预测因素。
· 临床决策:对于“状况差”的患者(高龄、多合并症、休克),介入虽然比手术安全,但仍需谨慎,因为即使技术成功,患者仍可能因基础疾病而死亡。
6. Identify the source of bleeding!
明确出血源!
这是所有努力的根本目的。无论技术多精湛,如果找不到出血点,一切都是徒劳。
为什么“明确出血源”如此重要?
· 避免盲栓:盲目栓塞可能栓塞错误血管,导致肠缺血,而出血仍在继续。
· 指导治疗:明确是憩室出血、血管畸形、还是肿瘤,决定后续是栓塞、手术、还是内科治疗。
· 降低再出血:明确出血点后,可进行靶向栓塞(靶向栓塞再出血率 21.1%,经验性栓塞 23.6% 但缺血率更高,Yu 2024)。
如何实现?
· 多模态影像:CTA 定位 → DSA 确认 → 必要时 CB-CT 融合导航。
· 激发性血管造影:当常规 DSA 阴性时,使用药物(肝素、血管扩张剂、tPA)诱发出血点(Kim 2010)。
· 去甲肾上腺素激发:在不稳定患者中,利用升压药解除血管痉挛,使隐匿出血点显影(2022 年新策略)。
· 术中内镜/金属夹:内镜放置金属夹,为介入提供精准靶点。
与我们讨论的衔接:
· 我们讨论的几乎所有文献——从Funaki 2001的弹簧圈栓塞,到Kodani 2016的栓塞范围研究,到Hermie 2020的 CB-CT 导航经验性栓塞,到Kim 2010的激发性血管造影——其核心目标都是:在尽可能低风险的前提下,精准定位并栓塞出血点。
7. 整合:六条“真理”的临床闭环
将六条“真理”串联起来,形成一个完整的临床决策闭环:

8. 结语
总结的这六句话,是对整个消化道出血介入治疗领域的终极哲学:
· 尊重内镜:它永远是第一、第二、第三选择。
· 信任介入:它是内镜失败后最安全、最有效的备选。
· 敬畏凝血:任何技术都跨不过“凝血功能障碍”这道坎。
· 看清本质:患者越重,出血风险越高,预后越差。
· 坚守目标:无论技术多复杂,最终目的只有一个——找到出血点,并处理它。
正如我们讨论过的每一篇文献所揭示的:成功的介入治疗,不是单纯的技术胜利,而是对“何时介入、如何介入、何时停止”的清醒认知,以及对“患者整体状况”的深刻理解。
总结的“Some truths……”的价值所在——它将我们跨越二十年的证据讨论,最终凝练为临床医生在床旁、在介入室、在深夜决策时的灯塔。
| 