ѧϰĿ��
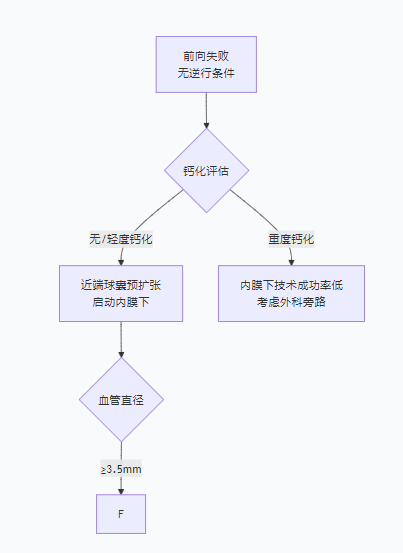
�������ս
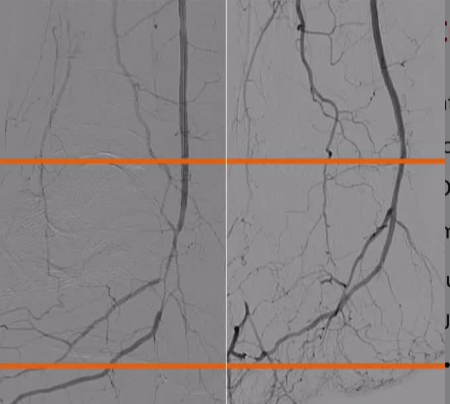
����CLTI (Chronic Limb-Threatening Ischemia) ����Щ����dz������Ұ��ж��ֲ���֢�Ļ��ߡ� ����Ѫ��ǰ��ѡ�������·��Diamantopoulo A 2014���Բ���·
������˿�����ܣ����ҵȽϳ�Ѫ������е�DZ���� ͬ����·
ֱ����Բ���Ĵ�������
ʹ�� 6 Fr ���� 7 Fr ���� → ����ѡ������е�����ͣ� �㶯����·....
ͨ��ϥ���¶�����խ
����BTKʼ���ڹ�ǻ����ʼ�մ�˳����·
���ص���խ������Ҫ���н��˴�����
���������Լ���Ħ�� ֻʹ��Сֱ�����ң��� 2 mm ���ң�
�ػص�Ѫ�ܻ����Ǹ����� ʹ�þ�������Ť�����ܵĵ�˿�����֣���
���ֵ�˿��
�������ÿ�Ť���ܣ����Ť�أ��������Լ�˵�֧���Ե�˿
�ۺ�����ˮͿ�� ����Ħ���� �͵�˿��˸��أ�Tip load�� �������õ�֧�֣����뵼˿��“ͷ���غ� (Tip Load)”��ָ�������Ƶ�˿��������һ������ʱ�����������������ͨ���Կ� (gf) Ϊ��λ�����Ǻ�����˿ͷ��Ӳ�ȵĹؼ�ָ�ꡣҽԴ�Ա����Լв㣨IOCD�� �У�����˿����ԽѰ�������ܼ������˳����ǻͨ���Ŀ��ܡ���ͷ���غ� (Low Tip Load)”�ĵ�˿����ͷ�˼�Ϊ������ͨ���Կ�Ϊ��λ������ͷ���غɷֱ��� 0.8g 1:1 ת����Ӧ ��϶���Ƶ�խ��·
“�� vs. ��”������ͷ�˵IJ���ѡ��
���ٴ�ʵ���У�“��”��“��”��������ԵIJ���ѡ�����ķ���ɲο��±���

|
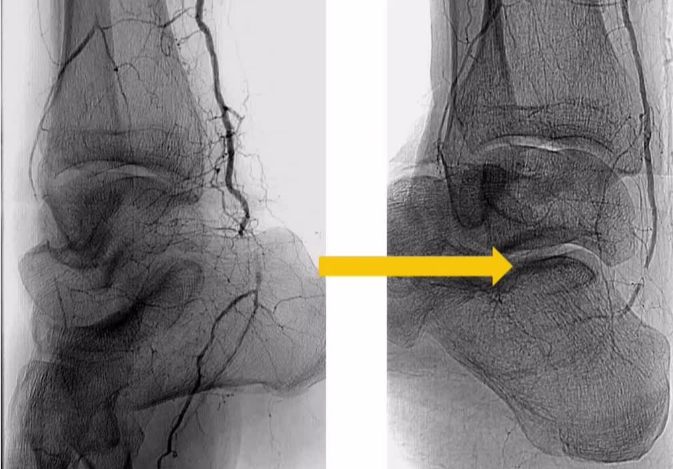 |
| �ڷ�/�ⷭ��������˿“����”�����ද�����㱳������֧ |
·
ʵ����
����˿���㱳��������������֧ʱ�����Ὣ���ڷ���ֺ����Ѫ�ܽǶȿ��Ա仯20-30°����Ͳ����Ѷȡ�|
�������Эͬ ��ʵս������������ |
���� | Ŀ�� |
| �� | �䵼˿ͷ��1��2mm������ | ����̽�飬���ٴ��� |
| �ӽ����� | �ɽ�����ǰ�������벡��1-2cm�� | �ṩ����+����֧�� |
| ͨ���ֲ�/��� | ������ת/���͵�˿��ͬʱ��̬���㲿�Ƕ� | ��Ѫ��“��·”����˿ |
| ������ǻ | ���ܸ���ȥ��ȷ��ǻ��λ�� | Ϊ����/DCB�������� |
�������������ۣ�����ʵʵ���ڿ�����DSA����̨������Ӧ�õļ��ɡ���������ٴ������������ǿ���ij���㲿������֧���������������“��һ�½�”——�����Ȼ�ʮ����˿�����á�
ϥ���¶�����������ͨ������
���������Ĺ�ϥ���¶�����խ�����ͨ��������������������ϥ���¶������������ͨ��������
�����Ƿdz����塢ʵ�õIJ������̡�����ȫ��һ�߽���ҽ����ʵս�ʼǣ�ÿһ�䶼ֵ�������⡣��Ŀ���Ż����Լ������⣬���г���Ҫ����һ���ٴ�ע�ͺ�����˼����Ҳ��֪�����Ƿ�ȷ��ÿ�������Լ����ٴ�ʵ���ж������Լ��ļ����ͼ������飬����Ҳ��һ����
���̺��ģ��������
1 ️“Always first try to stay intraluminal”
�������Ĥ�£�subintimal����ͨ��CTO��“��ѡ����”������ѡ����Ϊ��· ��Ĥ�»�������֧���ӳ�����ʱ�䡢��������խ���ա�
· ������BTK����֧����ƻ���ò���ʧ��
· ���滹ǿ����“С�ĵ�˿�Ѵ���prolapse��”��“�Ŵ�magnification essential��”������Ϊ�˱�ס��ǻ·�ߡ�
2 ️ “4 Fr Vertebral catheter + support of smaller catheter (2.6Fr Cxi) → Tri-axial system”
�dz������ͬ���ǿ֧���ṹ��· 4F����������ͨ��������䣬��Headhunter��VTK shape������Ϊ��㣬�ṩ����ķ����Ժͳ���֧�š�
· 2.6F Cxi������������CXI֧�ŵ��ܣ�Cook��ͬ���Ʒ�����ڲ��Ӳ��֧�ŵ��ܣ��ܷ�ֹ��˿�ڽ��˴��ۡ�
· 0.014"��˿�����ڲ㡣
· ��һ�����˳�й��N��ɽBTK�У��ܼ������“��˿������”������ʧ�ȡ�
2.6F Cxi���ھ��պü���0.014"��˿����������0.018"����ǡ�������“Avoid 0.018" wires”�IJ���һ�¡�
3 ️ “I try to only use 0.014" wires”
����BTK/�㲿��������ĺ���ԭ��֮һ��· 0.018"ϵͳ��Ӳ��Ť����Ӧ���ˮͿ��̡���������Զ��ϸСѪ�ܡ�
· 0.014"��˿����ִ����ܣ���ȫ������ɾ������ϥ�²��䣬�������������
���ⳡ����ֻ�����������Ҫ0.018"�����罻����CTO��Ҫ��2.5mm�������ң������ƺ��б�İ취�ƹ���
4 ️ “First choice hydrophilic wire with 1:1 torque response”
���ʹ�������Asahi Sion Black / Sion / Fielder XT������֮ǰ�Ĺ��ĵ�Tip��˿����· ��ˮͿ�� + �ۺ��ﻤ�� → ��Ħ�������������á�
· 1:1Ť�� → ��СѪ���ھ�ת������“��”��
· ��Tip Load → �ʺ���ĤѰ�������Ǵ��̡�
5 ️“Try to avoid 0.018" wires”
�ٴ�ǿ����0.018"��˿����V-18����Ȼ֧�źã�����· ͷ����Զۣ����������
· ���ضȸƻ���CTO����������ǻ�����Ի�ͷ��
· ����BTKֱ��2-3mm��Ѫ�ܣ�0.018"��Ӳ�ȹ��ߡ�
6 ️ “No need for CTO wires at this stage”
�dz��о�����жϣ����ڲ���Ҫ“������”��· CTOר�õ�˿����Miracleϵ�С�Gaia��Conquest��ͷ��Ӳ��������ǿ�����״���Ѫ����������Դ��ס�
· ������ˮ����˿“����”��ʵ�ڹ���ȥ���������ܶ��CTO�IJ�����ʵ������
7 ️ “Be careful for the wire not to prolapse too much”
��˿�Ѵ���prolapse���dz���ʧ��ģʽ��· �ڼ�Ӳ�Ľ�����άñ��ƻ�������˿��ǰ�������������������Ķ����ڴ�Ȧ��
· ���ĶԲߣ�4F�������� + Cxi�����γɵ�����ϵͳ���ܼ�����ٵ�˿���˵����ɳ��ȣ������Ѵ���
8 ️ “Magnification essential”
�ܶ��˺��ԣ�������ؼ���· ϥ��Ѫ����Ӱ��Ҫ����2���Ŵ����ܿ��嵼˿�����ܱڵĹ�ϵ��
· �������жϵ�˿�Ƿ�����ǻ���Ƿ��ѽ����ǻ���Ƿ��ڸƻ��߿��ϡ�
· �Ŵ� → äĿ���� → ����в㡣
�������� & �������ڵļ���
���ײ��Էdz����ԡ���ȫ����Ч����ȫ����“less is more”���ִ�������ѧ��
�����/���伸���Ƕȣ�
| ���Ĺ۵� | �ҵ�˼��/���ܵ���չ���� |
| ֻ��0.014"��˿ | ������Ҫֲ��2.5mm����֧�ܻ�DCBʱ��ijЩ��е������ϵͳ�ھ�Ҫ��0.018"������ֱ�Ӳ���������е������ͨ�����������������ֱ�Ӷ�ס�������ݣ� |
| Tri-axialϵͳ | 4F���������⾶Լ1.33mm����BTK˳��ʱ�������dz����������ϸ��<4mm�����������Ѫ�ܾ��η��գ��Ƿ���ijЩ����¸�Ϊ5F��ֱ��֧�����ܣ� |
| “No need for CTO wires” | ��ȫͬ�⡣������ڳ�������˿20���Ӻ���Ȼ��ͨ��������Ӱ��ȷ����������άñ����������·����ʲô���Ȼ��е�Ӳ�ȣ���Gaia 2������ֱ�Ӹ���Ĥ�£� |
| �Ŵ� | ���Ƿ�ʹ��·ͼ��roadmap��������ϷŴ��㲿Ѫ�ܵ�ʵʱ·ͼ�Է�ֹ���dz����á� |
���ϲ��ԣ���“��ס��ǻ”Ϊ�ռ�Ŀ�꣬�������Ĺ��ߡ���ǿ��ͬ��֧�š����������Ӿ��Ŵ�BTK/CTO������һ�ξ�ϸ��Ѱ·���Ǵֱ��Ĵ�ǽ��
������֮ǰ�ܽ��“��ͷ���غ� + �ɽ����� + �㲿����ѧ”��ȫһ����У������������˾������е�ͺź͵���������dz�����
�������ʱ�䣬�ܷ���չ��˵˵����ϵͳ��˳��BTK�еľ���װ��˳�������磺�ȷ�4F������SFA�ж� → �ٽ�Cxi��������� → ������˿��������������ҽ�����ֱ�ۡ�
 |
 |
| �ֺ������� | ��˿�ֽ��������� |
 |
 |
 |
| �����Ѵ���early prolapse��ָ��˿ͷ�����ܵ���С����ʱ�ͻ������γ�һ��С����loop�� |
 |
 |
���������dz�ʵս�Ĵ�Խ�������䣨Crossing Occlusions�� ���������档��ξ۽����ǣ�����ˮ����˿��ͨ��ʱ����ΰ�ȫ�����������ߴ����ĵ�˿��ͬʱ����ס�
���������������һЩ�ٴ�ϸ�ںͷ��տ���Ҫ�㡣
���IJ��Խ��
1. ️ “Consider swapping for a wire that could penetrate better” → ��ʱ������
��֮ǰ�ᵽ��“First choice hydrophilic wire (Sion Black��) ���Ժ�����ͨ��”������£���Ҫ��������������ָ��������
·
��˿ͷ�˷��������ǻ����Ĥ�£���������ǻ��
· ��˿�ڸƻ�/��άñ��“����”��ǰ������ʹ������֧�ţ���
· ��Ӱ��IVUS��ʾ����������άñ�����ظƻ������
· ���Գ���15-20���������Խ�չ��
�ؼ�ԭ������������“�һ�”�������в��Ե�����ͷ���غɺʹ�����ͬʱ���ֶ���ǻ�ĸ�֪��
2. ️“Please be careful to avoid extravasation” — ����֮��
����������CTOӲ��˿ʱ���ķ��ա�Ϊʲô�������磨��Ѫ�ܴ��ף���
· Ӳ��˿����Astato XS 40����ͷ���غɿɴ�6-12g����������һ��������Ĥ�»�Ѫ�ܱڣ�����û��“����ɲ��”��������
· ������BTK����Ѫ�ܱڱ�����Ĥ����������ܵ����㲿��С�ȹǽ�Ĥ���ۺ�����
�Բ�˼·��
· ����ǰ��������“��ס”������ˣ����ٵ�˿��¶���ȡ�
· ���߷Ŵ�����˫�Ƕ���Ӱ�²�������ʱȷ�ϵ�˿���λ�á�
· �����ȷ���Ƿ�����ǻ�����ɻس����ԣ���Ҫǿ�����͡�
3 ️. “Wires with early prolapse tips helpful to create a loop”
���Ǻܾ���ļ��ɡ������Ѵ���early prolapse��ָ��˿ͷ�����ܵ���С����ʱ�ͻ������γ�һ��С����loop���������Ե�˿��ASAHI Halberd��V14��Advantage 14��
�γɻ���Ŀ����
· ����Ĥ��ͨ���У��Ի�״�ṹ���Է�����֯�������Ǽ��̣��Ӷ����ʹ�������
· ����ֱ���ɿأ���������“����”��Ĥ�¿ռ䣬���ں������ܸ�����
· ���ּ�����Ϊ“loop technique”��“subintimal looping”���Ǵ�������CTO����Ч������
�ٴ�����������˿�Ѿ�������Ĥ�µ�ϣ�����½�����ǻʱ��������“����”��˿��ֱ����Ӳ��˿����ȫ��
4 ️.�оٵĵ�˿�������ص�
| ��� | ������˿ | ͷ���ص� | ��Ҫ��; |
| �����Ѵ�/���γ� | ASAHI Halberd | ͷ�˽϶̡��е�Ӳ�ȣ�~4g�����������ɻ� | ��Ĥ��Ѱ�������Է��� |
| V14 (ControlWire™) | �ɵ�Ӳ�ȣ�3g/6g���ֹ�� | ֧��+�ɿػ��γ� | |
| Advantage 14 | ��ˮͿ��+�����о��ͷ��Ӳ��Լ3g | ͨ���ͣ����γɻ� | |
| CTOר�ã����ͣ� | ASAHI Astato XS 20 | ͷ���غ�~20g����������Ӳ | ����������άñ |
| ASAHI Astato XS 40 | ͷ���غ�~40g������Ӳ�ȣ� | ���˸ƻ�/����CTO | |
| Victory (ASAHI) | ͷ���غ�~10-12g������� | �е�Ӳ�ȡ������� | |
| APPROACH (ASAHI) | ͷ���غ�~3-5g����ˮͿ�� | ���ڹ�����˿��CTO֮�� |
��Ҫ������Astato XS 20/40 �Ƿdz�“����”����������BTK����ʹ���輫�Ƚ�����ͨ��ֻ���������N�����Ĵ�Ѫ����ʹ�ã�ϥ�º�����Ҫ����12g�ĵ�˿��
ʵս��������������˿��CTO��˿������·��
| ���� | ��˿���� | ͷ���غ� | ����Ҫ�� |
| L1 | ��ˮ�ۺ��ﵼ˿ (Sion Black, Fielder XT) | ~0.8-1.5g | ����֧�ţ�Ѱ���� |
| L2 | �е�Ӳ����ˮ��˿ (V14, Advantage 14, Halberd) | ~3-6g | �ɳ���С���γɣ���Ĥ��̽�� |
| L3 | ������CTO��˿ (Victory, Approach, Astato 10) | ~8-12g | �̴�������˫�Ƕ�ȷ��λ�� |
| L4 | ����CTO��˿ (Astato 20/40) | ≥20g | �����ڹ��N��Ѫ�ܣ�BTK���� |
���IJ�����Ȼ��ѭ����һ����ʽ�������ر�ǿ�����������������Ѵ��γɻ���˵��������������“���Է���”����“����”��ͨ�����䡣
��֮ǰ���Ե��ν�
| ֮ǰ�Ĺ۵� | ���ڵIJ��� | һ���Է��� |
| “No need for CTO wires at this stage” | “Consider swapping for better penetration” | ��ì�ܣ�������Ӳ�����������������ֽε� |
| “Avoid 0.018" wires” | �оٵĵ�˿����0.014" | ����һ�£�ʼ��ʹ��0.014"ϵͳ |
| “Magnification essential” | “Be careful to avoid extravasation” | �Ŵ��Ƿ�ֹ������ǰ�ᣬ������ |
| “Tri-axial system for support” | ����Ӳ��˿ʱ����Ҫͬ��֧�� | Ӳ��˿�������Ѵ�������ϵͳ�����Ѵ� |
һ��ֵ�����۵�ϸ�ڣ�������ж�“��������”��
���ٴ��ϣ��ܶ�ҽ���������ִ���
1. ����������������˿����2����û��ȥ�ͻ��ص�˿��������ס�
2. ����������������˿��������40���ӣ����ߺ�����ʱ�䶼�ܳ���
��������û��һ���������Ľڵ������磺
· ��˿ͷ���α䳬��3�Σ�
· ������Ӱ��ʾԶ����ǻ��Ӱ����˿�����룿
· ���Ըо���“����”�У��������߿飩��
����������һ�����ԡ���ȫ���ֽε�CTO��˿����������
���õ�Tip����ˮ��˿Ѱ�� → �������׳ɻ����е�Ӳ�ȵ�˿��Halberd/V14��������Ĥ�¶��Է��� → ������ȷ��Ҫ�����ܸƻ�ʱ��ʹ������CTO��˿��Astato����ͬʱ��“��������”Ϊ���ԭ���Ը߷Ŵ��ʺ�˫�Ƕ���Ӱȫ�̻�����
����֮ǰ��“��ͷ���غ� + �ɽ����� + �㲿����ѧ”�������νӣ��γ��˴�ͨ��̽�� → ��Ĥ�»��γ� → ӲĤ���������������⡣
ǰ����������ϥ�¶��������Բ����������ʹ�õͺ��ص�˿ͷ��ͨ��ʧ��ʱ������“���”Ӳ�ĵ�˿���������۵�˿������
��������“������Deescalate��”���ԣ��Ƿdz�����CTO����˼ά��Ҳ�Ǻܶ��о���Ľ���ҽ��“�ض�����”�ĺ��ļ��ɡ��������������ν���֮ǰ�ᵽ��“������Ӳ”��“��������”��
����Ŀ����“����”��Ҫ�㣬����ٴ�ʵ�ʣ���һ����Ƚ�������죺
---
���ĸ��ΪʲôҪ“���ڽ���”��
ͨ����˼ά��“�������Ѿ�����”������Ӳ�ĵ�˿������“����”�IJ����ǣ��ڳ�����Ӳ��˿����Astato��Victory�����ж̴̳��̺�һ��ͨ�����Ӳ����άñ�������������������������õĵ�˿��
�������������ɣ�
| ���� | ���� |
| ��ȫ�� | Ӳ��˿����ǻ�ڳ��������ߣ����״�����֧��Զ�ˣ���������Դ��ס�����˿��ʹ�����ǻҲ����“ɲ��”�� |
| Ѱ������ | Ӳ��˿�����������Ҫ��“��”������˿����Sion��Fielder XT����1:1Ť�أ���“��֪”��ѡ���Խ�����ǻ���֧�� |
| �����ǻ���� | Ӳ��˿ǿ���ƽ���������Ĥ�¿ռ䣬�ƻ���֧������˿�����״Ӽ�ǻ“�ҵ�����”���½�����ǻ�� |
һ�仰�ܽӲ��˿����“����”������˿����“��·”��
---
����Ҫ�����
1. “Deescalate again early for wire with good feedback and 1:1 torque response”
�����“again”�ܹؼ���˵������һ�����ظ���ѭ����
· �� ��˿→ Ӳ��˿��ͻ����άñ�� → ������������˿������ǻ��ǰ���� → ������һ���ƻ��ڶ� → ������Ӳ�����ݴ��̣� → �ٽ����� …
���ʹ�����˿����
· ����Ŀ�꣺Asahi Sion��Fielder XT��Sion Black����Tip����ˮ��1:1Ť�أ�
· ����������Astato XS 10/20��Victory��Gaia 3���ߺ���Tip�������ͣ�
�ٴ�������
· ����Ҫ������ϵͳ��ֻ��Ҫ�������ڿ��ٽ�����˿��
· ������˿�����������“ϸ��”�����ܸо���������“������Ĥ”����“���ڸƻ���”��
2.“Support with micro catheter very useful”
�����ڽ��������е��������������أ�
| ���� | ˵�� |
| ���ٽ���ƽ̨ | ����Ҫ���½���ͨ·��ֱ��ͨ�����ܽ�����˿��ʡʱ�Ұ�ȫ�� |
| ����Ѫ�� | Ӳ��˿����ʱ����������ԭ������ֹѪ�����ݻ�ʧͨ·�� |
| ��ǿ֧�� | ����˿����֧�Ų�������ܶ�ס���ˣ����������Ը���Ч�ش�����ˡ� |
�����������������֮ǰ������ϵͳһ�£���
· ��㣺4F��������
· �в㣺2.6F Cxi ֧�ŵ���
· �ڲ㣺0.014" ��˿
����ʱ���γ�Ӳ��˿ → ͨ��Cxi��������˿ → ͷ��¶��1-2mm → ����ǰ����
3. “Different projections essential”
������ֹ���ͼ�ǻ�������Ӿ����ϣ�������ʹ��Ӳ��˿�ڼ�ͽ�����
Ϊʲô��Ҫ����Ƕȣ�
· ��ƽ����Ӱ��������Ѫ�ܿ�������һ��ֱ�ߣ�Ӳ��˿�����Ѿ�����Ѫ�ܱڵ�����������“ǻ��”��
· ˫�Ƕȣ���AP + ��λ������λ + бλ30°�����жϵ�˿��˵���άλ�á�
ʵ��Ҫ�㣺
· ������Ӳ��˿֮ǰ������˫�Ƕ���Ӱ����ȷ��������κ���Σ�յķ�֧��λ��· �ڴ̴���άñ������������һ�Ƕ�ȷ�ϵ�˿û�д�����
· ����Ϊ����˿������˫�Ƕȵ�����
---
��������-����ѭ������ͼ��CTA = CTO��
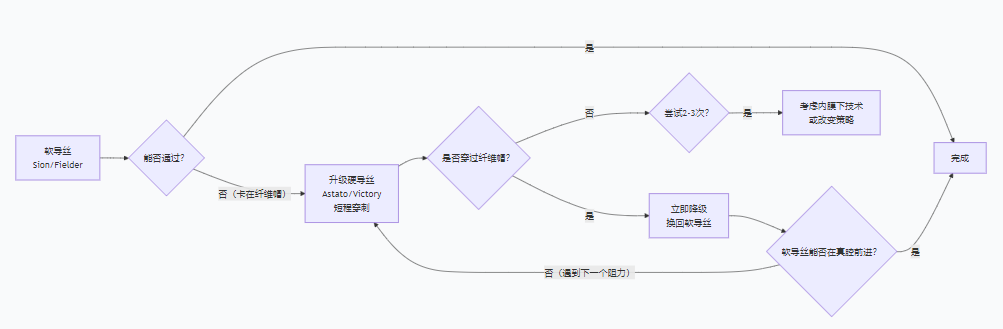
---
���ײ��Եĺ�Ӧ
| ��֮ǰ�Ĺ۵� | ���������е����� |
| “Avoid extravasation” | �����Ƿ�ֹӲ��˿����Ѫ�ܵ���ֱ�ӷ��� |
| “Magnification essential” | ��ͬͶӰ + �Ŵ� = �ж��Ƿ�ý������Ӿ����� |
| “No need for CTO wires at this stage” | ������ص�“��CTO��˿”�İ�ȫ״̬ |
| “1:1 torque response” | ������Ŀ�굼˿����߱�������� |
| “Support with micro catheter” | �����IJ������� |
---
ֵ�����۵�ϸ��
1. ������ʱ��������ô�ж�“�ý�����”����Ӳ��˿�ոմ�����άñ��˲�䣨ͨ���ָ�“��ո�”�жϣ������DZ�������˫�Ƕ���Ӱȷ��λ�ã�
2. �������ǰ����������������˿����һ�����������ǰ����Զ������ʼ�ձ������ܾ����˺ܽ���<5mm���Է�ֹ�ٴ��Ѵ���
3. ��IVUS��������ڸ���CTO�У��������Ƿ���ҪIVUSȷ�ϵ�˿����ǻ��
“���ڽ���”���ԣ���CTO��������ȫ����Ч�ʵ����ƽ�������������“һζ����”��˼ά��ʽ����Ӳ��˿��λΪ“�̳����Ϲ���”������ȫ������Ȩ�������������á�����ȫ������˿��
��һ������BTK��СѪ�������䱦��——��Ϊ����Щ����һ�δ��Ϳ��ܻٵ�����֫�塣
���ļ�����Ҫ����
�� ���ٽ�������ƽ̨
�� ��ʱ�ɽ���������˿��1:1Ť�أ�
�� ˫�Ƕ���Ӱȷ��λ�á�
��������������——��0.014"�������������֧�ŵ��ܣ���ͨ������Ԥ���������ͳ��α�����Ħ����——��һ���dz���������д���̿��鵫����ʵ�õ��ַ�������������BTK���㲿��������CTO�����ߵ���������֧���Ը�“�Ʋ���”ʱ��
�ҳ��Խ����ļ���Ҫ���Ⲣ�����ٴ�ԭ�������������ʹ�á�
1. Ϊʲô��0.014"���������Ҵ���֧�ŵ��ܣ�
��ͳ������ʹ�����ܣ���CXI��Finecross����Ϊ��˿��“����”����������һ��ȱ�㣺�⻬��Ħ������ʵ��С�������Ǿۺ�����Ƥ�ڸƻ����ֲڵı���ͨ���У���
��0.014"���ң�ͨ���ǿ��ٽ����ͣ���Mini Trek��Emerge��Armada 14�ȣ���Ϊ֧�ŵ��ŵ㣺
| �ص� | ���� |
| ���͵�ͨ������ | ����δ����ʱ�⾶��С��1.5-2.0mm�����ұ�������ˮͿ�㣬�����ܸ�˳���� |
| �������� | ����ԭ��“������”ê��Ѫ�ܱڣ���Ϊ�ȶ����ƽ�ƽ̨�� |
| ��“Ԥ��”���� | �������ź�ɼ��ٺ����ƽ���Ħ������ |
| ��ֱ������ | һ���������䣬����ֱ�����Ų��䣨���轻����е���� |
�ٴ�����������������Ѿ����˱����ν��˵���ô���Ʋ���ȥ�����䳤�θƻ���������ͬ��ĵ��������ң�����2.0×20mm��������˳�����롣
2. “������������Ħ����
→ ������Ҫ�������������Խ���Ħ���� → ֻʹ��2mm���Сֱ������”
ԭ����
�������κܳ���>15cm���ҳ����ƻ���������ά��֯ʱ����˿��Ȼͨ���ˣ����κκ�����е�����ҡ����ܣ�������ܵ���ı�������������������Ҫ���Ա���ͨ���ڲ��Ĵֲڱ����Լ�ͨ��ֱ������е��“����”��
��ʱ���ڱ����εĽ��ˣ���ڴ�������С���ҽ��оֲ����ţ���2.0mm���С����������ڸ�����ͨ��“�ؿ�һ��”����һ��“����”��“����©��”��ʹ�ú��������һ��ܹ����벢��һ��ǰ����
ΪʲôҪ��≤2mm���ң�
- ��ȫ��BTKѪ�ܱ���ֱ��2-3mm��2mm�������Ų�����ɴ������ؼв㡣
- Ŀ�Ľ�����“���ͳ�ʼĦ����”�������������������䡣
- �������̫��≥3mm�������ܵ���Ѫ��˺�ѻ��ǻ����
�������裺
1. ��˿��ͨ�������Σ����ٵ���Զ����ǻ����
2. ��2.0mm�����͵������ν�����ڣ���˿��¶������
3. ����������2-4atm����ʹ�������ſ�����ά��10-20�롣
4. �س����ң���ʱͨ����ڵ�����Ӧ�����½���
5. ���Խ����ң���һ�����ң���ǰ���ʹ������������Ρ�
ע�⣺��Ҫ���������С����һ�������ų��β���——��������������ѻ�Ѫ�����ˡ�
3. “�����ڵ�һ�����ź�ʹ���µ�����”����Ϊ�ù���������ʱ������ͨ������”
�������dz����������������ٴ�ԭ��
- ���Σ������ڵ�һ�����ź�ʹ��ֻس飬���۵����ܲ�����������������С�������“����ЧӦ”����������Ѫ�ܱڵ�Ħ����
- Ϳ��ĥ����ˮͿ���ڵ�һ��ͨ����խ����ʱ�ᱻ����ĥ�𣬵ڶ���ʹ��ʱĦ����������
- ����С�ƻ���Ƭ�����ұ������Ƕ��ϸС������ôֲڡ�
��ˣ��������ڽ���Ԥ������ɺ���һ��ȫ�µ�����ȥ��Խ���α����������ҵ�ƽ�����桢����Ϳ��������۵�ʹ�����������Ѿ������ֿ�ͨ��ͨ����
4. ʵս���������ϣ�����֮ǰ�Ľ��������νӣ�
| ���� | ���� | Ŀ�� |
| 1 | ����˿ + ���� ����ͨ��CTO | ����Ѱ�� |
| 2 | ������̫���θƻ��������� 2.0mm�����ң������ܣ� | �������������ù⻬�� |
| 3 | ���ҵ������������ڣ���ѹ���ţ�2-4atm�� | �������Ħ�����γ�“©��” |
| 4 | ���������ң��������س�ã� | —— |
| 5 | ���õڶ���ȫ��2.0mm���� | ����Ϳ��ͱ������� |
| 6 | ���Խ��ڶ��������ƹ����������� | ���ɹ�������ֱ�����Ż�֧�ܡ� |
5. ע�����������
- ��������ţ�BTKСѪ��ʹ��2mm���������д��ס��в��Ѫ�����ѷ��ա�
- �������“��”���ţ���Ҫ����һ���������������䡣
- ȷ�ϵ�˿����ǻ������ڼ�ǻ����Ĥ�����ţ��ᵼ�¼�ǻ����֧��ʧ��
- ����ͨ��ʧ����ô�죺������������ͨ�����ɿ�������Ϊ0.018"ϵͳ����Ȼ�������ڱ��⣩����ʹ��֧�ŵ���+��ˮ��˿������Ĥ�³��ԡ�
ͨ��ϥ�¶��������Բ���“���Ҵ���֧�ŵ���”���������˴�������CTOʱ�Ĺ���ѧ˼ά���Ƚ���Ħ�����������¹���ͨ����
“����С����Ԥ�� + ����������ͨ��”��������߳��θƻ������Ľ���ɹ��ʣ������ʺ�BTK����
��˳�У�Antegrade����·����ʧ��
��ǰ��Antegrade����·����ʧ�ܺ���ξ�����һ������CTO�����о����ɰܵĹؼ��ڵ㡣����“˼��ʧ��ԭ��”�Լ�����ѡ������/��Ĥ�£��;������أ��ƻ�/Ŀ��/Զ����·�����dz�ϵͳ��
�����ٴ�ʵս������һ�������ľ��߿�ܡ�
һ�����ʣ�ǰ��Ϊʲôʧ�ܣ�
�ڿ��ǻ�·��֮ǰ������۸��̡�����ʧ��ԭ���Ϊ���ࣺ
| ʧ������ | ������� | �Բ߷��� |
| ��ǻ��ʧ | ��˿�ѽ�����Ĥ�£�����ͨ��������ǻ����ʹʹ������װ�ã� | → ����Ĥ�¼��������Զ��δ���𣩻� → ������· |
| ������άñ | ��˿ͷ���ڽ���ñ����������/�����룬��ʹʹ�ø�Tip���ɵ�˿��Astato 20�ȣ� | → ���д��̣�����ƻ�ñ���� → ʹ�����Ӽ���/IVUSָ������ |
| Զ����½������ | Զ����ǻϸС���������䡢����“��” | → ������·�ṩ���õ�Զ��ָ�� → ����Ѫ���ؽ������ٴ��ɽ��ܣ� |
�ؼ��㣺ʧ�ܲ�����“����”������Ϊ��һ���ṩ��Ϣ��
����ǰ��ʧ�ܺ����Ҫѡ��
1. ������·��Retrograde Approach��
������
- ǰ��˿����Ĥ����������ǻ����Զ���н�����Ѫ�ܶο���Ϊ���̰С�
- Զ���в�֧ѭ�����㲿�������ɹ����д��̣����㱳�������ֺ������趯��Զ�ˣ���
��·��ʽ��
- ���Բ�“����”��·��ͨ����֧�����γɻ�·���羭��ǰ→���→�ֺ����У������������С�
�ŵ㣺
- �ṩ���̵Ĵ����룬�������Ʒ���
- ��ͬʱ����“��ʦ”��kissing wire����“ͨ��ץ��”��externalization��������
ȱ��/���գ�
- �������ӡ�����ʱ�䳤��
- ��ҪԶ���пɴ��̵Ľ��������Σ��ƻ���ϸС���������ѣ���
 |
 |
 |
 |
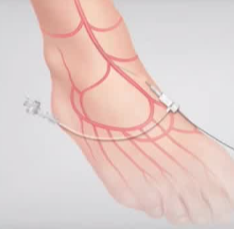
�����㲿��·�Ǵ�������ϥ�¶���CTO��������ȫ����������Ҫ��������������·����ɶ������̣�ʧ��ʱ����Ϊ��ͨѪ���ṩ�˹ؼ���“����ͨ·”��
����˵��һ������������ͨ·������һ�������Ĺܵ��������ξ����ڽ��״����ء������㲿��·���Ǵ�“����”�����Σ��㲿����Դͷ�����ࣩ���̺Ͳ�����
�����������
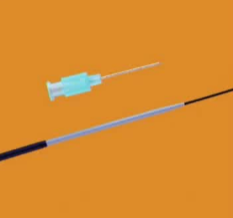
רҵ�Ĵ�������������·�ɹ��Ļ�������ʹ����������С�Ĵ�����ɴ��̡����������ֵ���������ؼ�����Աȣ��������������������| ��� / ���� | Cook Micropuncture® Pedal Access Set | Merit PAK™ Pedal Access Kits(��MiniΪ��) |
| ������ | 21G, 4cmEchoTip®�� | ��������ǿ(ͬ��)������������ |
| ������ (ID/OD) | 2.9Fr (ID)/ ~4Fr (OD)���䳬ϸ�ھ���Ϊ�ؼ� | 4Fr��ˮ�� (PreludeEASE®) |
| ��˿ (GW) | 0.018" ����ŵ��˿ | ����ŵ/���� (NPD) ��˿ |
| �������� | ��������רΪ�����������ƣ�2.9Fr�ھ��DZ�־ | �ṩ�����ھ������ں�����е���룻������ˮ |
ע��IDָ�����ھ���ODָ�����⾶��
���˺������������ɹ����벻������������е��������ϣ�
· ֧�ŵ�������CXI® (2.6 Fr) ��XO Cross 14����������ǿ֧���ԣ�ΪϸС��˿�ṩ“����ͨ��”��
· ��������/���������ڴӹɶ�����·�����ȶ���ͨ·�����ץ������ȡ��˿��
���̳ɰܵĹؼ�����·��ѡ��
ѡ���ĸ��㲿�������д��̣��Dz��Եĵ�һ��������Ҫȡ���ڲ���λ�ã��Լ��ĸ�Ѫ����������ĩ�˵�·���̡��Ƕȼѡ�· ��ǰ����/�㱳��������ã�λ���㱳��
· �ֺ�����λ��������γ��á�
· �趯����λ�������ǰ������ʹ��ʱ�ſ��ǡ�
�߲�����ָ��
����������е�ʹ��̵�����⣬���������д��̲����������£���1����������
�ڳ��������£�ʹ��21G��������ǿ��������ֱ�Ӵ���Ŀ�궯������������������ϸС�ҳ����иƻ��Ķ����뾲����������߳ɹ��ʲ��������ա���2�������뵼˿
��Ѫ����ζ������ڶ����ڣ���ͨ�����������������Դ���0.018Ӣ������ŵ��˿���õ�˿�������ܣ�������Ӧ�㲿����·���������ṩ�㹻��֧��������3����������
�ص�˿���������ʡ���һ�����ȹɶ�����ܸ�����ս����Ϊ�㲿Ѫ�ܸ�ϸ�������Ρ���Cook Pedal Access Set�����⾶������4Fr�������ھ�Ϊ2.9Fr����������ȼ��ٴ��ˡ���4�����������͵�˿��֧�ŵ���
ͨ���ʣ�����0.014Ӣ���CTOר�õ�˿��֧�ŵ��ܣ���CXI֧�ŵ�����XO Cross 14������������������͡���5����������ʦ
���е�˿��ͨ��������˿����Fielder XT����ɶ���˳�е�˿�ڱ������������ж���“��ʦ”������ѡ��· ��ʦǣ������Kissing-Wire Technique��������˿���ơ�
· ��˿�⻯������ץ���������������ܣ��Ӷ�������ץס���е�˿ͷ�˲��ӹɶ������������γ�������“��ͨ”ͨ·��Ϊ������е���뽨��“���”��
��6����������Ԥ����
��ʦ����“���”����С���ң���1.5-2.5mm������Ԥ���ţ���ֱ�ӽ��к������ơ���7�������̵�ֹѪ
���ж������̵��ֹѪ�м��ֳ��÷�����· ���̵����ҷ�����ص�˿��С���������̵㣬��ѹ���������ӣ����dz�������Ч�İ취��
· �ӳ�ѹ������������ʱ���������ڴ��̵���г�������Ч���˹�ѹ�ȡ�
· �������Ϸ������������ѡ��ͨ�����̵�ע����������ȷ�²��ϣ����������ڸ߷��ջ��ߡ�
��ս��Ӧ��
�����㲿��·����Ч�����������ܣ���Ҫ��ս��Ӧ�Դ�ʩ���£�· Ѫ�ܾ������㲿ϸСѪ�ܶԴ̼����С�����Ӧ���ᡢ���٣���Ҫʱ��ͨ�����ܻ��ʹ�ע��������͵�Ѫ�����ż���
· Ѫ��/���Զ���������Ҫ��ֹѪ�������йء���ˣ�����Ҫȷ����֡���Ч�ҳ־õİ�ѹ��
· ����ʧ�������Զ��������·�ȸƻ�����������ɴ��̻�ͨ������ʱ����ƶ������������Ǹ��ɿ��ı�֫�������������ֶ�������ʹ�ã�����ḻ�����߿���ѡ���趯����
2. ��Ĥ�¼�����Subintimal Approach�� ��ǿ������
ע�⣺�ܶ�ǰ��ʧ�ܵIJ�����ʵ�Ѿ�����Ĥ�¡�������“����Ĥ��”��ָ��������˿������Ĥ��ƽ�棬���ƻ��Ե�Զ��������ǻ��
�ʺ������
- �����γ����ƻ������أ���Ĥ��ƽ����Թ⻬��
- û�к��ʵ����д��̰е㣨Զ�����������Ѫ��̫ϸ����
���ߣ�
- ���ߵ���������˿��������loop technique������Ĥ��Ѱ����ǻ�ڡ�
�ŵ㣺
- ���ڳ��Ρ��Ǹƻ�Ϊ���ı������ɹ��ʽϸߡ�
ȱ�㣺
- �������ڸƻ����صIJ��䣨��Ĥ��ƽ��ƻ����γɣ���
- ����ʧ����������������Ӷ����ߡ�
����ٴ�ʵ��������Ƚ���ͷ��տ��Ʋ��䡣
(1) Ϊʲô��Ҫ“������Ĥ��”��
��֮ǰ�������У�����һֱǿ��“����������ǻ”��������������ͬʱ����ʱ��������Ĥ�³�ΪΨһ���е�ǻ��ѡ��
| ���� | ˵�� |
| ��Զ�˰е� | Զ����ǻ��������խ���ƻ�����������Ϊ���д���Ŀ�� |
| ��������· | �㲿����ȫ������/����/ϸС�����������ܶ���� |
| ǰ����ʧ�� | ��ǻѰ����ͨ������CTO��˿Ҳ���̴��ƻ�ñ |
| ��֫ѹ���� | CLTI�������ٽ�֫���գ����볢�Կ�ͨ |
����������Ĥ�¼����ı�����“��������һ���ɿصļв�”���ƹ������Σ�Ȼ����Զ�����½�����ǻ���������˲�֧�������������ɿ�ͨ�Ļ��ᡣ
��2������
1.“Intentional balloon dilatation proximal to start the subintimal”
ΪʲôҪ�ڽ��������ţ�
��Ĥ�¼�������ʼ�����ǣ��ڱ����ν��˵Ľ���Ѫ�ܶΣ��õ�˿����“����”��Ĥ��������Ĥ��ƽ�档����ʱ����Ĥ�ܼ��ͣ���˿���Դ��롣
���ļ��ɣ��ڼƻ�������Ĥ�µ�λ�ã���������ʼ���Խ��ˣ�������һ��С���ң�2.0-2.5mm����ѹ����һ�£���ɾֲ�����Ĥ“˺��”���ɳڣ�Ȼ�������뵼˿������������Ĥ�¡�
�������裺
1. ��˿�͵������ν��˵Ľ���Ѫ���ڡ�
2. ����2.0mm���ң����������Ĥ�µ�λ�õ�ѹ���ţ�2-4atm������10�룩��
3. �������ң����õ�˿����ˮ����˿���Ӳ��˿���������Ŵ�������ת���ͣ���˿����Ȼ������Ĥ��ƽ�档
���ƣ���������Ӳ��˿ǿ�д�����Ĥ�����IJ��ɿ�˺�ѡ�
2. “Don't be afraid to use half-stiff 0.035" Terumo for tibials if no calcifications”
����۵�dz�����ʵ�ã����������ϸ�ǰ�ᡣ
����֪��ϥ��Ѫ�ܣ���ǰ���ֺ��趯����ͨ��ֻ��0.014"��0.018"ϵͳ��0.035"��˿����Ϊ̫�֡�̫Ӳ����������Ѫ�ܡ�
���飺���ƻ����ֶ����У���Ӳ0.035" Terumo��˿��ͨ��ָTerumo ST-35��RS-35�ȣ�ͷ�˽������岿��һ��֧����������ֱ����������Ĥ��ͨ����
Ϊʲô���У�
- 0.035"��˿֧������ǿ��������������ͨ�����α�����
- ͷ����ˮ��J�Σ�������“���Է���”���ԣ��ʺ���Ĥ����չ��
�����ռ��ߣ��������㣺
- ✅ Ѫ��ֱ���㹻������3mm������0.035"��˿�γɵĻ����ܳ���Ѫ�ܣ���
- ✅ Զ������ȷ������е㣨����˿�����������죩��
- ❌ �������ڹ��N���������СѪ�ܣ���������㱳����Զ�ˣ���
3.“Very useful if no target and no distal access for retrograde puncture”
������ǿ������Ӧ֤���ġ�
��Զ����ǻ��ȫ�����ϣ������Ա�������������Ϊ�е㣩�����������д���ʱ����Ĥ�¼�����Ψһ��ѡ��
��ʱ�IJ��Ե�����
- ������“������”�����Ǿ����ܳ���������Ĥ��ͨ����ֱ��Զ�˳��ֿ�ʶ�����ǻ��
- ���Զ��ʼ������ǻ�����Գ�������Ĥ��ֱ�ӷ��ø�Ĥ֧�ܣ���Viabahn��������֧�ܵĻ�е���Ͻ�Ѫ�����ǻ����——��BTK�����������������֧���ױ�����
4. “If no re-entry consider a re-entry device”
����Ĥ��ͨ���Ѿ�����������˿����Ȼ������ǻʱ��ʹ������װ���DZ�������
��������װ�ã�
| װ�� | �ص� | ����Ѫ�� |
| Outback (Cordis) | 0.014"���ݣ��ɵ�����ͷ | ���N������BTKҲ���ã���������� |
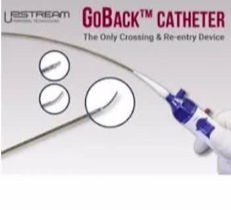
| Pioneer (Medtronic) | ��IVUS̽ͷ��ʵʱȷ������λ�� | ���N����Ϊ�� |
| OffRoad (Boston Scientific) | ˫ǻ����+������ | ���N���� |
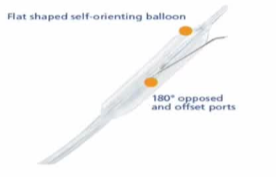
| Enteer (Covidien) | ���ͳɱ� | ���N���� |
 |
 |
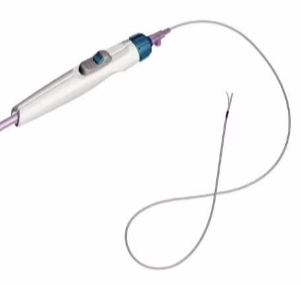 |
| Pioneer Catheter (Philips) | GoBACK CATHETER | OUTBACKIM Elite Re-Entry Catheter (Cordis) |
 |
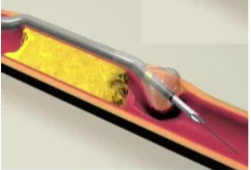 |
| Enteer Re-entry Catheter-(Medtronic) | Offroad catheter (Boston scientific) |
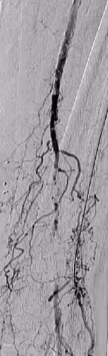
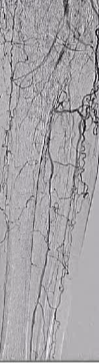
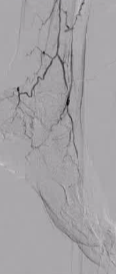
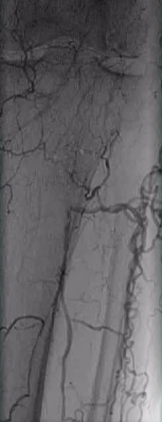
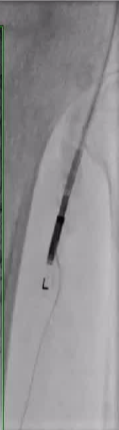
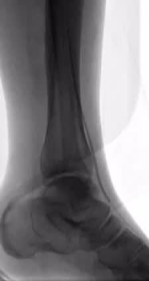
82 ��Ů�ԣ�����������Ѫ֢֬�Լ���֫����Ӳ������֢��
 |
 |
 |
 |
 |
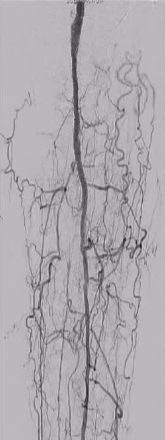 |
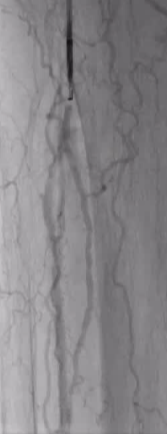
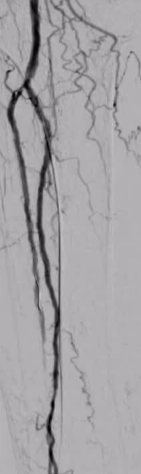
�N��������
 |
 |
 |
 |
 |
 |
| Outback������ϥ�����µĶ����� �Ӽ��������������� 10 �γ����гɹ�ʵ��������ǻ�Ĵ����ﵽ�� 9 �Ρ� |
��BTK��ʹ������װ�õ���ս��
- װ�ñ����⾶�ϴ�ͨ��4-5F�������ֶ����ڲ������¾��Ρ�
- ���飺����≥3.5mm���ֶ�������ʹ�ã�Զ�˾���������Ȼ�����С����������
��3����Ĥ�¼���������������
��4����Ĥ�¼����ķ�����Բ�
| ���� | ������ | Ԥ��/���� |
| ��ǻ���� | ���� | ���Ƶ�˿��ֱ�����ƻ�ʱԼ5-8mm���������ν��� |
| ��֧�ƻ� | ��Ȼ���� | ��ǰ��֪���ߣ�����������Ĥ�³��� |
| ������ | 10-30% | ��ǰ������װ�ã����Ϊ�������� |
| Ѫ�ܴ��� | 5-15% | ˫�Ƕ�ȷ�Ϸ��������ҵ�ѹ����ƿ� |
| Զ��˨�� | �ټ� | ʹ�ñ���װ�ã���SpiderFX����С����Ԥ�� |
��5��֮ǰ���Եĺ�Ӧ
| ֮ǰ�IJ��� | ��Ĥ�¼����е����� |
| “����������ǻ” | ��ǻʧ�ܺ�����ѡ�� |
| “������·����” | ����������ʱ������Ĥ�� |
| “�ƻ���������” | �ƻ�������0.035"���ضȸƻ����Ƽ���Ĥ�� |
| “��������” | ��Ĥ��ͨ�������轵������˿������ǻ |
| “����֧��” | ��������Ԥ����������Ĥ�� |
��һ�Σ���CTO��������“�Ƹ�����”�ļ�����
��ǰ����ǻ�����֡�������·������ʱ��������Ĥ��������ǻ�ڱ�֫�ֶΡ�����ļ��ɰ�������������Ԥ����������Ĥ�£��ƻ����ֶ����ɿ�����0.035"��Ӳ��˿����ͨ��������������װ��Ӧ������Ȼ����������
һ�仰���ɣ���Ĥ�¼���������ѡ��������û������ѡ��ʱ�������ܾ���һ֫��ǰ�����������֪�����գ������д�������֢��������
�����ٴ��У���û����������Ĥ�¼�������Զ��Ѫ����ȫ�ƻ�����������ȱѪ�İ���������“���䱣��”�ľ��߽߱�����������������ľ��顣
����ָ�����ߵ���Ҫ�أ����ᵽ�ĸƻ�/Ŀ��/Զ����·��
�� �ƻ���Calcification��
| �ƻ��̶� | �Ƽ����� | ԭ�� |
| ����ȸƻ� | ��Ĥ�¼������� | �����γ���Ĥ��ƽ�棬����ɹ��ʸ� |
| �жȸƻ����ڶ��ԣ� | ������Ĥ��+����װ�ã���ʧ��→���� | �ƻ����谭��Ĥ��ͨ������չ������ |
| �ضȸƻ������Ρ����Σ� | ������·����������Զ�������̣� | �ƻ�ñ̫Ӳ��ǰ�����Ĥ�´����ոߣ�������ֱ�Ӵ�����Ľϱ���άñ |
�ƻ��Ǿ����ܷ�ȫ����Ĥ�µ�����Ҫ���ء����CTOȫ����“ʯͷ��”����Ĥ�¸����߲�����
�� Ŀ�꣨Target / ����㣩
- Զ����ǻ�������䡢ϸС�����������Ĥ������ʧ���ʸ� → ������������·����Ϊ���е�˿��ֱ�Ӵ�Զ����ǻ���֣�������“��”��
- Զ������Ҫ��֧�������������ƻ� → ������·���ɿء�
�� Զ����·������Distal Access Feasibility��
- Զ�������̣��缫ϸ���ƻ������ؾ��λ���ȫ������→ �������У�ֻ������Ĥ�»���Ĥ�£���·���������룬���߽���������·��
- ���̷��ոߣ��综�߿�����ѪС��͡��㲿��Ⱦ��→ �����������У�����Ĥ�¡�
�ġ�ʵս��������ͼ���棩
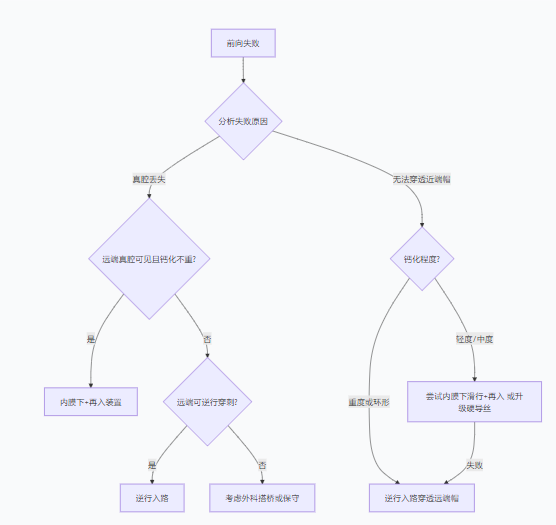
ǰ��ʧ�ܺ��ضȸƻ���Զ����ǻ���� → ��ѡ������·�����жȸƻ���Զ���������е� → ������Ĥ��+����װ�ã�Զ�������� → ����ǻ�ڻ�ת��ơ�
�ܽ������**���ڸƻ��̶ȵĶ��ַ���������**�dz���������CTO�����зdz�ʵ�õ�ʵս��ܡ����ڴ˻�������һЩ�ٴ�ע�ͺ����죬ʹ���������
A) �������ƻ���No or limited calcium��
“Do whatever you can to stay intraluminal → retrograde”
�ؼ�����
· ����/�ٸƻ��IJ����У���ǻѰ������ȫ���е�����Ϊ�������“����”����˿������˳��ͨ������֯ƽ�����Զ�ˡ�· ���ǰ���Ժ�����ͨ����������·����ѡ����������Ĥ�¼�����
Ϊʲô��ѡ���У�
·���к��������ȫ����ǻͨ����������Ĥ�²��������IJ�֧�ƻ�������խ���ա�
·������·������
�������п�Խ��ͨ����֧��·���羭�趯��→���→�ֺ����뵼˿����ͨ�������Ρ�
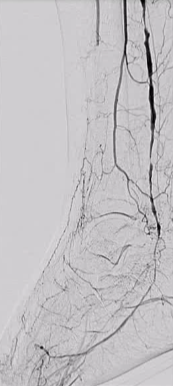 |
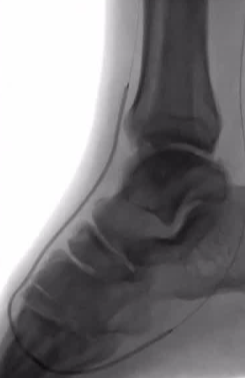 |
 |
�ٴ�Ҫ����
· �ƻ���ǰ��ʧ�ܵij���ԭ��˿������Ĥ�µ������롢����ǻ��ʧ�����п��Դ�Զ��“�ӻ���”��· ����Ҫʹ������CTO��˿��������ˮ��˿��Sion��Fielder XT�������������ͨ����
B) �ضȸƻ���Severe calcium��
“Try to stay intraluminal → CTO wires → Retrograde��”
�ؼ�����
· �ضȸƻ�ʱ����ǻ�����Ѿ���ȫ���ƻ�������˳��ǰ������ҵ���ǻ��ڡ�· ����Ȼ���ȳ���“����������ǻ”��ʹ�ø�Tip���ɵ�CTO��˿����Astato��Victory�����Դ̴��ƻ�ñ��Ѱ�ҿ��ܴ��ڵ�Сͨ����
· ��ǰ��CTO��˿��ʧ�ܣ��ٴο���������·������ʱ�Ѷȸ��ߣ���
Ϊʲô�ضȸƻ�ʱ������·���м�ֵ��
· ���п����ṩ��ͬ�Ĵ��Ƕ�����Զ�����̸ƻ������“Զ��ñ”����ʱ��ǰ������ף�Զ��ñ���ܸ�����ƻ��̶Ƚ��ᣩ��· ���е�˿������ǰ��˿“��ʦ”��kissing wire��������������ʦ��ץ���⻯��externalization������������������“��ͨ”��������ں�����еͨ����
�ضȸƻ�ʱ��������ս��
· ���д��̱������ѣ�Զ�˶���Ҳ���ܸƻ������̺��������ܸ����ѡ�· ���е�˿Ҫ���д������θƻ���������Ҫ��ǿ��֧�źʹ�����
· �������Ҳ��������ǻ�����ܱ��Ƚ�����Ĥ��ͨ���������·��
Ϊʲô“�ƻ�”�Ǿ��ߵķ�ˮ�룿
�ƻ����ı��˲����“��������”��
| ���� | ��/�ٸƻ� | �ضȸƻ� |
| ��ǻ���ڿ����� | �ϸߣ���ͨ���� | ���ͣ��ƻ������� |
| ��Ĥ�¼����Ŀ����� | �����γ���Ĥ��ƽ�� | �ƻ���ֹ��Ĥ����չ |
| ������·���Ѷ� | ������ף�Զ��Ѫ�ܺã� | �ܸߣ�Զ��Ҳ���ܸƻ��� |
| CTO��˿�ı�Ҫ�� | ����Ҫ�������Ҫ | �������� |
| �⻯�����ļ�ֵ | ���п��� | �dz��м�ֵ |
һ�仰���ƻ��������“����֯ͨ��”ת��Ϊ“ʯ��”�����漼������ʧЧ��
�����ľ�������ͼ
����ж�“��/�����ƻ�” vs “�ضȸƻ�”��
��ʵ�ʲ����У��ƻ����ж���Ҫ��ģ̬Ӱ��
| ���� | ��/�����ƻ� | �ضȸƻ� |
| ��ǰCTA | ������ɫ���ܶ�Ӱ | ���Ρ����Ρ������ܶ�Ӱ |
| ������ | �����Բ���Ӱ | ����ɼ��Ĺ�״���ܶ�Ӱ |
| IVUS�����У� | dz��������ƻ� | >270°���Ρ���㡢����Ӱ |
| ��˿�ָ� | ����������“����” | Ӳ���ֲڡ���“ɰֽ��” |
TIP��������з��ֵ�˿ͷ�˷���“��ס”����ͨ���κ��������ƽ�����ʹ�����е�Ӳ�ȵ�˿Ҳ������“�����”��Ӧ�߶Ȼ����ضȸƻ���
���ַ�ֱ�ӡ�ʵ�ã�
· ��/�ٸƻ�→ ������· > ��Ĥ�£�Ŀ����ȫ����ǻ��
· �ضȸƻ�→ CTO��˿ǰ���� → ʧ�ܺ�������·�������⻯������ǻ��Ϊ��ѡ����������Ĥ����Ϊ��ѡ��
��������ǰ���ᵽ��“��������”��“����֧��”��“�㲿����ѧ”��ϸ����ȫ���ݣ�������һ���Ӽ����ӡ�����ǻ����Ĥ�¡���ǰ�����е�����CTO������ϵ��
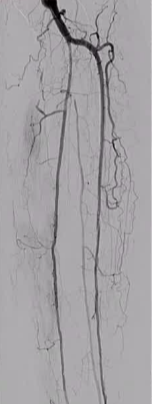
3֧Ѫ������
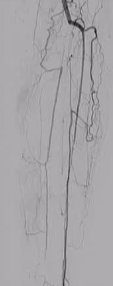 |
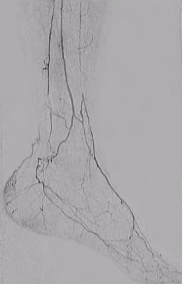 |
 |
 |
 |
 |
 |
����
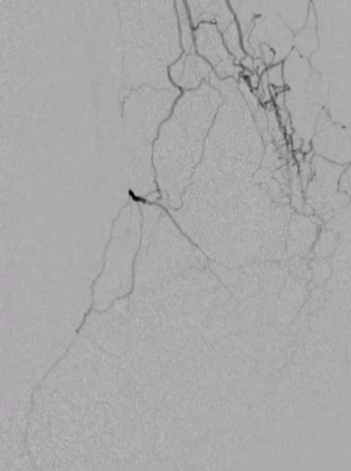
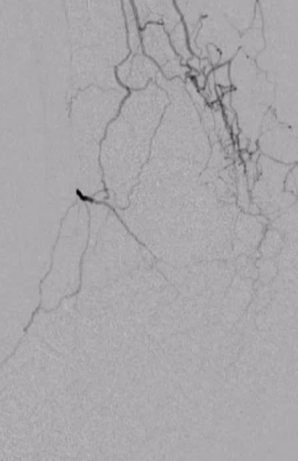
ϥ���¶���������ǻ��ͨ��
��������λ�ã�
�Ա����и��
��ͨ�����ֹ��ϣ�
������˿Ӳ��ʾ����
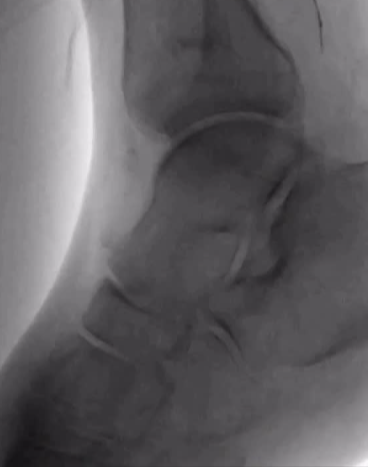
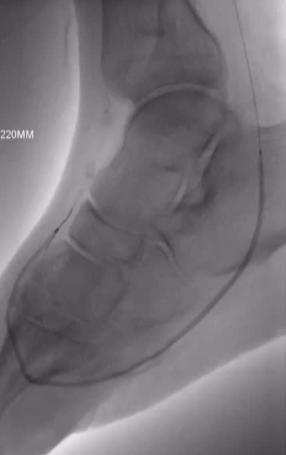
ϥ���¶�������������Ĥ��ͨ��
�������й�ǻͨ����ʱ��
ת������Ѫ����Ĥ�µĿռ���в�����
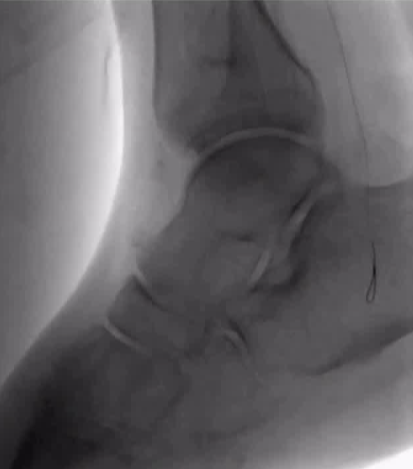
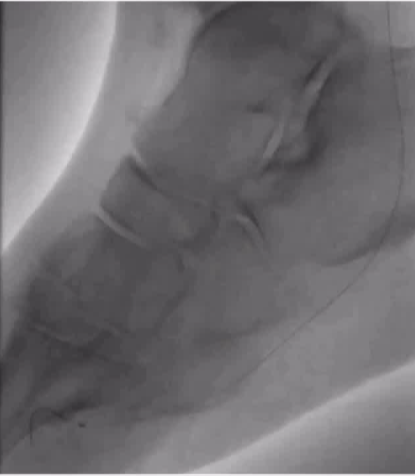
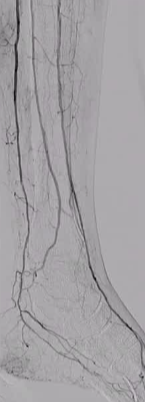
�����ε���������������Χ
ʹ���ٽ���װ�û�ר�õ��������½��������Ĺ�ǻ�ڡ�
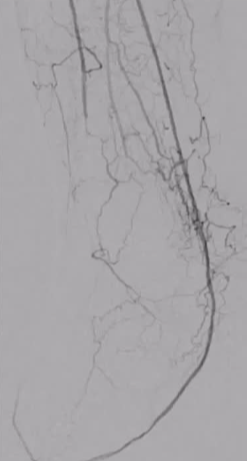
����ḻ����Ա�����£��ɹ��ʿɴ� 85%��
�ֶ���PTA�ļ����ѵ������Ҫ��С�ᾶ���ҵ��ܣ�ϸ��˿������ʱ������ʹ�ø��ء�Ѫ�����ż��Ϳ�����ҩ��ֶ������ҵ���4.3F���С����˿ֱ��<=0.018Ӣ�硣�۸�ȳ���ĵ��ܺ͵�˿��2-5����
������ֶ��������֢״������Ҫ���ƵĻ����Ƕ�ˮƽ���䡣���Զ����������Ҫ���ȴ������N�������䡣���N����PTA���ƣ�˳�д��̹ɶ��������5F�ʹܻ��Сֱ�����ʹ��ڹ�dz�����ڣ�������“·ͼ”�����½�0.018ֱ����˿ͨ��������ص�˿�����������ŵ��ܡ�����ֱ�����ֶ����϶�ѡ��3-4mm���ж�Ϊ2-3mm�����¶�Ϊ<2mm���������ڵ�������������������ȷ������ֱ������“·ͼ”Ӱ�����������ʱ����ȷ�����ŵ�����ֱ����Ҫ������������������ֱ����
�ֶ���PTAʱ�����ǿ���ػ����״θ��ؼ���Ϊ8,000-10,000��λ�������ʱ���ӳ����Ӽ�����Ҳ�н���ҽ����ǰ��ͨ�����ͼ�����Ī��ƽ 10mg ���£���Ѫ������ҩ��cutaneous nitroglycerin paste, or serial intraarterial bolus of 100ugof nitroglycerin���Լ���Ѫ�ܾ��Ρ���ʹ��Ѫ�����ż�ʱ��ϸ�ؼ��Ѫѹ�Ա���Ѫѹ���͡�
PTA������Ҫ���ڵĿ�ѪС�����ƣ�ͨ���ڷ���˾ƥ��325mg/�ա����������Ѫ���ٶ������������Ʋ��ɹ������߲������ض���Ҫ�����Ի��������