МвДҝұИҪПҙуЈ¬ХвАпЦчТӘІыКцөДКЗ Intrahepatic cholangiocarcinoma what can you offer? №ШУЪёОДЪөЁ№Ь°©өД¶ЁТеЈ¬ұҫАёДҝТСҫӯУРІыКц
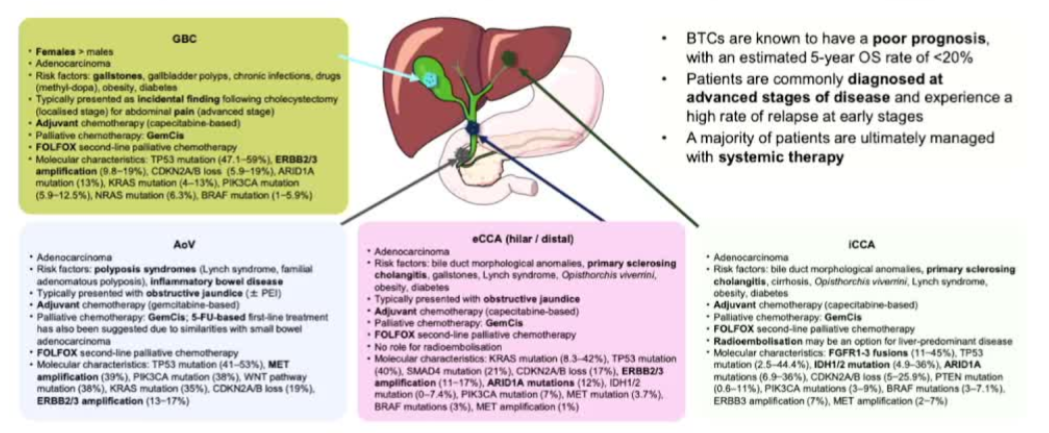
өЁДТ°©1. БчРРІЎС§МШХч· РФұр·ЦІјЈәЕ®РФ¶аУЪДРРФЈЁFemales > MalesЈ©ЎЈ
o өЁДТ°©ФЪИ«ЗтҫщУРГчПФЕ®РФЖ«әГЈ¬ҝЙДЬУлЕ®РФөЁҪбКҜ»јІЎВКёьёЯЎўҙЖјӨЛШУ°ПмөЁЦӯіЙ·ЦУР№ШЎЈ
|
| »щТт | ұдТмАаРН | ЖөВК | БЩҙІТвТе |
| TP53 | Н»ұд | 47.1–59% | ЧоіЈјыН»ұдЈ¬УлФӨәуІоПа№Ш |
| ERBB2/3ЈЁHER2/3Ј© | А©Фц | 9.8–19% | HER2А©ФцФЪөЁДТ°©Па¶ФіЈјыЈ¬ҝЙіўКФҝ№HER2°РПтЦОБЖ |
| CDKN2A/B | ИұК§ | 5.9–19% | ТЦ°©»щТтИұК§Ј¬Пё°ыЦЬЖЪК§ҝШ |
| ARID1A | Н»ұд | ~13% | ИҫЙ«ЦКЦШЛЬ»щТтЈ¬өЁөА°©МШХчРФН»ұдЦ®Т» |
| KRAS | Н»ұд | 4–13% | өЁөА°©ЦРҪПөНЈ¬ө«ҙжФЪМбКҫMAPKНЁВ·»о»Ҝ |
| PIK3CA | Н»ұд | 5.9–12.5% | PI3K/AKTНЁВ·»о»Ҝ |
| NRAS | Н»ұд | ~6.3% | ЙЩјы |
| BRAF | Н»ұд | 1–5.9% | ЙЩјыЈ¬¶ајыУЪV600E |
· ұКјЗЦРERBB2/3 98-19%УҰОӘ9.8-19%ұКОуЈЁОЮЦЧБцHER2А©ФцВК98%Ј©ЎЈ
· COKN2A/BУҰОӘCDKN2A/BЎЈ
К®¶юЦёіҰИйН·ПЩ°©
Хв¶ООДЧЦКЗ№ШУЪК®¶юЦёіҰИйН·ПЩ°©ЈЁAmpulla of Vater AdenocarcinomaЈ©өДБЩҙІТӘөгЧЬҪбЈ¬ө«ФӯОДҙжФЪІҝ·ЦЖҙРҙҙнОуәНЛхРҙЈ¬ТФПВКЗРЮХэәуөДНкХыЦРОДҪвКНЈә
Т»Ўў·зПХТтЛШ
· ПўИвІЎЧЫәПХчЈәБЦЖжЧЫәПХчЈЁLynch syndromeЈ©ЎўјТЧеРФПЩБцРФПўИвІЎЈЁFAPЈ©
· СЧЦўРФіҰІЎЈЁIBDЈ¬ИзҝЛВЮ¶чІЎЎўАЈСсРФҪбіҰСЧЈ©
¶юЎўБЩҙІұнПЦ
· өдРНұнПЦОӘ№ЈЧиРФ»ЖргЈЁ± ТИПЩНв·ЦГЪ№ҰДЬІ»И«Ј¬PEIЈ©
· ТтЦЧБцО»УЪК®¶юЦёіҰИйН·Ј¬ФзЖЪјҙҝЙЧиИыөЁЧЬ№ЬҝӘҝЪ
ИэЎўЦОБЖ
1. ёЁЦъ»ҜБЖЈЁКхәуЈ©
2. №ГПў»ҜБЖЈЁНнЖЪ/ЧӘТЖЈ©
· УЙУЪёГІЎУлРЎіҰПЩ°©ФЪЙъОпС§ЙПҫЯУРПаЛЖРФЈ¬5-FUОӘ»щҙЎөДТ»ПЯЦОБЖТІұ»МбіцЧчОӘҝЙСЎ·Ҫ°ё
ЛДЎў·ЦЧУМШХчЈЁіЈјыН»ұдЈ©
· MET PЈҝЈәҙЛҙҰФӯОД“MET P mutation (38%)”ҝЙДЬОӘұКОуЈ¬НЖІвЦёMET»щТтН»ұд»тMETА©ФцЈ¬Іҝ·ЦОДПЧұЁөАФј38%
· KRASН»ұдЈә35%
· CDKN2A/BИұК§Јә19%
· ERBB2/3А©ФцЈә13–17%
І№ідЛөГч
· К®¶юЦёіҰИйН·ПЩ°©ЛдКфәшё№ЦЬО§°©Ј¬ө«ЖдЙъОпС§РРОӘёьҪУҪьіҰРНПЩ°©Ј¬¶ш·ЗТИПЩ°©Ј¬ТтҙЛ»ҜБЖІЯВФУРКұІОХХҪбЦұіҰ°©»тРЎіҰ°©ЈЁИзә¬5-FU·Ҫ°ёЈ©ЎЈ· ERBB2ЈЁHER2Ј©А©ФцМбКҫҝЙДЬККәПҝ№HER2°РПтЦОБЖЎЈ
Из№ыРиТӘЈ¬ОТҝЙТФҪшТ»ІҪХыАніЙұнёс»тБЩҙІЛЩІйҝЁёсКҪЎЈ
CCA ёОГЕ/ёьД©ЙТЈЁcholangiocarcinomaЈ©hCCA әНpCCA
ЈЁAdenocarcinomaЈ©Ј¬ө«ҙУ·зПХТтЛШЈЁөЁ№Ь»ыРОЎўФӯ·ўРФУІ»ҜРФөЁ№ЬСЧЎўёООьіжЈ©әНЦОБЖ·Ҫ°ёЈЁGemCisЎўFOLFOXЈ©АҙҝҙЈ¬МШЦёөЁөА°©ЈЁөЁ№Ь°©»төЁДТ°©Ј©Ј¬ЗТДЪИЭЖ«ПтёОДЪ»тёОНвөЁ№Ь°©ЎЈ
ТФПВКЗ¶ФДгМṩөДФӯОДөДЦрМхРЈХэЎў·ӯТлУлБЩҙІҪв¶БЈ¬ұгУЪДгАнҪв»тУГУЪ»гұЁ/ҝјКФЈә
Т»Ўў·зПХТтЛШ
| ГыҙК | Ҫв¶Б |
| Bile duct morphological anomalies | өЁ№ЬРОМ¬ТміЈЈЁИзCaroliІЎЎўөЁ№ЬДТЧҙА©ХЕЈ© |
| Primary sclerosing cholangitis (PSC) | Фӯ·ўРФУІ»ҜРФөЁ№ЬСЧ——Оч·ҪөЁ№Ь°©ЧоіЈјы·зПХТтЛШ |
| Gallstones | өЁҪбКҜЈЁУИЖдУлөЁДТ°©Па№ШЈ© |
| Lynch syndrome | БЦЖжЧЫәПХчЈЁҙнЕдРЮёҙИұПЭЈ© |
| Opisthorchis viverrini | М©№ъёООьіжЈЁ¶«ДПСЗөЁ№Ь°©ЦчТтЈ© |
| Obesity, diabetes | ·КЕЦЎўМЗДтІЎЈЁҙъР»Па№ШЈ© |
¶юЎўБЩҙІұнПЦ
Typically presented with obstructive jaundice
өдРНұнПЦЈә№ЈЧиРФ»Жрг
өЁ№Ь°©Тт¶ВИыөЁ№ЬЈ¬ФзЖЪјҙҝЙіцПЦОЮНҙРФ»ЖргЈ¬іЈ°йҙуұгұд°ЧЎўДтЙ«јУЙоЎЈ
ИэЎўЦОБЖТӘөг
| ФӯОД | РЈХэ/Ҫв¶Б |
| Adjuvant chemotherapy | ёЁЦъ»ҜБЖЈәҝЁЕаЛыұхЈЁ»щУЪBILCAPСРҫҝЈ¬ЛдОҙҙпЦчТӘЦХөгЈ¬ө«ПЦОӘұкЧј·Ҫ°ёЈ© |
| Pallative chemotherapy GemCis | №ГПў»ҜБЖЈәјӘОчЛыұх + ЛіІ¬ЈЁGemCisЈ©——ABC-02СРҫҝИ·БўөДТ»ПЯұкЧј·Ҫ°ё |
| FOLFOX second-line palliative chemotherapy | ¶юПЯ№ГПў»ҜБЖЈәFOLFOX·Ҫ°ёЈЁ»щУЪABC-06СРҫҝЈ¬mFOLFOX6ПФЦшёДЙЖOSЈ© |
| No role for radioembolsation | ОЮ·ЕБЖЛЁИы/·ЕЙдЛЁИыЈЁRadioembolizationЈ©өДөШО»——І»НЖјцУГУЪөЁөА°© |
ЛДЎў·ЦЧУМШХч
| »щТтёДұд | ЖөВК | БЩҙІТвТе |
| KRAS mutation | 8.3–42% | іЈјыУЪёОДЪөЁ№Ь°©Ј»УлФӨәуҪПІоПа№Ш |
| TP53 mutation | 40% | іЈјыЈ¬УИЖдФЪҪшХ№ЖЪ |
| SMAD4 mutation | 21% | УлЧӘТЖј°ЗЦП®РФПа№Ш |
| CDKN2A/B loss | 17% | К§»оҝЙөјЦВПё°ыЦЬЖЪК§ҝШ |
| ERBB2/3 mutation | 0–7.4% | ¶ајыУЪөЁДТ°©»тёОНвөЁ№Ь°©Ј»Іҝ·ЦУРHER2°РПт»ъ»бЈЁИзZanidatamabЈ© |
| PIK3CA mutation | 7% | Йжј°PI3KНЁВ·Ј¬әұјы°РПт |
| MET mutation | 3.7% | ЙЩјы |
| BRAF mutation | 3% | ¶ајыУЪёОДЪөЁ№Ь°©ЈЁV600EЈ©Ј»ҝЙУГBRAF+MEKТЦЦЖјБ |
| MET amplification | 1% | әұјы |
ОеЎўЧЬҪбЈЁБЩҙІТӘөгЈ©
**өЁөА°©ЈЁТФөЁ№Ь°©ОӘЦчЈ©**өДөдРНМШХчЈ»
И·ХпТААөІЎАн+У°ПсЈ¬№ЈЧиРФ»ЖргКЗЧоіЈјыКЧ·ўЦўЧҙЈ»
ЦОБЖВ·ҫ¶Јә
oІ»ҝЙЗРіэ/ЧӘТЖ →GemCisТ»ПЯ»ҜБЖЈ»
oТ»ПЯҪшХ№ →FOLFOX¶юПЯ»ҜБЖЈ»
·ЦЧУјмІвЦБ№ШЦШТӘЈЁKRASЎўBRAFЎўHER2ЎўMSIөИЈ©Ј¬Іҝ·Ц»јХЯҝЙДЬУР°РПт»тГвТЯЦОБЖ»ъ»бЎЈ
ёОДЪөЁ№ЬПё°ы°©
Хв¶ОДЪИЭКЗ№ШУЪёОДЪөЁ№Ь°©·ЗіЈҫ«Б¶өДБЩҙІұКјЗЎЈОӘБЛ·ҪұгФД¶БЈ¬ОТҪ«Ль“·ӯТл”іЙҪб№№ЗеОъөДПөНіҪв¶БЈ¬
1. јІІЎ¶ЁО»
ICCA= Intrahepatic CholangiocarcinomaЈЁёОДЪөЁөЁ№Ь°©Ј©2. ОЈПХТтЛШЈЁRisk FactorsЈ©
ХвІҝ·ЦБРіцБЛёГІЎөДёЯОЈИЛИәЈ¬РЮХэәуИзПВЈә
· Фӯ·ўРФУІ»ҜРФөЁ№ЬСЧЈЁPSCЈ©Ј»
· ёОУІ»ҜЈЁCirrhosisЈ©ЈәФӯОДЖҙРҙОӘcirtosisЈ»
· ёООьіжёРИҫЈәФӯОДOpisthorchis viveminiёьХэОӘOpisthorchis viverriniЈЁчкГЁәуШәОьіжЈ©Ј¬¶«ДПСЗөШЗшіЈјыЈ»
· БЦЖжЧЫәПХчЈЁLynch syndromeЈ©ЈәТЕҙ«РФ·ЗПўИвІЎРФҪбЦұіҰ°©Ј»
· ·КЕЦЎўМЗДтІЎЈәҙъР»РФјІІЎКЗГчИ·өДЦВ°©НЖКЦЎЈ
3. ЦОБЖІЯВФЈЁ°ҙҪЧ¶О·ЦІгЈ©
ЈЁ1Ј©ёЁЦъ»ҜБЖЈЁКхәуЈ©
· ·Ҫ°ёЈәҝЁЕаЛыұхЈЁCapecitabine-basedЈ©· ДҝөДЈәКхәуҪөөНёҙ·ў·зПХЎЈ
ЈЁ2Ј©НнЖЪ/ЧӘТЖРФ №ГПў»ҜБЖ
· Т»ПЯЈәјӘОчЛыұх + ЛіІ¬ЈЁGemCisЈ©—— И«Зт№«ИПұкЧј·Ҫ°ёЈ»· ¶юПЯЈәFOLFOX·Ҫ°ёЈЁ5-FU+°ВЙіАыІ¬Ј©—— ФЪABC-06БЩҙІКФСйЦРұ»ЦӨКөУРР§ЎЈ
ЈЁ3Ј©ҫЦІҝЦОБЖЈЁёОДЪХјЦчөјЈ©
· ·ЕЙдЛЁИыЈЁRadioembolisationЈ©ЈәјҙTAREЈЁоЖ-90ОўЗтСЎФсРФДЪ·ЕЙдЦОБЖЈ©Ј¬ККУГУЪёОФаІЎФоОӘЦчЎўІ»ККәПКЦКх/ПыИЪөД»јХЯЎЈ4. ·ЦЧУМШХчЈЁMolecular CharacteristicsЈ©
ХвІҝ·ЦКЗ°РПтЦОБЖөДТАҫЭЈ¬АЁәЕДЪОӘОДПЧұЁөАөД·ўЙъВК·¶О§Јә
| »щТтұдТм | ·ўЙъВКЈЁФјЈ© | БЩҙІТвТе |
| FGFR2ИЪәПЈЁФӯОДРҙFGFR1-3Ј¬ө«iCCAТФFGFR2ИЪәПОӘЦчЈ© | 11-45% | ТСУР°РПтТ©ЈәЕеГЧМжДбЈЁPemigatinibЈ©ЎўУў·ЖёсАӯМжДбЈЁInfigatinibЈ©өИ |
| IDH1/2Н»ұд | 4.9-36% | ТСУР°РПтТ©Јә°¬·ьДбІјЈЁIvosidenibЈ© |
| TP53Н»ұд | 2.5-44.4% | ФӨәуҪПІоЈ¬іЈјыУЪHBVПа№ШөЁ№Ь°© |
| ARID1AН»ұд | 0.6-11% | ИҫЙ«ЦКЦШЛЬПа№Ш |
| PIK3CAН»ұд | 3-9% | ҝЙДЬУлPI3K/AKTНЁВ·јӨ»оУР№Ш |
| BRAFН»ұд | 3-7.1% | V600EН»ұдҝЙҝјВЗҙпАӯ·ЗДб+ЗъГАМжДб |
| ERBB3А©Фц | Фј7% | ЈЁERBBјТЧеЈ¬ЙЩјыЈ© |
| METА©Фц | 2-7% | ЙЩјыЈ¬ҝЙіўКФҝЁВнМжДбөИ |
ЧЬҪб
ДгМṩөДХв¶ОұКјЗВЯјӯЗеОъЈ¬°ҙ**БЩҙІБчРРІЎС§ЈЁОЈПХТтЛШЈ© → ·ЦІгЦОБЖЈЁёЁЦъЎўНнЖЪЎўҫЦІҝЈ© → °йЛжХп¶ПЈЁ»щТтН»ұдЈ©**ҪшРРКйРҙЈ¬»щұҫЙПКЗПЦҙъЦЧБцҝЖХл¶ФөЁөА°©өДНкХыХпБЖЛјВ·ЎЈ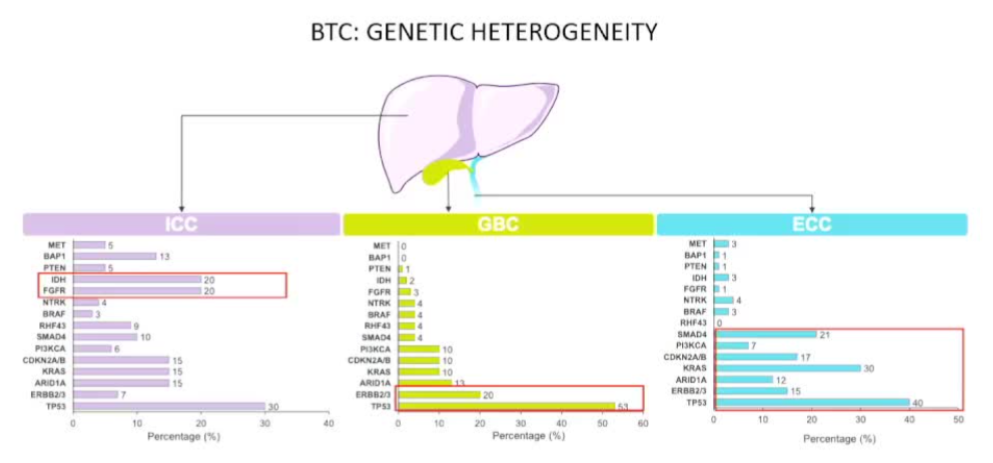
·ЦЧУ°РПтБЖ·ЁЈәөЁөА°©ЦОБЖөД“»ЖҪрКұҙъ”јҙҪ«өҪАҙ
өЁ№Ь°©ЦОБЖөДАъК·УлСЭұд
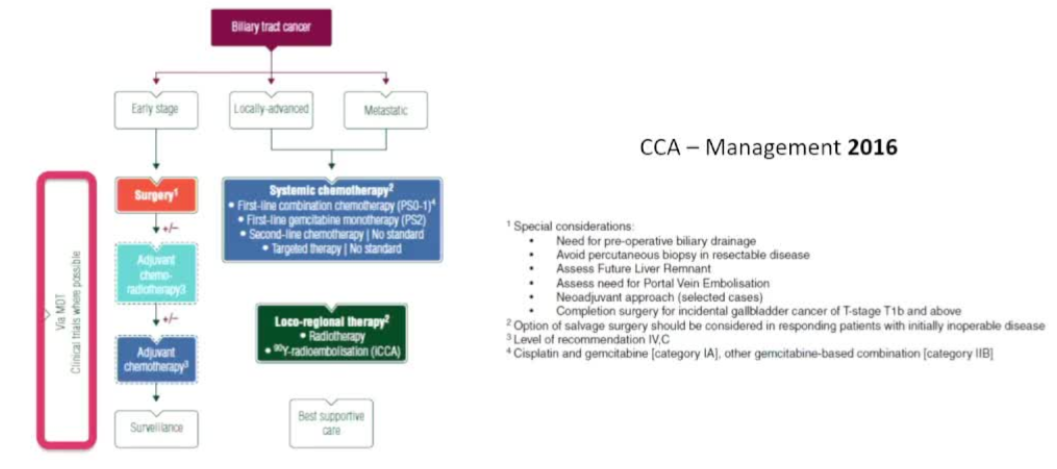
өЁөА°©ПөНіЦОБЖ·ўХ№КұјдПЯ
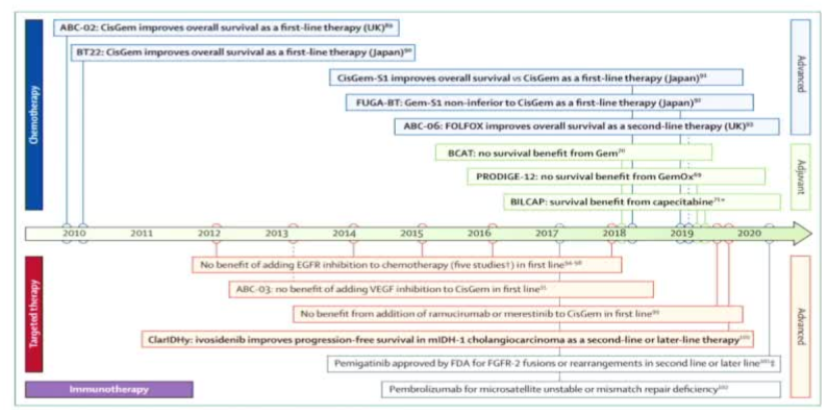
өЁ№Ь°© cholangiocarcinoma ЦОБЖөД№эИҘәНСЭұд
өЁ№Ь°©ЈЁCholangiocarcinomaЈ¬CCЈ©өДЦОБЖАнДоФЪ№эИҘјёК®ДкАпҫӯАъБЛЙоҝМұдёпЎЈЛьҙУЧоіхТФ»әҪв»ЖргОӘЦчТӘДҝұкөД№ГПўЦОБЖЈ¬ЦрІҪСЭұдОӘөұҪсТФНвҝЖёщЦОРФЗРіэОӘәЛРДЈ¬ІўХыәПБЛҫ«ЧјХп¶ПЎў¶аС§ҝЖЧЫәПЦОБЖЈЁMDTЈ©әНёцМе»Ҝ°РПт/ГвТЯЦОБЖөДёҙФУМеПөЎЈ
ФзЖЪҪЧ¶ОЈәіхІҪИПК¶Ул№ГПўЦОБЖЈЁФј1965Дк - 1990ДкҙъЈ©
1965ДкЈ¬ГА№ъС§ХЯKlatskinКЧҙОПөНіІыКцБЛёОГЕІҝөЁ№Ь°©ЈЁұ»іЖОӘKlatskinБцЈ©Ј¬ІўЦёіцХвАаЦЧБцФӨәуј«ІоЈ¬»јХЯ¶аЛАУЪёО№ҰДЬЛҘҪЯ»тСПЦШёРИҫ-1ЎЈЎЈФЪХвТ»КұЖЪЈ¬УЙУЪ¶ФёГІЎЙъОпС§РРОӘөДИПК¶УРПЮЈ¬јУЦ®Хп¶ПјјКхөДВдәуЈ¬ёщЦОРФЗРіэВКј«өНЎЈ
ЦОБЖөДЦчТӘДҝұкКЗ»әҪв№ЈЧиРФ»ЖргЈ¬ёДЙЖЙъ»оЦКБҝЈ¬СУіӨ¶МЖЪЙъҙжЎЈЦчТӘКЦ¶О°ьАЁёчЦЦөЁөАТэБчјх»ЖКЦКх»т·ЕЦГЦ§јЬЈ¬КфУЪ№ГПўРФЦОБЖ·¶іл-
ЎЈ
Хп¶ПУл·ЦЖЪөДҫ«Пё»ҜСЭҪш
ҫ«ЧјөДЦОБЖКјУЪҫ«ЧјөДХп¶ПЈ¬ХвКЗЦОБЖСЭұдөД»щКҜЎЈХп¶ПјјКхҙУДЈәэЧЯПтҫ«И·Ј¬ЦчТӘМеПЦФЪТФПВјёёц·ҪГжЈә
-
·ЦЧУұкЦҫОпөДУҰУГЈәМЗБҙҝ№Фӯ19-9ЈЁCA19-9Ј©әН°©ЕЯҝ№ФӯЈЁCEAЈ©іЙОӘХп¶ПәНФӨәуЕР¶ПөДЦШТӘСӘЗеС§ЦёұкЎЈСРҫҝ·ўПЦЈ¬ЖдЛ®ЖҪУлЦЧБц·ЦЖЪәНФӨәуГЬЗРПа№ШЎЈ
-
У°ПсС§өД·ЙФҫЈәХп¶ПјјКхҙУЧоіхөДі¬ЙщЙёІйЈ¬·ўХ№өҪФцЗҝCTЎўҙЕ№ІХсіЙПсЈЁMRIЈ©әНҙЕ№ІХсТИөЁ№ЬіЙПсЈЁMRCPЈ©ЎЈХвР©јјКхДЬёьЗеОъөШПФКҫЦЧБц·¶О§ЎўСӘ№ЬЗЦ·ёЗйҝцЈ¬КЗКхЗ°ҪшРР Bismuth-Corlette ·ЦРНәНЦЖ¶ЁКЦКх·Ҫ°ёөДЦчТӘТАҫЭ-ЎЈҪьДкАҙЈ¬ИэО¬ҝЙКУ»ҜЦШҪЁјјКхөДіцПЦЈ¬К№өГКхЗ°ҫ«И·ЖА№АФӨБфёОМе»эЎў№ж»®ёҙФУКЦКхВ·ҫ¶іЙОӘҝЙДЬЈ¬КЗҫ«ЧјНвҝЖөДЦШТӘЦ§іЕЎЈ-
-
·ЦЖЪПөНіөДёьРВЈә·ЦРНПөНіТІФЪІ»¶ПҪш»ҜТФёьәГөШЦёөјЦОБЖЎЈіэБЛҫӯөдөД Bismuth-Corlette ·ЦРНУГУЪЦёөјКЦКх·¶О§НвЈ¬TNM·ЦЖЪПөНіТІФЪІ»¶ПёьРВЎЈАэИзЈ¬өЪ8°ж AJCC TNM ·ЦЖЪҪ«Іҝ·ЦT4ЖЪЦЧБцҪөЖЪЈ¬·ҙУіБЛНвҝЖјјКхөДҪшІҪК№өГІҝ·Ц№эИҘИПОӘІ»ҝЙЗРіэөДЦЧБцПЦФЪУР»ъ»бКөПЦёщЦОЎЈН¬КұЈ¬ёьҫ«ПёөДMSKCC·ЦЖЪөИТІұ»МбіцЈ¬ТФЧЫәПЖА№АЦЧБцҝЙЗРіэРФЎЈ
НвҝЖЦОБЖІЯВФөДёпРВ
НвҝЖКЦКхКјЦХКЗөЁ№Ь°©ОЁТ»ҝЙДЬЦОУъөДКЦ¶ОЈ¬ө«ЖдАнДоәНјјКхТС·ўЙъҫЮҙуұд»ҜЎЈ
-
ҙУҫЦІҝЗРіэөҪёщЦОРФЗРіэЈәФзЖЪөҘҙҝөДҫЦІҝөЁ№ЬЗРіэКхТтЗРФөСфРФВКёЯЈ¬ёҙ·ўВКәНЛАНцВКҫУёЯІ»ПВЎЈЛжЧЕ¶ФЦЧБцСШөЁ№ЬҪюИуМШРФөДИПК¶јУЙоЈ¬НвҝЖТҪЙъИ·БўБЛR0ЗРіэЈЁПФОўҫөПВЗРФөТхРФЈ© ОӘКЦКхөДҪрұкЧјЎЈОӘБЛҙпөҪR0ЗРіэЈ¬КЦКх·ҪКҪЦрҪҘЧӘПтБӘәПҙу·¶О§ёОТ¶ЗРіэөДА©ҙуёщЦОКхЈ¬ЦјФЪі№өЧЗеіэПтёОДЪЗЦ·ёөДЦЧБцЎЈ
-
КхЗ°ЧјұёөДҫ«Пё»ҜЈә
-
ГЕҫІВцЛЁИыКхЈЁPVEЈ©Јә¶ФУЪРиТӘЗРіэҙуІҝ·ЦёОФаөД»јХЯЈ¬КхЗ°НЁ№эЛЁИыДвЗРіэІаөДГЕҫІВцЈ¬К№ұЈБфІаөДёОФаҙъіҘРФФцЙъЈ¬ҙУ¶шҪөөНКхәуёО№ҰДЬЛҘҪЯөД·зПХЎЈ
-
КхЗ°өЁөАТэБчЈә¶ФУЪ°йУРСПЦШ№ЈЧиРФ»ЖргөД»јХЯЈ¬КЗ·сТФј°ИзәОҪшРРКхЗ°јх»ЖЈЁИзPTCD»тENBDЈ©ЛдИФУРХщТйЈ¬ө«ТСіЙОӘҙҰАнёҙФУІЎАэКұөДЦШТӘҝјБҝЈ¬ТФёДЙЖ»јХЯ¶ФКЦКхөДДНКЬРФЎЈ
-
-
ОўҙҙјјКхөДМҪЛчЈәҫЎ№Ьё№З»ҫөёОГЕІҝөЁ№Ь°©ёщЦОКхТтЖдј«ёЯөДјјКхМфХҪРФ¶ш·ўХ№»әВэЈ¬ө«ТСФЪТ»Р©ҙуРНЦРРДЦрІҪҝӘХ№Ј¬ЦчТӘУГУЪМҪІй·ЦЖЪәНІҝ·ЦФзЖЪІЎАэөДіўКФЈ¬ҙъұнЧЕНвҝЖјјКхПтОўҙҙ·ҪПтөДМҪЛчЎЈ
ЧЫәПЦОБЖКұҙъөДөҪАҙ
Ҫь¶юК®ДкАҙЈ¬өЁ№Ь°©өДЦОБЖТСҙУөҘҙҝТАҝҝНвҝЖКЦКхЈ¬ВхИлБЛТФНвҝЖОӘЦчЎў¶аЦЦЦОБЖКЦ¶ОІўЦШөДЧЫәПЦОБЖКұҙъЎЈ
-
ПөНі»ҜБЖөДИ·БўУлҪшІҪЈә2010ДкЈ¬јӘОчЛыұхБӘәПЛіІ¬ЈЁGC·Ҫ°ёЈ© іЙОӘНнЖЪөЁ№Ь°©Т»ПЯ»ҜБЖөДұкЧј·Ҫ°ёЈ¬ПФЦшёДЙЖБЛ»јХЯөДЙъҙжЖЪЎЈФЪёЁЦъ»ҜБЖ·ҪГжЈ¬ҝЁЕаЛыұхөИТ©ОпөДУҰУГТІФЪБЩҙІКөјщЦРұ»№г·әІЙДЙЎЈГА№ъ№ъјТ°©ЦўКэҫЭҝвөДТ»ПоСРҫҝПФКҫЈ¬ФЪ2010ДкЦ®әуЈ¬ҪУКЬКЦКхЗ°әу»ҜБЖөД»јХЯұИАэҙУ39%ҙу·щФҫЙэЦБ70%Ј¬ХвЦұҪУНЖ¶ҜБЛөЁ№Ь°©»јХЯЦРО»ЧЬЙъҙжЖЪҙУ16ёцФВМбёЯөҪ27ёцФВ
-
°РПтЦОБЖУлГвТЯЦОБЖөДН»ЖЖЈә»щУЪЦЧБцЧйЦҜҪшРРөД·ЦЧУЖЧ·ЦОцЈ¬К№өГХл¶ФМШ¶Ё»щТтН»ұдөД°РПтЦОБЖіЙОӘҝЙДЬЎЈАэИзЈ¬Хл¶ФFGFR2ИЪәП»щТтәНIDH1Н»ұдөД°РПтТ©ОпЈ¬ТСФЪТ»Іҝ·ЦёОДЪөЁ№Ь°©»јХЯЦРПФКҫіцЧҝФҪөДБЖР§Ј¬ҝӘЖфБЛёцМе»ҜЦОБЖөДРВЖӘХВ-ЎЈ
-
ГвТЯЦОБЖЈәТФ¶И·ҘАыУИөҘҝ№»тЕБІ©АыЦйөҘҝ№ОӘҙъұнөДГвТЯјмІйөгТЦЦЖјБЈ¬БӘәПGC»ҜБЖ·Ҫ°ёЈ¬ТСұ»ЦӨКөДЬҪшТ»ІҪСУіӨНнЖЪ»јХЯөДЙъҙжЖЪЈ¬іЙОӘРВөДТ»ПЯЦОБЖұкЧјЎЈ
-
¶аС§ҝЖЧЫәПЦОБЖЈЁMDTЈ©ДЈКҪөДЖХј°ЈәДҝЗ°Ј¬ҙуРНТҪБЖЦРРДЖХұйІЙУГMDTДЈКҪЈ¬УЙёОөЁНвҝЖЎўЦЧБцДЪҝЖЎў·ЕБЖҝЖЎўҪйИлҝЖЎўІЎАнҝЖәНУ°ПсҝЖЧЁјТ№ІН¬ОӘ»јХЯЦЖ¶ЁёцМе»ҜөДЦОБЖ·Ҫ°ёЈ¬И·ұЈ»јХЯДЬ»сөГЧоИ«ГжЎўЧоәПАнөДЦОБЖ-
ЎЈ -
№ГПўЦОБЖөДҪшХ№Јә¶ФУЪОЮ·ЁЦОУъөДНнЖЪ»јХЯЈ¬іэБЛ»ҜБЖәН°РПтЦОБЖЈ¬ҪйИл·ЕЙдС§јјКхИзЙдЖөПыИЪЎўҫӯөј№Ь¶ҜВц»ҜБЖЛЁИыЈЁTACEЈ© өИЈ¬ТІОӘҝШЦЖҫЦІҝЦЧБцЎў»әҪвЦўЧҙЎўМбёЯЙъ»оЦКБҝМṩБЛёь¶аСЎФс-9
ЧЬҪб
өЁ№Ь°©өДЦОБЖФЪ№эИҘ°лёц¶аКАјНАпЈ¬ЧЯ№эБЛТ»МхҙУ“КшКЦОЮІЯ”өҪ“НвҝЖЦчөј”Ј¬ФЩөҪ“ЧЫәПК©ІЯ”өДСЭҪшЦ®В·ЎЈ
| О¬¶И | №эИҘ | ПЦФЪ |
|---|---|---|
| әЛРДАнДо | №ГПўјх»ЖЈ¬»әҪвЦўЧҙ | ёщЦОРФЗРіэОӘәЛРДЈ¬MDTЧЫәПЦОБЖ |
| НвҝЖКЦКх | ҫЦІҝЗРіэЈ¬R0ЗРіэВКөН | БӘәПёОТ¶ЗРіэөДА©ҙуёщЦОКхЈ¬ёЁТФPVEөИКхЗ°Чјұё |
| Хп¶ПУлЖА№А | ТААөі¬ЙщЎўCTЈ¬ЖА№АКЦ¶ОөҘТ» | MRI/MRCPЎўИэО¬ЦШҪЁЎў·ЦЧУұкЦҫОпЈ¬·ЦЖЪПөНіҫ«Пё»Ҝ |
| ПөНіЦОБЖ | »ҜБЖР§№ыУРПЮЈ¬СЎФсЙЩ | GC·Ҫ°ёОӘұкЧјЈ¬°РПтЎўГвТЯЦОБЖҙшАҙН»ЖЖЈ¬ПФЦшСУіӨЙъҙж |
| ЦОБЖДЈКҪ | өҘТ»ҝЖКТЦчөј | ¶аС§ҝЖНЕ¶УЈЁMDTЈ©№ІН¬ҫцІЯөДёцМе»Ҝҫ«ЧјТҪБЖ |
Из№ыДъ¶ФЖдЦРДіТ»ЦЦЦОБЖ·ҪКҪЈЁИз°РПтЦОБЖөДҫЯМеТ©ОпЈ©»тДіТ»АаРНөЁ№Ь°©өДЦОБЖПёҪЪёРРЛИӨЈ¬ОТГЗҝЙТФјМРшЙоИлМҪМЦЎЈ
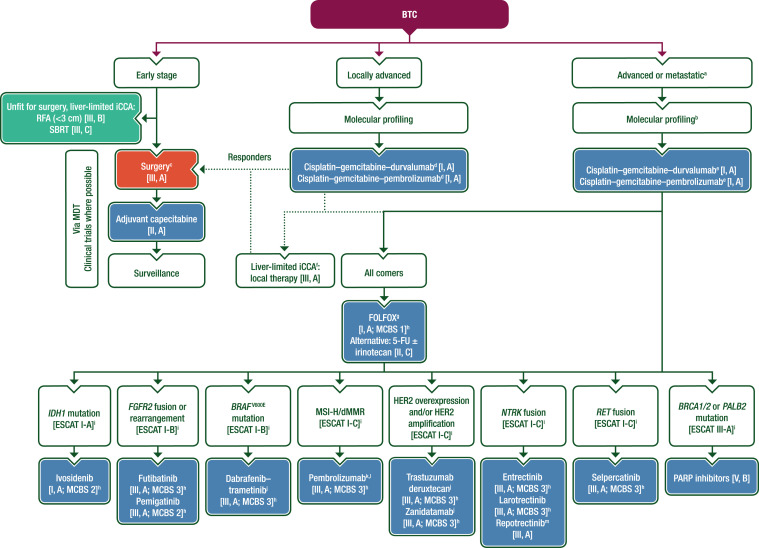
»щУЪABC-02БЩҙІКФСйҪб№ыЈ¬Ҫ«ЛіІ¬БӘәПјӘОчЛыұхИ·БўОӘНнЖЪөЁөА°©ұкЧјТ»ПЯ»ҜБЖ·Ҫ°ёЎЈ
1. КхУпІрҪвЈәЛьҙъұнКІГҙЈҝ
-
FIRST-LINE (Т»ПЯЦОБЖ)ЈәЦё¶ФУЪіхҙОХп¶ПОӘҫЦІҝНнЖЪ»тЧӘТЖРФЎўОЮ·ЁНЁ№эКЦКхЗРіэөДөЁөА°©»јХЯЈ¬ЛщІЙУГөДКЧСЎЎўЧоіхөДЦОБЖ·Ҫ°ёЎЈ
-
ABC-02ЈәХвКЗТ»ПоҫЯУРАпіМұ®ТвТеөД№ъјК¶аЦРРДЛж»ъIIIЖЪБЩҙІКФСйөДГыіЖЈЁAdvanced Biliary Tract Cancer-02Ј¬јҙНнЖЪөЁөА°©-02СРҫҝЈ©ЎЈёГКФСйөм¶ЁБЛДҝЗ°өЁөА°©»ҜБЖөД»щҙЎ1
-
CisGem (»т GemCis)ЈәХвКЗ»ҜБЖ·Ҫ°ёөДЛхРҙЎЈ
-
Cis ҙъұн CisplatinЈЁЛіІ¬Ј©
-
Gem ҙъұн GemcitabineЈЁјӘОчЛыұхЈ©
-
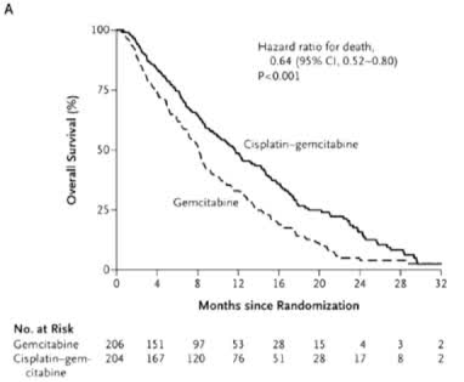
2. әЛРДТАҫЭЈәABC-02КФСйөД№Шјь·ўПЦ
ABC-02КФСйұИҪПБЛ“CisGemБӘәП·Ҫ°ё”Ул“GemөҘТ©·Ҫ°ё”өДБЖР§Ј¬ЖдҪб№ыИ·БўБЛCisGemЧчОӘИ«ЗтұкЧјЦОБЖөДөШО» -
ЎЈ
| Цёұк | CisGemБӘәП·Ҫ°ё | GemөҘТ©·Ҫ°ё | »сТжЛөГч |
|---|---|---|---|
| ЦРО»ЧЬЙъҙжЖЪ ЈЁOSЈ© | 11.7ёцФВ | 8.2ёцФВ | БӘәПЦОБЖПФЦшСУіӨБЛ»јХЯөДХыМеЙъҙжКұјд -1ЎЈ |
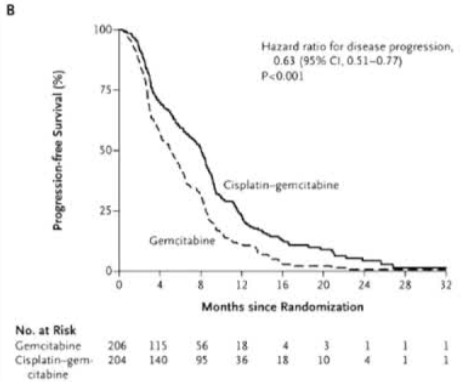
| ЦРО»ОЮҪшХ№ЙъҙжЖЪ ЈЁPFSЈ© | 8.5ёцФВ | 6.5ёцФВ |
БӘәПЦОБЖУРР§ҝШЦЖБЛЦЧБцөДҪшХ№- ЎЈ |
| ·зПХұИ ЈЁHRЈ© | 0.68 ЈЁ¶ФУЪOSЈ© | - | ХвТвО¶ЧЕПаұИөҘТ©Ј¬БӘәПЦОБЖҪөөНБЛ32% өДЛАНц·зПХ |
ҪбВЫЈәABC-02СРҫҝЦӨГчЈ¬¶ФУЪТ»°гЧҙҝцЙРҝЙЈЁECOGЖА·Ц0-1Ј©өДНнЖЪөЁөА°©»јХЯЈ¬CisGemБӘәП»ҜБЖІ»ҪцДЬПФЦшСУіӨЙъҙжЖЪЈ¬¶шЗТ¶ҫёұЧчУГҝЙҝШЈ¬ТтҙЛұ»И·БўОӘРВөД№ъјКұкЧјЦОБЖ·Ҫ°ё -1-2ЎЈ
 |
 |
3. БЩҙІУҰУГУлПЦЧҙ
-
ККУГИЛИәЈәЧоіхЦчТӘХл¶ФЙнМеЧҙҝцҪПәГЈЁECOGЖА·Ц0-1Ј©өДНнЖЪөЁөА°©»јХЯЈ¬°ьАЁёОДЪ/ёОНвөЁ№Ь°©ЎўөЁДТ°©өИ -1ЎЈәуРшСРҫҝТІМбКҫЈ¬¶ФУЪТтөЁөА№ЈЧиөјЦВ»ЖргөД»јХЯЈ¬ФЪід·ЦТэБчәуК№УГCisGemТІКЗ°ІИ«УРР§өД -3ЎЈ
-
АъК·өШО»ЈәФЪіӨҙпҪьК®ДкөДКұјдАпЈ¬CisGemКЗНнЖЪөЁөА°©ОЁТ»өДТ»ПЯұкЧјЦОБЖ·Ҫ°ё -2ЎЈ
-
өұЗ°·ўХ№ЈәҪьДкАҙЈ¬ОӘБЛҪшТ»ІҪМбЙэБЖР§Ј¬ФЪCisGem»щҙЎЙПБӘәПГвТЯЦОБЖЈЁИз¶И·ҘАыУИөҘҝ№»тЕБІ©АыЦйөҘҝ№Ј©өД“ИэБӘБЖ·Ё”ТСұ»ҙуРНБЩҙІКФСйЦӨКөР§№ыёьјСЈ¬іЙОӘБЛРВөДұкЧјТ»ПЯЦОБЖ -2-6ЎЈјҙұгИзҙЛЈ¬CisGemИФИ»КЗХыёцЦОБЖ·Ҫ°ёөДәЛРД»ҜБЖ№ЗјЬЎЈ
ЧЬҪбАҙЛөЈ¬“FIRST-LINE: ABC-02 (CisGem)” ТвО¶ЧЕ¶ФОЮ·ЁКЦКхөДНнЖЪөЁөА°©»јХЯЈ¬ІЙУГ»щУЪАпіМұ®КҪABC-02КФСйЛщИ·БўөДЛіІ¬+јӘОчЛыұхБӘәП»ҜБЖ·Ҫ°ёЧчОӘКЧСЎЦОБЖЎЈ
Из№ыДъПлБЛҪвөұЗ°ЧоРВөД“ЛіІ¬+јӘОчЛыұх+ГвТЯЦОБЖ”ИэБӘБЖ·ЁЈ¬»тХЯ¶ФЖдЛы·ҪГжёРРЛИӨЈ¬ЛжКұҝЙТФёжЛЯОТЎЈ